-
回答下列问题:
1L海水在逐渐浓缩过程中析出盐的种类和质量(单位:g)的关系如下表所示:
海水密度(g∙mL-1)
CaSO4
NaCl
MgCl2
MgSO4
NaBr
1.21
0.05
3.26
0.004
0.008
—
1.22
0.015
9.65
0.01
0.012
—
1.26
0.01
2.64
0.02
0.02
0.04
1.31
—
1.40
0.54
0.03
0.06
注:画“—”的数据少于10-4,可以忽略不计。
(1)从海水中获得粗盐,一般采用的方法是___。
(2)根据上表,要获得杂质较少的食盐,应控制海水的最佳密度为___g∙mL-1(填字母)。
A.1.21 B.1.22 C.1.26 D.1.31
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,要除去这些杂质,按顺序加入的试剂依次为NaOH、BaCl2、___、___等(填化学式)。
(4)工业上电解熔融氯化钠制取金属钠的化学方程式为___。
(5)钠元素的一种常见氧化物可作为呼吸面具的供氧剂,写出该氧化物和CO2反应的化学方程式___。
高一化学解答题中等难度题查看答案及解析
-
海洋是“聚宝盆”,工业上,人们直接从海水中得到食盐。海水在浓缩过程中析出盐类物质的种类和质量,如下表:
海水密度(g/L)
CaSO4
NaCl
MgCl2
MgSO4
NaBr
1.13
0.56
1.20
0.91
1.21
0.05
3.26
0.004
0.008
1.22
0.015
9.65
0.01
0.04
1.26
0.01
2.64
0.02
0.02
0.04
1.31
1.40
0.54
0.03
0.06
(1)常采用____________的方法从海水中得到食盐。
(2)为得到含杂质较少的食盐,实际生产中卤水的密度控制在_____之间。
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,通常在实验室中依次加入_________、__________、___________、___________等四种物质除去杂质。(填化学式)
(4)电解饱和食盐水可以制取氯气,同时得到几种重要的化工产品,
该反应的化学方程式为_________________________________________。通电时阳极产物是__________该产物的检验方法是___________________________________________
(5)电解过程中得到气体物质还可以化合为HCl,在实验室中我们利用_________________和_____________ 反应(写名称)来制取。该气体__________________溶于水,可以做喷泉实验。写出氯化氢气体溶于水后的电离方程式_____________________________________
(6)新制的氯水显_______色,这是因为氯水中有__________(填微粒符号)存在。向氯水中滴入几滴AgNO3溶液,观察到的现象是____________________________,发生变化的化学方程式为______________________________________________。蓝色石蕊试纸遇到氯水后的现象是___________________________,氯气有毒,不能直接排放到空气中,需要用________________________来吸收,写出反应的化学方程式为_________________________________________
高一化学综合题中等难度题查看答案及解析
-
将铁粉和铝粉的混合物逐渐加入100mL的稀硝酸中,其产生的有关离子浓度与加入铁粉和铝粉的混合物的质量的关系如下图所示:
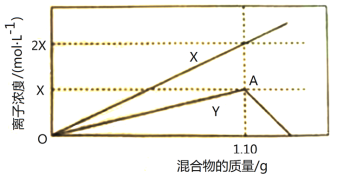
若反应过程中生成的气体为NO,溶液的体积变化忽略不计。请回答下列问题:
(1)X表示的变化离子是_______________(填离子符号)。
(2)OA段发生反应的离子方程式是___________________________________。
(3)稀硝酸溶解1.10g铁粉和铝粉后溶液还能继续溶解混合物的原因是________________
(4)该硝酸的浓度是_____________mol·L-1。
高一化学推断题中等难度题查看答案及解析
-
一定量的质量分数为14%的KOH溶液,若蒸发掉100g水后,其质量分数变为28%,体积为125mL,且蒸发过程中无晶体析出,则浓缩后的KOH溶液的物质的量浓度为( )
A.2.2 mol•L-1
B.4 mol•L-1
C.5 mol•L-1
D.6.25 mol•L-1高一化学选择题中等难度题查看答案及解析
-
把100g某NaOH溶液(密度为1.22g/cm3),蒸发浓缩至50mL时物质的量浓度为8mol/L(蒸发浓缩时无固体析出),则原溶液用下列方式表示正确的是( )
①160g/L ②3.28mol/L ③4.88mol/L ④16%
A. ① B. ②④ C. ③④ D. ①③
高一化学单选题中等难度题查看答案及解析
-
质量分数为a%,物质的量浓度为cmol/L的NaCl溶液,蒸发溶剂,恢复到原来的温度,若物质的量浓度变为2cmol/L,则质量分数为(蒸发过程中没有晶体析出,且NaCl溶液的密度大于1g/mL)
A.等于2a% B.大于2a% C.小于2a% D.无法确定
高一化学选择题困难题查看答案及解析
-
现用质量分数为98%.密度为1.84 g/ml的浓硫酸来配制500ml0.2mol/l的稀硫酸,可供选择的仪器如下;①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙请回答下列问题。
(1)上述仪器中,在配制稀硫酸时用不到的仪器有________(填序号)
(2)经计算,需浓硫酸的体积为________。现有①10ml.②50ml.③100ml三种规格的量筒,你选用的量筒是________(填序号)
(3)将浓硫酸稀释后,冷却片刻,随后全部转移到________ml的容量瓶中,转移时应用玻璃棒________,转移完毕后,用少量蒸馏水洗涤烧杯玻璃棒2~3次,并将洗涤液也转入容量瓶中,在加适量蒸馏水直到液面接近刻线________处。改用________滴加蒸馏水到瓶颈刻度的地方,将溶液振荡,摇匀后,装瓶,贴签。
高一化学填空题简单题查看答案及解析
-
海水晒盐的原理( )
A.利用热蒸发浓缩海水达饱和并进一步结晶
B.通过降温降低食盐的溶解度使食盐析出
C.利用加入沉淀剂的方法是食盐沉淀析出
D.利用泥沙使海水达到饱和,然后利用日光使食盐析出
高一化学选择题简单题查看答案及解析
-
实验室需要250mL 0.5mol/L的稀硫酸溶液,现用密度为1.84g/mL,质量分数为98%浓硫酸配制;填空并请回答下列问题:
(1)请先通过计算(要有计算过程),再确定量取______mL浓硫酸.
(2)下列仪器中,不会用到的是______
A.250mL容量瓶; B.500mL容量瓶; C.托盘天平; D.10mL量筒; E.玻棒;
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是______.
(4)容量瓶在使用前必须进行的操作是______.
(5)配制过程简述为以下各步:其正确的操作顺序为______(填各步骤序号).A.冷却; B.洗涤; C.量取; D.溶解; E.定容; F.摇匀; G.移液
(6)在配制过程中,定容时若俯视刻度线,则所配溶液的浓度偏______(填“高”或“低”); 若在滴加蒸馏水时,不慎超过了刻度线,应如何处理?______.高一化学解答题中等难度题查看答案及解析
-
用质量分数为98%的浓硫酸配制100ml 3.0mol/L 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀
回答下列问题
(1)若所用浓硫酸密度为1.84g/cm3,则该浓硫酸的物质的量浓度为______,配制上述稀硫酸所需浓硫酸的体积是______(小数点后保留一位),量取浓硫酸所用的量筒的规格是______(从下列中选用A.10ml B.20ml
C.50ml D.100ml)
(2)第⑤步实验的操作是______
(3)为了保证实验的准确性,在第③和第④步操作之间还应该加多一步什么操作______,如果在配制溶液过程中出现下列情况对所配稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水______
B.所用过的烧杯、玻璃棒未洗涤______
C.定容时仰视容量瓶刻度线______.高一化学解答题中等难度题查看答案及解析