目前环境问题已有多种解决方案,垃圾是放错地方的财富,上海实行垃圾分类的措施获得一致好评,某科研小组利用惰性电极和离子交换膜对厨房垃圾发酵液进行直流电渗析法处理可得到乳酸(HA),其原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )

A.电子从电源a极流到c极,从d极流入电源b极
B.离子交换膜B为阳离子交换膜
C.通电后,左室的pH会上升
D.c电极发生的反应为:2H2O-4e-=4H++O2↑
高二化学单选题中等难度题
目前环境问题已有多种解决方案,垃圾是放错地方的财富,上海实行垃圾分类的措施获得一致好评,某科研小组利用惰性电极和离子交换膜对厨房垃圾发酵液进行直流电渗析法处理可得到乳酸(HA),其原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )

A.电子从电源a极流到c极,从d极流入电源b极
B.离子交换膜B为阳离子交换膜
C.通电后,左室的pH会上升
D.c电极发生的反应为:2H2O-4e-=4H++O2↑
高二化学单选题中等难度题
目前环境问题已有多种解决方案,垃圾是放错地方的财富,上海实行垃圾分类的措施获得一致好评,某科研小组利用惰性电极和离子交换膜对厨房垃圾发酵液进行直流电渗析法处理可得到乳酸(HA),其原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )

A.电子从电源a极流到c极,从d极流入电源b极
B.离子交换膜B为阳离子交换膜
C.通电后,左室的pH会上升
D.c电极发生的反应为:2H2O-4e-=4H++O2↑
高二化学单选题中等难度题查看答案及解析
垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。实验方案如下:
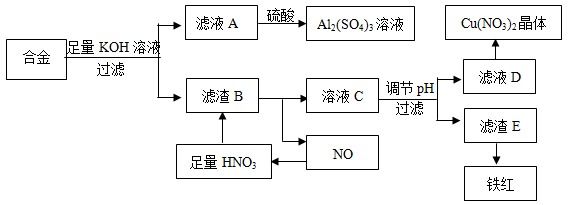
(1)滤渣B中发生反应的离子反应方程式为: ; 。
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全。下列物质中可用作调整溶液C的pH的试剂是 (填序号)。
A.铜粉 B.氨水 C.氢氧化铜 D.碱式碳酸铜
(3)常温,若溶液C中金属离子均为1mol·L-1,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]= 2.2×10-20。控制pH=4,溶液中c(Fe3+)= mol·L-1。
(4)将20mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液70mL混合,反应的离子方程为 。
(5)在0.1L的混合酸溶液中,c(HNO3)=2mol·L-1,c(H2SO4)=3mol·L-1,将0.3mol的铜放入加热充分反应后,所得溶液的溶质的物质的量浓度为 。(溶液体积不变)
高二化学实验题极难题查看答案及解析
(10分)某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。
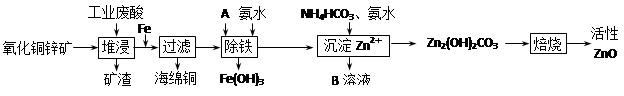
已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
⑴氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)________ Ksp(ZnS)(选填“>”“<”或“=”)(Ksp 沉淀离子浓度积)。
⑵物质A可使用下列物质中的________。
A.KMnO4 B.O2 C.H2O2 D.Cl2
⑶除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在________范围之间。
⑷物质B可直接用作氮肥,则B的化学式是________。
高二化学填空题简单题查看答案及解析
(12分)某科研小组设计出利用工业废酸(稀H2SO4)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。
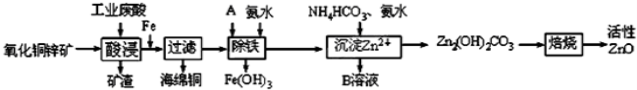
已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是 。(任写一点即可)
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:
Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(3)物质A最好使用下列物质中的 。
A.KMnO4 B.空气 C.HNO3 D.NaClO
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(5)物质B可直接用作氮肥,则B的化学式是 。
(6)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂——K2FeO4,写出该反应的离子方程式 。
高二化学填空题困难题查看答案及解析
(10分)垃圾是放错地方的资源,工业废料也可以再利用。某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3)。实验方案如下:
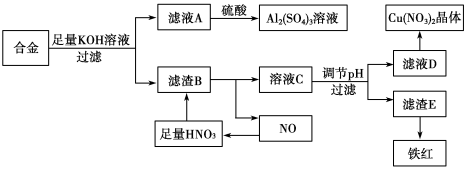
(1)写出滤液A中加入足量硫酸后所发生反应的离子方程式:__________________。
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全。下列物质中可用作调整溶液C的pH的试剂是________(填序号)。
A.铜粉 B.氨水 C.氢氧化铜 D.碳酸铜
(3)常温,若溶液C中金属离子均为1 mol·L-1,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20。控制pH=4,溶液中c(Fe3+)=____________,此时________Cu(OH)2沉淀生成(填“有”或“无”)。
(4)将20 mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液80 mL混合,反应的离子方程式为_______________。
高二化学实验题困难题查看答案及解析
某科研小组设计出利用工业废酸(稀硫酸)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示。
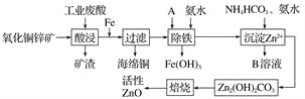
已知:各离子开始沉淀及完全沉淀时的pH如表所示:
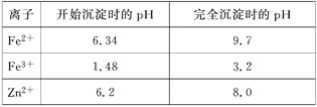
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是(任写一点即可)__________________________________________________________。
(2)物质A最好使用下列物质中的____________(填选项序号)。
A.KMnO4 B.H2O2 C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在__________范围之间。
(4)物质B可直接用作氮肥,则B的化学式是________。
(5)除铁后得到的氢氧化铁可用次氯酸钾溶液在碱性环境将其氧化得到一种高效的多功能处理剂(K2FeO4),写出该反应的离子方程式:__________________________。
高二化学实验题困难题查看答案及解析
(14分))某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如下图所示。
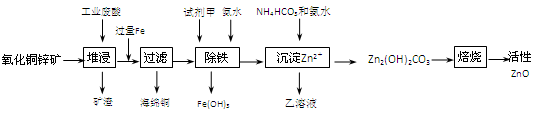
已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS
不溶,这是由于相同温度下:Ksp(CuS)________ Ksp(ZnS)(选填“>”“<”或“=”)。
(2)你认为在除铁过程中选用下列物质中的________(填序号)作为试剂甲是比较合适的。
A.KMnO4 B.HNO3 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在________范围之间。
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方程式________。
(5)298K时,残留在乙溶液中的c(Fe3+)在 __________ mol/L以下。
[Fe(OH)3的= 2.70×10-39]
(6)乙的溶液可直接用作氮肥,则乙的化学式是________。
(7)请写出“沉淀Zn2+”步骤中发生反应的化学方程式________。
高二化学填空题简单题查看答案及解析
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿,提取锌、铜元素,实现废物综合利用,方案如图所示:
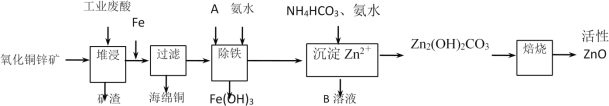
已知:各离子开始沉淀及完全沉淀时的pH如表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)加入A物质的目的是___,物质A可使用下列物质中的___。
A.KMnO4 B.O2 C.H2O2 D.Cl2
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)___Ksp(ZnS)(选填“>”“<”或“=”)。
(3)反应生成海绵铜的离子方程式:___。
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在___范围之间。
(5)写出NH4HCO3溶液与Zn2+反应生成Zn2(OH)2CO3的离子方程式:___。
(6)物质B可用作生产化肥,其化学式是___。
高二化学工业流程中等难度题查看答案及解析
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿,提取锌、铜元素,实现废物综合利用,方案如图所示:
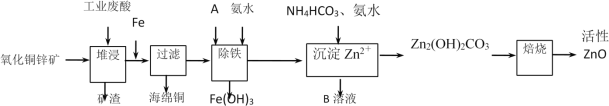
已知:各离子开始沉淀及完全沉淀时的pH如表所示。
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)加入A物质的目的是___,物质A可使用下列物质中的___。
A.KMnO4 B.O2 C.H2O2 D.Cl2
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)___Ksp(ZnS)(选填“>”“<”或“=”)。
(3)反应生成海绵铜的离子方程式:___。
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在___范围之间。
(5)写出NH4HCO3溶液与Zn2+反应生成Zn2(OH)2CO3的离子方程式:___。
(6)物质B可用作生产化肥,其化学式是___。
高二化学工业流程中等难度题查看答案及解析
燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述错误的是
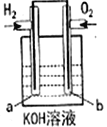
A. a电极是负极,该电极上发生氧化反应
B. b极反应是O2+2H2O-4e-=4OH-
C. 总反应方程式为2H2+O2=2H2O
D. 使用过程中电解质溶液的pH逐渐减小
高二化学单选题简单题查看答案及解析