-
氨在国民经济中占有重要地位。
(1)已知:





则 的
的 ________。
________。
(2) 的活化能
的活化能 ,则氨分解反应:
,则氨分解反应: 的活化能
的活化能 ________。
________。
(3)我国科学家以 为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。
为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。
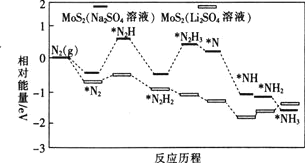
 在________
在________ 填“
填“ ”或“
”或“ ”
” 溶液中催化效果更好;在
溶液中催化效果更好;在 溶液与
溶液与 溶液中,
溶液中, 反应中的
反应中的 ________
________ 填“前者大”“后者大”或“一样大”
填“前者大”“后者大”或“一样大” 。
。
(4) 时,在一体积为2L的恒容刚性密闭容器中发生反应:
时,在一体积为2L的恒容刚性密闭容器中发生反应: 。改变反应的一个条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质的物质的量随时间变化的曲线如图所示:
。改变反应的一个条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质的物质的量随时间变化的曲线如图所示:
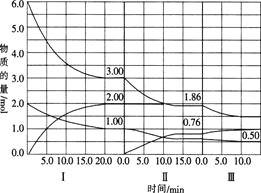
① 内,
内, ________
________ 。
。
② 时,第Ⅰ阶段的平衡常数
时,第Ⅰ阶段的平衡常数 为________
为________ 保留2位有效数字
保留2位有效数字 。
。
③第Ⅱ阶段平衡时 与
与 的物质的量之比为________。
的物质的量之比为________。
④比较第Ⅱ阶段平衡常数 和第Ⅲ阶段平衡常数
和第Ⅲ阶段平衡常数 的大小:
的大小: ________
________ 填“
填“ ”“
”“ ”或“
”或“ ”
” ,判断的依据是____________________。
,判断的依据是____________________。
-
甲烷和氨在国民经济中占有重要地位。
(1)制备合成氨原料气H2,可用甲烷蒸汽转化法,主要转化反应如下:
CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH = +206.2 kJ/mol
CO(g) + 3H2(g) ΔH = +206.2 kJ/mol
CH4(g) + 2H2O(g)  CO2(g) +4H2(g) ΔH = +165.0kJ/mol
CO2(g) +4H2(g) ΔH = +165.0kJ/mol
上述反应所得原料气中的CO能使氨合成催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是________。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
① 反应热ΔH(填“>”、“<”或“=”)_______0。
② 在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。

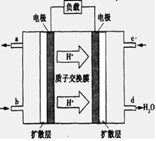
(3)已知甲烷燃料电池的工作原理如下图所示。该电池工作时,a口放出的物质为_________,该电池正极的电极反应式为:____ ,工作一段时间后,当3.2g甲烷完全反应生成CO2时,有________mol 电子发生转移。
-
催化剂在现代化学工业中占有极其重要的地位,主要涉及过渡元素及其化合物、硅、铝化合物等。中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。
(1)硅、碳位于同一主族,用“>”“<”或“=”填空:
| 性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
| 项目 | ①Si__________C | ②C_________Si | ③CO2______SiO2 | ④H-Si_______H-C |
(2)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有_____________(任写一种);1mol[Fe(CN)6]3-中含____________mol σ键。
(3)已知:反应2CH4 CH2=CH2+2H2,碳原子的杂化类型转化过程为___________;
CH2=CH2+2H2,碳原子的杂化类型转化过程为___________;
(4)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________方法区分晶体、准晶体和非晶体。
(5)基态F原子的价层电子排布图为___________。
(6)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为____________。
(7)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
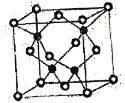
①CuF的熔点比CuCl的高,原因是____________________________________________。
②已知NA为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数a=__________nm(列出计算式)。
-
氨在国民经济中占有重要地位。
I.合成氨工业中,初始时氮气、氢气的体枳比为1:3时,每反应1mol N2,放出92.2kJ热量。
(1)工业合成氨的热化学方程式是_________________。
(2)如图为合成氨反应在不同温度和压强、使用相同催化剂条件下,平衡混合物中氨的体积分数。

①由图可知:p1、p2、p3的大小关系为____________,理由是___________________。
②A、B点生成氨气的速率大小关系为____________________。B、C点,合成氨反应的化学平衡常数大小关系为__________,C点,N2的转化率为_____。③下列关于合成氨的说法正确是______(填序号)。
A.断开1个N=N键的同时有6个N—H键形成,反应一定达到平衡状态
B.混合气体的平均相对分子质量不再改变状态,反应一定达到平衡状态
C.由于△H<0、△S>0,故合成氨反应一定能自发进行
D.增大n(N2):n(H2)的比值,有利用提离H2的转化率
II.最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。其电池反应为4NH3+3O2==2N2+6H2O,你认为电解质溶液应显_______(填“酸性”“中性”或“碱性”),写出负极的电极反应式:_________。若电池产生的电流为1A,反应时间为1小时,氨气的转化率为80%,则最低需要______mol氨气(列出计算式即可,已知一个电子的电量是1.6×10-19C)。
-
氨在国民经济中占有重要地位.请回答有关氨的下列问题:
(1)已知:N2(g)+O2(g)═2NO(g)△H=+akJ/mol
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-bkJ/mol
2H2(g)+O2(g)═2H20(g)△H=-ckJ/mol
则N2(g)+3H2(g)⇌2NH3(g)的△H=________;
(2)在一定温度下,将3molN2气体和7molH2气体通入到体积为1L的密闭容器中.当反应达到平衡时,容器内气体的压强为起始时的80%,则其平衡常数为________.改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是________;
①增大压强 ②增大反应物质的浓度 ③使用催化剂 ④降低温度
(3)可以用氯气来检验输送氨气的管道是否漏气,如果漏气则会有白烟(成份为氯化铵)生成.该反应的化学方程式为________;
(4)工业生产氨水的物质的量浓度为20mol/L,实验室若需用80mL浓度为5mol/L的氨水时,需取20mol/L的氨水________mL(用100mL的容量瓶).假如该氨水的pH=a,加入相同体积的盐酸时,两溶液恰好反应,则此盐酸的pH________14-a(填“大于”“小于”或“等于”).
-
氨在国民经济中占有重要地位。
(1)工业合成氨时,合成塔中每产生1 mol NH3,放出46.1 kJ的热量。
① 工业合成氨的热化学方程式是________。
② 已知:
N2 (g) 2N (g)
2N (g)
H2 (g) 2H (g)
2H (g)
则断开1 mol N-H键所需的能量是_______kJ。
(2)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
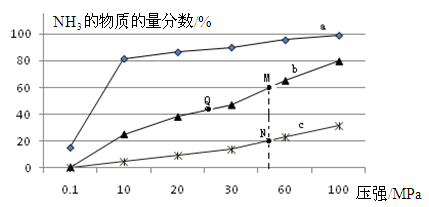
① 曲线a对应的温度是________。
② 关于工业合成氨的反应,下列叙述正确的是________(填字母)。
A. 及时分离出NH3可以提高H2的平衡转化率
B. 加催化剂能加快反应速率且提高H2的平衡转化率
C. 上图中M、N、Q点平衡常数K的大小关系是K(M)= K(Q) >K(N)
③ M点对应的H2转化率是________。
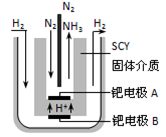 (3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)。
则该燃料电池的负极反应式是________。
-
碘及其化合物在人类活动中占有重要地位。已知反应H2(g) + I2(g) 2HI(g) ΔH=﹣11 kJ·mol-1。716K时,在一密闭容器中按物质的量比1:1充入H2(g)和I2(g),测得气体混合物中碘化氢的物质的量分数与反应时间的关系如下图:
2HI(g) ΔH=﹣11 kJ·mol-1。716K时,在一密闭容器中按物质的量比1:1充入H2(g)和I2(g),测得气体混合物中碘化氢的物质的量分数与反应时间的关系如下图:
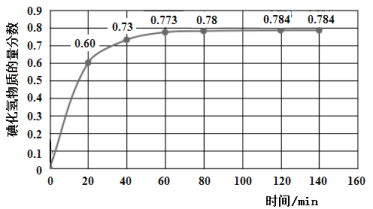
(1)若反应开始时气体混合物的总压为p kPa,则反应在前20 min内的平均速率 (HI)=_____kPa·min-1(用含p的式子表示)。
(HI)=_____kPa·min-1(用含p的式子表示)。
(2)反应达平衡时,H2的转化率α(H2)=____________。
(3)上述反应中,正反应速率为v正= k正·c(H2)·c(I2),逆反应速率为v逆=k逆·c2(HI),其中k正、k逆为速率常数。升高温度, ________(填“增大”“减小”或“不变”)。
________(填“增大”“减小”或“不变”)。
(4)降低温度,平衡可能逆向移动的原因是__________。
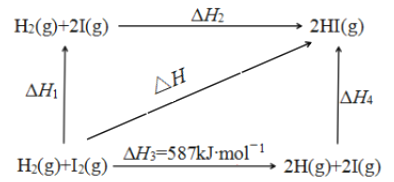
(5)1 mol H2(g)分子中化学键断裂时需要吸收436 kJ的能量,下图中的ΔH2=________kJ∙mol-1

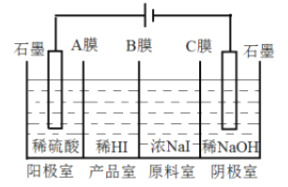
(6)氢碘酸可用“四室式电渗析法”制备,电解装置及起始的电解质溶液如上图所示。
①阳极电极反应式为______________。
②阳膜和阴膜分别只允许阳离子、阴离子通过,A膜为阳膜,则B膜为______膜,C膜为______膜。
-
碘及其化合物在人类活动中占有重要地位。已知反应H2(g) + I2(g) 2HI(g) ΔH=﹣11 kJ·mol-1。716K时,在一密闭容器中按物质的量比1:1充入H2(g)和I2(g),测得气体混合物中碘化氢的物质的量分数与反应时间的关系如下图:
2HI(g) ΔH=﹣11 kJ·mol-1。716K时,在一密闭容器中按物质的量比1:1充入H2(g)和I2(g),测得气体混合物中碘化氢的物质的量分数与反应时间的关系如下图:
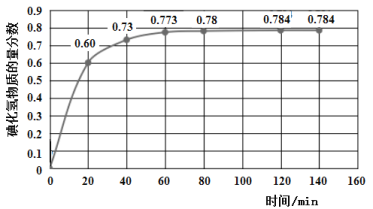
(1)若反应开始时气体混合物的总压为p kPa,则反应在前20 min内的平均速率 (HI)=_____kPa·min-1(用含p的式子表示)。
(HI)=_____kPa·min-1(用含p的式子表示)。
(2)反应达平衡时,H2的转化率α(H2)=____________。
(3)上述反应中,正反应速率为v正= k正·c(H2)·c(I2),逆反应速率为v逆=k逆·c2(HI),其中k正、k逆为速率常数。升高温度, ________(填“增大”“减小”或“不变”)。
________(填“增大”“减小”或“不变”)。
(4)降低温度,平衡可能逆向移动的原因是__________。
(5)1 mol H2(g)分子中化学键断裂时需要吸收436 kJ的能量,下图中的ΔH2=________kJ∙mol-1
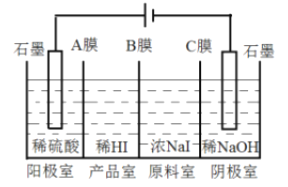
(6)氢碘酸可用“四室式电渗析法”制备,电解装置及起始的电解质溶液如上图所示。
①阳极电极反应式为______________。
②阳膜和阴膜分别只允许阳离子、阴离子通过,A膜为阳膜,则B膜为______膜,C膜为______膜。
-
氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)已知反应NO2(g)+CO(g) = NO(g) +CO2(g)的能量变化如图所示,下列说法正确的是________。
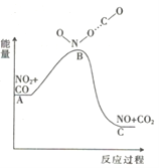
A.图中A→B的过程为放热过程
B.1molNO2和1molCO的键能总和大于1molNO和1mol CO2 的键能总和
C.该反应为氧化还原反应
D.1molNO2(g)和1molCO(g)的总能量低于1mol NO(g) 和1mol CO2(g)的总能量
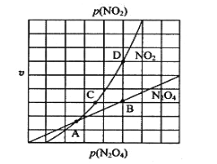
(2)N2O4与NO2之间存在反应N2O4(g) 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
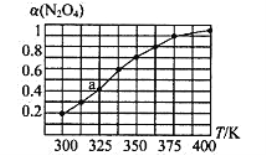
①由图推测该反应的△H___0(填“>”或“<”),理由为________________。
②图中a点对应温度下,已知N2O4的起始压强为108 kPa,则该温度下反应的平衡常数Kp=_________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
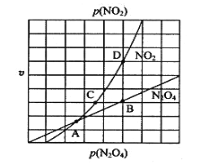
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系v( N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=___________,在下左图上标出的点中,能表示反应达到平衡状态的点为__________(填字母代号)。
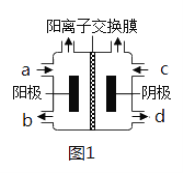
(3)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
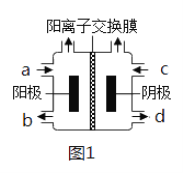
①收集到(CH3)4NOH的区域是______(填a、b、c或d)。
②写出电解池总反应(化学方程式)___________________________。
-
氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)已知反应NO2(g)+CO(g) = NO(g) +CO2(g)的能量变化如图所示,下列说法正确的是________。
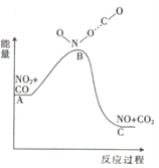
A.图中A→B的过程为放热过程
B.1molNO2和1molCO的键能总和大于1molNO和1mol CO2 的键能总和
C.该反应为氧化还原反应
D.1molNO2(g)和1molCO(g)的总能量低于1mol NO(g) 和1mol CO2(g)的总能量
(2)N2O4与NO2之间存在反应N2O4(g) 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。

①由图推测该反应的△H___0(填“>”或“<”),理由为________________。
②图中a点对应温度下,已知N2O4的起始压强为108 kPa,则该温度下反应的平衡常数Kp=_________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系v( N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=___________,在下左图上标出的点中,能表示反应达到平衡状态的点为__________(填字母代号)。
(3)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
①收集到(CH3)4NOH的区域是______(填a、b、c或d)。
②写出电解池总反应(化学方程式)___________________________。
的
________。
的活化能
,则氨分解反应:
的活化能
________。
为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。

在________
填“
”或“
”
溶液中催化效果更好;在
溶液与
溶液中,
反应中的
________
填“前者大”“后者大”或“一样大”
。
时,在一体积为2L的恒容刚性密闭容器中发生反应:
。改变反应的一个条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质的物质的量随时间变化的曲线如图所示:

内,
________
。
时,第Ⅰ阶段的平衡常数
为________
保留2位有效数字
。
与
的物质的量之比为________。
和第Ⅲ阶段平衡常数
的大小:
________
填“
”“
”或“
”
,判断的依据是____________________。




 (3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:












