-
实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图:
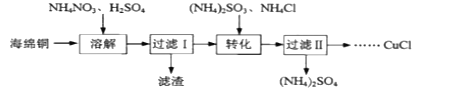
已知:①CuCl为白色固体,难溶于水和乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl有水存在时在空气中易被氧化,在酸性条件下较稳定。
(1)“溶解”时选用约为0.5mol•L-1的硫酸,过程中无气体产生。若硫酸浓度过大,反应会产生NO、NO2等有害气体,NH4NO3的用量会___(填“增大”或“减小”或“不变”)。
(2)“转化”步骤中发生反应的离子方程式为___。加入的(NH4)2SO3需要适当过量的原因是__。
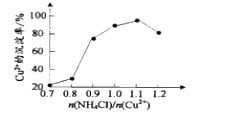
(3)氯化铵用量[ ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是___。
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是___。
(4)检验CuCl沉淀是否洗涤完全的方法是___。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:__。(实验中可选试剂:0.1mol•L-1盐酸、10mol•L-1盐酸、蒸馏水、无水乙醇)
-
氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:
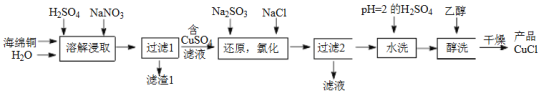
(1)“溶解浸取”时,需将海绵铜粉碎成细颗粒,其目的是___________。
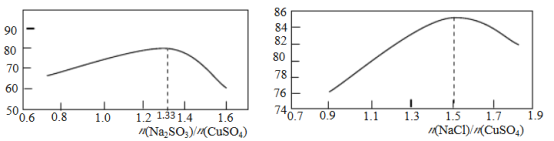
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图所示:
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为___________。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是___________。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是___________。
(3)“粗产品”用pH=2的H2SO4水洗,若不慎用稀硝酸进行稀释,则对产品有何影响___________。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为______________________。
(5)某同学拟测定产品中氯化亚铜的质量分数。实验过程如下:准确称取制备的氯化亚铜产品1.600g,将其置于足量的FeCl3溶液中,待样品全部溶解后,加入适量稀硫酸,用0.2000mol·L-1的KMnO4标准溶液滴定到终点,消耗KMnO4溶液15.00mL,反应中MnO4-被还原为Mn2+,则产品中氯化亚铜的质量分数为______________________。
-
CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下: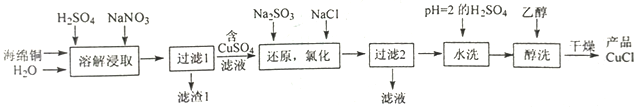
(1)“溶解浸取”时,下列措施不能提高铜的浸取率的是__________(填序号)。
a.将海绵铜粉末与水搅拌成浆液 b.投料时,NaNO3适当过量
c.缩短浸取时间 d.将滤渣1返回再次溶解浸取
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如 图-1、图-2所示:
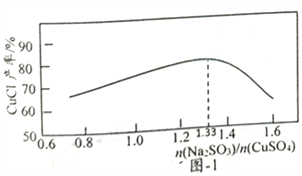
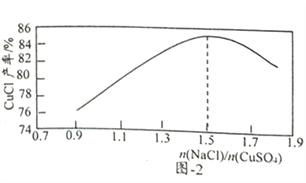
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离了方程式为__________。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是__________。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是__________。
(3)“过滤2”所得滤液中溶质的主要成分为__________(填化学式)。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl 的化学方程式为__________。
-
氯化亚铜(CuCl)广泛应用于化工等行业,其难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺流程如图所示:

下列说法正确的是
A.步骤①,为加快海绵铜的溶解速度,可将其进行适当粉碎并用大火持续加热
B.步骤③主要离子方程式:H2O+2Cu2++SO32-+2Cl-=CuCl↓+SO42-+2H+
C.步骤⑤包括用pH=2的酸洗、水洗两步操作,为了防止CuCl被氧化,故不采用硝酸,而应采用硫酸或盐酸
D.步骤⑥中醇洗主要目的是去除CuCl表面水分,但在步骤⑦中仍需要烘干,故节约成本可删除醇洗操作
-
某实验小组采用刻蚀废液(主要含CuCl2、FeCl3、FeCl2、HCl)制取Cu和Cu2Cl2,实验流程如下:

已知:Cu2Cl2是白色固体,微溶于水,难溶于乙醇,受潮后在空气中易被迅速氧化。
(1)“预处理"时,需用Na2CO3调节溶被至微酸性而不是碱性,其原因是_____
(2)“还原Ⅰ”需在80℃条件下进行,适宜的加热方式为_______
(3)“还原Ⅱ”中,Cu2+参与反应的离子方程式为______
(4)“搅拌”时加入NaCl粉末的作用是________
(5)“过滤Ⅱ”得到的Cu2Cl2需用无水乙醇洗涤,并在真空干燥机内于70℃干燥2小时,冷却,密封包装。于70℃真空干燥的目的是_________
(6)①请设计从“过滤Ⅰ”所得滤渣中获取Cu的实验方案:_______(实验中可供选择的试剂:稀硫酸、稀硝酸、蒸馏水)。
②现欲测定途径a、b回收铜元素的回收率比,请补充实验方案:_______________,分别按途径a、b制取Cu和Cu2Cl2,测得Cu的质量为m1g,Cu2Cl2的质量为m2g,则途径a、b铜素的回收率比为________(铜元素回收率=产品中铜元素质量/废液中铜元素的质量×100%)
-
CuCl常用于有机合成催化剂,并用于颜料、防腐等。工业上以黄铜矿 主要成分是
主要成分是 ,含有少量
,含有少量 为主要原料制备CuCl的主要流程如下:
为主要原料制备CuCl的主要流程如下:
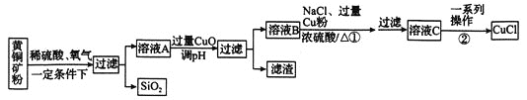
已知:CuCl难溶于水和乙醇,在空气中易被氧化,在水溶液中存在平衡: 白色
白色 无色溶液
无色溶液 。
。
回答下列问题:
 滤渣的主要成分是________
滤渣的主要成分是________ 填化学式
填化学式 。
。
 溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
溶液A中含有硫酸铜、硫酸铁,则在一定条件下黄铜矿与稀硫酸、氧气发生反应的化学方程式为_____。
 ①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
①中发生反应的离子方程式为_________,当观察到__________现象,即表明反应已经完全。
 ②中的一系列操作是________。
②中的一系列操作是________。
 已知:常温下
已知:常温下 ,
, 。若溶液A中
。若溶液A中 ,加入氧化铜
,加入氧化铜 忽略溶液体积变化
忽略溶液体积变化 ,使溶液中
,使溶液中 恰好沉淀完全,此时是否有
恰好沉淀完全,此时是否有 沉淀生成_______
沉淀生成_______ 列式计算
列式计算 。
。 已知:溶液中离子浓度
已知:溶液中离子浓度 时可认为沉淀完全
时可认为沉淀完全 。
。
 工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
工业上还可以利用铜电极电解饱和食盐水制备CuCl,阳极的电极反应式为________。
-
氯化亚铜是用途广泛的铜盐产品。CuCl晶体呈白色,微溶于水,不溶于乙醇和稀盐酸,溶于浓盐酸,见光易分解。某研究小组以CuCl2(含少量Fe2+)粗品为原料制取CuCl晶体,设计如下制备流程:
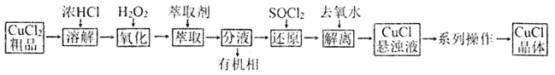
实验涉及的操作及装置如下:
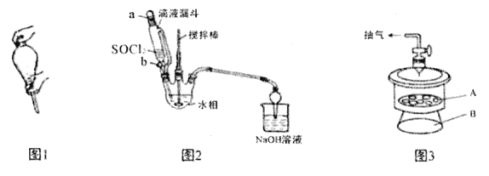
已知
①在较浓的盐酸溶液中:
a.Cu2+主要以[CuCl4]2-(呈黄色)形式存在
b.Fe3+能溶解于萃取剂一甲基异丁基甲酮(无色透明液体,密度为0.8g/cm3)
②CuCl在溶液中存在络合与解离平衡:CuCl(s)+3Cl-(aq) [CuCl4]3-(aq无色)
[CuCl4]3-(aq无色)
③SOCl2熔点-105℃、沸点76℃、遇水剧烈水解生成SO2和HCl气体
请回答:
(1)下列有关CuCl2提纯操作正确的是______
A.将氧化液转移至分液漏斗中,加入萃取剂后,塞上玻璃塞,用力振摇(见上图1)
B.经几次振摇并打开上口玻璃塞放气后,将分液漏斗置于铁架台的铁圈上,静置片刻
C.Fe2+经氧化、萃取、分液,进入有机相除去
D.取分液后的水相少许,滴入KSCN溶液检验萃取是否完全
(2)还原反应装置如上图2所示:
①向三颈烧瓶中缓慢滴加SOCl2时,需打开活塞_____(填“a”、“b”或“a和b”)。
②水相中[CuCl4]2-被SOCl2还原为[CuCl4]3-的离子方程式为______。
③判断反应完成的实验现象是________________。
(3)向混合液中加入大量去氧水能得到CuC1悬浊液的原因是___________
(4)“系列操作”包括:抽滤→洗涤→干燥。下列说法不正确的是__________
A.抽滤操作用到的器材包括滤纸、布氏漏斗、吸滤瓶、安全瓶和抽气泵等
B.可选用无水乙醇洗涤CuCl,洗涤时应关闭水龙头,使洗涤剂缓慢通过沉淀物
C.取最后一次洗涤液,滴加BaCl2溶液,若无白色沉淀产生,则证明产品已洗净
D.在避光下产品应置于A处真空干燥(上图3)
-
铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO) 为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:
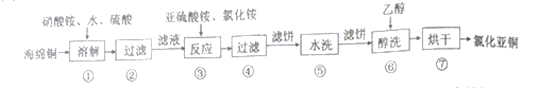
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。回答下列问题:
(1)步骤①中N 元素被还原为最低价,则Cu溶解的离子方程式为_______________。
(2)步骤③中(NH4)SO3要适当过量,目的是使Cu2+充分还原,并保证Cu2+的还原速率和_____,其主要反应的离子方程式________________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl]/n(Cu2+)] 与Cu2+沉淀率的关系如下图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是_____________________。
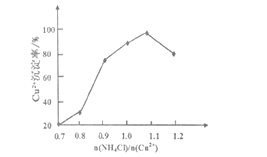
(3)步骤⑥中醇洗的目的是____________________________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利太阳能热化学循环法分解H2O制H2,其物质转化如图所示。
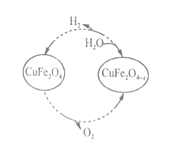
(4)氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_______________。
(5)若x=0.15,则1mol CuFe2O4-x参与一次该循环,理论上能制得的H2体积为_______L(标准状况下)。
-
铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:
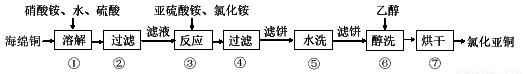
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。
回答下列问题:
(1)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为________。
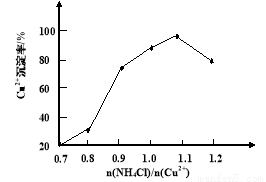
(2)步骤③中 (NH4)2SO3要适当过量,目的是使Cu2+充分还原速率和________,其主要反应的离子方程式为_________。已知NH4Cl、Cu2+的物质的量之比[n( NH4Cl )/n(Cu2+)]与Cu2+沉淀率的关系如右图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利用太阳能热化学循环法分解H2O制H2,其物质转化如图甲所示。
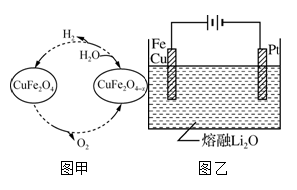
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为________。
②若x=0.15,则1 mol CuFe2O4参与该循环过程理论上一次能制得标准状况下的H2体积为________L。(标准状况下)
③CuFe2O4可用电化学方法得到,其原理如图乙所示,则阳极的电极反应式为__________。
-
【化学-选修2:化学与技术】
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料采用硝酸铵氧化分解技术生产CuC1的工艺过程如下:
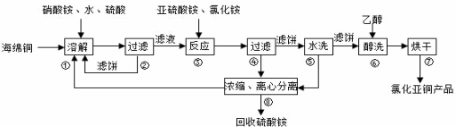
回答下列问题:
(1)步骤①中得到的氧化产物是___________,溶解温度应控制在60-70℃,原因是___________;
(2)写出步骤③中主要反应的离子方程式_________________;
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是_________________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有_______(填字母)
A、分馏塔 B、离心机 C、反应釜 D、框式压滤机
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为___________。

]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,其原因是___。

















