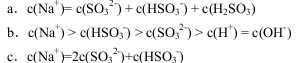-
新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的 ,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用
,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用 外,还能得到一种复合肥料。
外,还能得到一种复合肥料。
(1)①若氨水与 恰好完全反应生成正盐,则此时溶液呈________性
恰好完全反应生成正盐,则此时溶液呈________性 填“酸”或“碱”
填“酸”或“碱” 。常温下弱电解质的电离平衡常数如下:氨水
。常温下弱电解质的电离平衡常数如下:氨水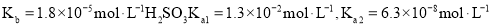
 溶液中通入________气体可使溶液呈中性。
溶液中通入________气体可使溶液呈中性。 填“
填“ ”或
”或 ”
” 此时溶液中
此时溶液中 ________
________ 填“
填“ ”“
”“ ”或“
”或“ ”
”
(2)向 溶液通入过量
溶液通入过量 ,充分反应后所得溶液中离子浓度大小顺序为________________。
,充分反应后所得溶液中离子浓度大小顺序为________________。
-
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义。
(1)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为______________________(写出一种即可)。
(2)25℃ 101KPa,将1molCH4与一定量的O2混合后,充入一密闭绝热容器内,在连续电火花的作用下反应,恢复至原状况放出QkJ热量,容器内无无CH4和O2剩余且无固体物质生成,装置内气体全部通入足量的碱石灰后,剩余bmol气体。则:
①反应开始时CH4与O2的物质的量之比为___________________________。
②若已知 C(s) + O2(g) = CO2(g) △H1= -m kJ/mol
CO2(g) + C(s) = 2CO(g) △H2= +n kJ/mol
则表示CH4燃烧热的热化学方程式为_____________________________________________。
(3)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应,
NO+NO2+Na2CO3===2NaNO2+CO2,2NO2+Na2CO3===NaNO2+NaNO3+CO2
① 用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则混合气体中NO和NO2的体积比为____________。
② 用Na2CO3溶液吸收法处理氮的氧化物存在的缺点是___________________。
(4)氮的固定是几百年来科学家一直研究的课题
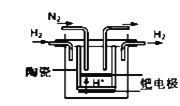
①20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现高温常压下的电化学合成氨,提高了反应物的转化率,其实验简图如图所示,正极的电极反应式是___________________________________。
②近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(l)≒4NH3(g)+3O2(g),则其反应热△H=________________。
(已知:N2(g)+3H2(g)≒2NH3(g)△H=﹣92.4kJ.mol﹣1,2H2(g)+O2(g)≒2H2O(l) △H=﹣571.6kJ.mol﹣1 )
-
研究烟气的脱硫(除SO2)和脱硝(除NOx)具有重要意义,请回答下列问题.
(1)烟气脱硫、脱硝的环境意义是______;
(2)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中SO2,再用一定量的磷酸与上述吸收产物反应,得到一种复合肥(含有两种或以上营养元素),该复合肥料可能的化学式______(只写一种);
(3)火力发电厂的燃煤排烟中含大量的氮氧化物(NOx),可利用甲烷和NOx在一定条件下反应消除其污染,写出CH4与NO2反应的化学方程式______;
(4)脱硝反应2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H<0,在低温恒容的密闭容器中进行并达平衡,下列说法正确的是______;(填序号)
A.降低温度平衡常数变大
B.充入NH3,NO和NO2转化率变大,平衡常数变大
C.使用催化剂,达平衡的时问缩短,△H变小
D.充入惰性气体,压强变大,平衡向左移动
(5)使用催化技术利用反应2NO(g)+2CO(g)=N2(g)+2CO2(g),根据传感器在某温度下测得的数据绘制如图.
①前1S内的平均反应速率v(CO2)=______.②该温度下的平衡常数K=______;
(6)目前科学家正研究以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理及脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图:为达脱硝最佳效果,你认为应选用的条件是______.

-
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一。
(1) 新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,其吸收的化学反应方程式为________再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(只要求写一种)。
(2) 工业上生产硫酸时,将SO2氧化为SO3是关键一步。
① 某温度下,SO2(g)+1/2O2(g) SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时混合气体的总物质的量为8.0mol,该温度下平衡常数K=________。
SO3(g);△H= —98 kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时混合气体的总物质的量为8.0mol,该温度下平衡常数K=________。
② 一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g)达到平衡后改变下述条件,SO3的体积分数变大的是________
2SO3(g)达到平衡后改变下述条件,SO3的体积分数变大的是________
A、保持温度和容器压强不变,充入2mol SO3
B、保持温度和容器体积不变,充入2mol N2
C、保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2
D、升高温度
E、移动活塞压缩气体
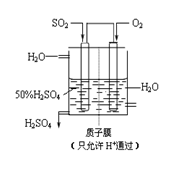
(3) 某人设想以如图所示装置用电化学原理生产硫酸,通入O2的一极的电极为________极; 写出通入SO2的电极的电极反应式:________。
-
下表列出了3种燃煤烟气脱硫方法的原理。
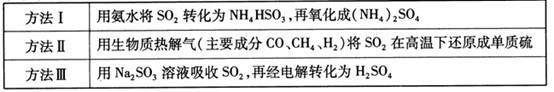
(1) 方法Ⅰ中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为:



能提高燃煤烟气中 去除率的措施有 ▲ (填字母)。
去除率的措施有 ▲ (填字母)。
A.增大氨水浓度
B.升高反应温度
C.使燃煤烟气与氨水充分接触
D. 通入空气使 转化为
转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的 ,原因是▲(用离子方程式表示)。
,原因是▲(用离子方程式表示)。
(2) 方法Ⅱ重要发生了下列反应:








 与
与 反应生成
反应生成 的热化学方程式为________。
的热化学方程式为________。
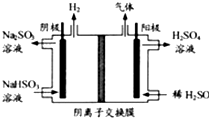
(3) 方法Ⅲ中用惰性电极电解 溶液的装置
溶液的装置
如右图所示。阳极区放出气体的成分为________。
(填化学式)
-
烟气的脱硝(除 )技术和脱硫(除
)技术和脱硫(除 )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
(1)工业上可以采用“质子膜电解槽”对烟气进行脱硫脱硝,其工艺如图甲所示:
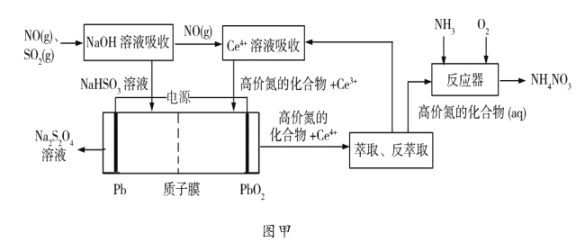
① 溶液吸收
溶液吸收 主要反应的化学方程式为___________;
主要反应的化学方程式为___________;
②电解的主要目的是______________,阴极的电极反应式为______________;
③“高价氮的化合物”中NO2在反应器中发生化合反应的化学方程式为______;
(2)利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的 与活性焦炭反应生成
与活性焦炭反应生成 和
和 ,当生成
,当生成 时,转移电子的物质的量为__________
时,转移电子的物质的量为__________ ;
;
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入 的
的 乳浊液中,发生的反应如下:
乳浊液中,发生的反应如下: ,
, ,改变
,改变 ,
, 的去除率变化情况如图乙所示。
的去除率变化情况如图乙所示。
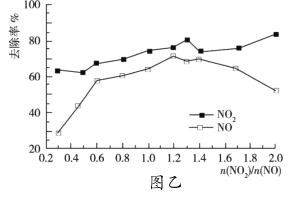
①当 大于1.4时,
大于1.4时, 去除率升高,但
去除率升高,但 的去除率却降低。其可能的原因是__;
的去除率却降低。其可能的原因是__;
② 和
和 发生的主要反应为
发生的主要反应为 。保持
。保持 的初始浓度不变,改变
的初始浓度不变,改变 ,将反应后的混合气体通入
,将反应后的混合气体通入 乳浊液中吸收。为节省
乳浊液中吸收。为节省 的用量,又能保持
的用量,又能保持 去除效果,则
去除效果,则 合适的值约为___________;
合适的值约为___________;
(4)已知: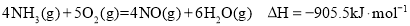 ,
, ,则
,则 ______________________。
______________________。
-
下表列出了3种燃煤烟气脱硫方法的原理.

(1)方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3(NH4)2SO3+SO2+H2O=2NH4HSO3能提高燃煤烟气中SO2去除率的措施有______(填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是______(用离子方程式表示).
(2)方法Ⅱ重要发生了下列反应:
2CO(g)+SO2(g)=S(g)+2CO2(g)△H=8.0kJ•mol-1
2H2(g)+SO2(g)=S(g)+2H2O(g)△H=90.4kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ•mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式为______.
(3)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如右图所示.阳极区放出气体的成分为______.(填化学式)
-
烟气中 和
和 的转化和综合利用既有利于节约资源,又有利于保护环境。
的转化和综合利用既有利于节约资源,又有利于保护环境。

 采用“联合脱硫脱氮技术”处理烟气
采用“联合脱硫脱氮技术”处理烟气 含
含 、
、 、
、 可获得含
可获得含 、
、 、
、 的副产品,工业流程如图1所示。
的副产品,工业流程如图1所示。
 反应釜 Ⅰ中
反应釜 Ⅰ中 与足量石灰乳反应的化学方程式为________。
与足量石灰乳反应的化学方程式为________。
 下列措施能提高各反应釜中气体去除率的有 ________
下列措施能提高各反应釜中气体去除率的有 ________ 填字母
填字母 。
。
A. 加快通入气体的速率
B. 采用气、液逆流的方式吸收气体
C. 吸收过程中定期补充吸收液
 反应釜 Ⅱ中
反应釜 Ⅱ中 转化为
转化为 反应的化学方程式为________。
反应的化学方程式为________。
 预处理器中发生的主要反应为
预处理器中发生的主要反应为 ,
, 。室温下,固定进入预处理器的NO的物质的量,改变加入
。室温下,固定进入预处理器的NO的物质的量,改变加入 的物质的量,反应一段时间后体系中
的物质的量,反应一段时间后体系中 、
、 随反应前
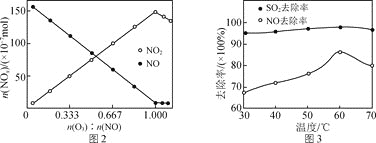
随反应前 的变化如图2所示。当
的变化如图2所示。当 时,反应后
时,反应后 的物质的量减少,其原因是__________________________________。
的物质的量减少,其原因是__________________________________。
 研究表明:
研究表明: 酸性复合吸收剂可同时有效脱硫、脱硝。图3所示为复合吸收剂组成一定时,温度对脱硫、脱硝的影响。
酸性复合吸收剂可同时有效脱硫、脱硝。图3所示为复合吸收剂组成一定时,温度对脱硫、脱硝的影响。
 温度高于
温度高于 后,NO去除率下降的原因为________。
后,NO去除率下降的原因为________。
 写出废气中的
写出废气中的 与
与 反应的离子方程式:________。
反应的离子方程式:________。
-
化学与生活密切相关。下列说法错误的是
A. 泡沫灭火器利用硫酸铝和小苏打溶液反应的产物来灭火
B. 为使水果尽快成熟,可用浸泡过高锰酸钾溶液的硅土吸收水果产生的乙烯
C. 煤的干馏、燃煤烟气的脱硫、煤的液化和气化等过程都是化学变化
D. 面粉生产中禁止添加的过氧化钙(CaO2)阴、阳离子的个数之比为1:1
-
煤炭是我国的主要能源之一,与之伴生的二氧化硫(SO2)和酸雨污染问题较为突出。目前我国采用的控制方法是电厂烟气脱硫。烟气脱硫的原理是利用碱性物质吸收并固定酸性的二氧化硫,主要有如下两种方法:
I、钠碱循环法脱硫技术。
(1)此法是利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得,该反应的离子方程式: 。
(2)NaOH溶液吸收SO的过程中,pH随 变化关系如下表:
变化关系如下表:

①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当溶液呈中性时,离子浓度关系正确的是(选填字母): 。
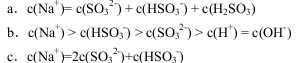
II、石灰石脱硫法
此法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4 (s)+ CO (g) CaO(s)+ SO2 (g)+ CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ)
CaO(s)+ SO2 (g)+ CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) △H2= -175.6kJ·mol-1 (反应Ⅱ)
CaS(s)+ 4CO2(g) △H2= -175.6kJ·mol-1 (反应Ⅱ)
请回答下列问题:
(1)结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s)的热化学反应方程式 。
(2)对于气体参与的反应,表示平衡常数 Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅰ的Kp= (用表达式表示)。
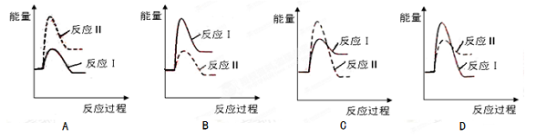
(3)假设某温度下,反应Ⅰ的速率(v1)小于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
(4)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数 的关系曲线。则降低该反应体系中产生的SO2生成量的措施有 。
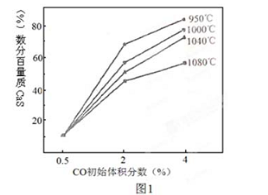
A、向该反应体系中投入生石灰
B、在合适的温度区间内控制较低的反应温度
C、降低CO的初始体积百分数
D、提高反应体系的温度
,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用
外,还能得到一种复合肥料。
恰好完全反应生成正盐,则此时溶液呈________性
填“酸”或“碱”
。常温下弱电解质的电离平衡常数如下:氨水
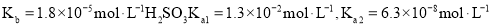
溶液中通入________气体可使溶液呈中性。
填“
”或
”
此时溶液中
________
填“
”“
”或“
”
溶液通入过量
,充分反应后所得溶液中离子浓度大小顺序为________________。







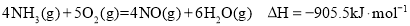 ,
,