-
硫酸亚铁铵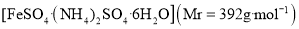 又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
Ⅰ 摩尔盐的制取:
摩尔盐的制取:
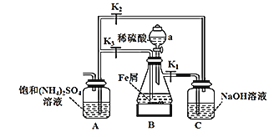
(1)仪器a的名称为:_________________
(2)检查装置气密性,加入药品,先关闭 ,打开
,打开 、
、 和仪器a活塞,装置B中有气体产生,该气体的作用是______________。反应一段时间后,欲使摩尔盐在装置A中生成的对应操作为___________。
和仪器a活塞,装置B中有气体产生,该气体的作用是______________。反应一段时间后,欲使摩尔盐在装置A中生成的对应操作为___________。
Ⅱ 摩尔盐纯度测定:取
摩尔盐纯度测定:取 硫酸亚铁铵样品配制成
硫酸亚铁铵样品配制成 溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
 甲
甲 方案一:取
方案一:取 硫酸亚铁铵溶液用
硫酸亚铁铵溶液用 的酸性
的酸性 溶液进行三次滴定。
溶液进行三次滴定。
 乙
乙 方案二:
方案二:


 丙
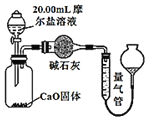
丙 方案三:实验设计图如图所示:
方案三:实验设计图如图所示:
(3)写出方案一发生反应的离子方程式____________,若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因: _________;设计实验验证你的推测:_____________。
(4)方案三测得 的体积为
的体积为 已折算为标准状况下
已折算为标准状况下 ,计算摩尔盐的纯度________。
,计算摩尔盐的纯度________。 计算结果保留一位小数
计算结果保留一位小数
-
(15分)硫酸亚铁铵又称莫尔盐,是浅绿色晶体。它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂。某实验小组利用工业废铁屑制取莫尔盐,并测定其纯度。
已知:①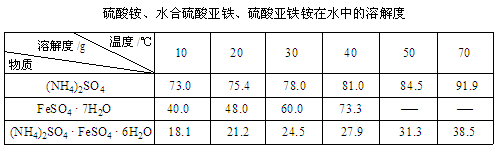
②莫尔盐在乙醇溶剂中难溶。
Ⅰ.莫尔盐的制取

试分析:
(1)步骤2中加热方式 (填“直接加热”﹑“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是 。
(2)步骤3中包含的实验操作名称 。
(3)产品莫尔盐最后用 洗涤(填字母编号)。
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500 mL溶液,根据物质组成,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000 mol·L-1的酸性KMnO4溶液分三次进行滴定。
(乙)方案二:取20.00 mL硫酸亚铁铵溶液进行如下实验。

(1)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为
,验证推测的方法为: 。
(丙)方案三:(通过NH4+测定)实验设计图如下所示。取20.00 mL硫酸亚铁铵溶液进行该实验。

(2)①装置 (填“甲”或“乙”)较为合理,判断理由是 。量气管中最佳试剂是 (填字母编号。如选“乙”则填此空,如选“甲”此空可不填)。
a.水 b.饱和NaHCO3溶液 c.CCl4
②若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为 。
-
硫酸亚铁铵又称莫尔盐,是浅绿色晶体.它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂.某实验小组利用工业废铁屑制取莫尔盐,并测定其纯度.
已知:①
| 
| 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.3 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | ﹣ | ﹣ |
| (NH4)2SO4•FeSO4•6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
②莫尔盐在乙醇溶剂中难溶.
Ⅰ.莫尔盐的制取

试分析:
(1)必须在铁屑少量剩余时进行过滤,其原因是______________________.
(2)步骤3中包含的实验操作名称_____________________.
(3)产品莫尔盐最后用______________________ 洗涤(填字母编号).
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500mL溶液。根据物质组成甲、乙、丙三位同学设计了如下三个实验方案,请回答:
方案一:取20.00mL硫酸亚铁铵溶液用0.1000molL﹣1的酸性KMnO4溶液分三次进行滴定.
方案二:取20.00mL硫酸亚铁铵溶液进行如下实验.

(4)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为_________,验证推测的方法为:___________________________________________方案三:(通过NH4+测定)实验设计图如下所示.取20.00mL硫酸亚铁铵溶液进行该实验.
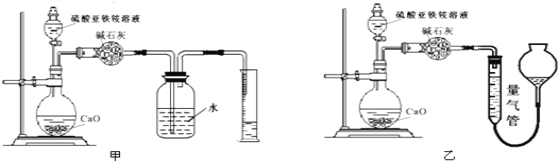
(5)装置___________ (填“甲”或“乙”)较为合理,判断理由是_______________.
(6)量气管中最佳试剂是__________ (填字母编号.如选“乙”则填此空,如选“甲”此空可不填).
a.水 b.饱和NaHCO3溶液 c.CCl4
(7)若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为_______.
-
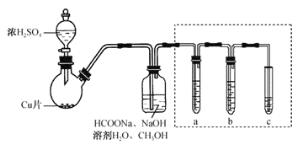
某实验小组利用甲酸钠(HCOONa)制备Na2S2O4并测定产品的纯度,实验装置(夹持、加热仪器略)如图
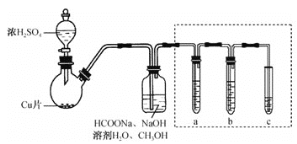
回答下列问题
(1)盛放浓硫酸的仪器名称为________,写出浓H2SO4与Cu反应的化学方程式 ________ 。
(2)SO2与HCOONa、NaOH反应生成Na2S2O4和CO2, 其离子方程式为________。
(3)图中虚线框中装置用于检验逸出气体中的CO2 , a、b、c所盛放的试剂依次为________、________、________。
(4)将反应液分离提纯得到Na2S2O4产品,取产品mg溶于水,并定容为100mL,取25.00mL加入锥形瓶中,加入NaOH溶液及指示剂,用cmol·mol-1的K3[Fe(CN)6]标准溶液进行滴定{4K3[Fe(CN)6]+2Na2S2O4+8NaOH=3K4[Fe(CN)6]+4Na2SO3+Na4[Fe(CN)6]+4H2O},滴定至终点时,消耗标准液VmL。则产品的纯度为________(写出计算式)。
-
某校课外小组的同学设计实验用甲烷还原二氧化硫制取单质硫。
(1)甲组同学分别利用如图所示装置制取SO2 和CH4。

①仪器M的名称为______________。
②用A装置制备SO2,不宜使用稀硫酸,其原因是_________________。
③用B装置制取甲烷的化学方程式为CH3COONa+NaOH CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是____________________________________。
CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是____________________________________。
(2)乙组同学利用甲组制得的CH4和SO2进行实验,并验证产物中除单质硫外还含有CO2。为进行验证,选用甲组实验中的装置A、B和下图所示的装置进行实验,发现G中有淡黄色固体生成,C中澄清石灰水变浑浊。

①乙组同学的实验装置中,依次连接的合理顺序为A、B→H→_____→ → → → 。
②E装置的作用是________________,G装置的作用是_______________。
③F装置中发生反应的化学方程式为____________________。
-
某校课外小组的同学设计实验用甲烷还原二氧化硫制取单质硫。
(1)甲组同学分别利用如图所示装置制取SO2 和CH4。
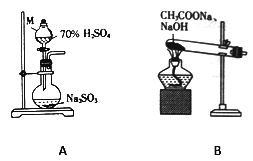
①仪器M的名称为______________。
②用A装置制备SO2,不宜使用稀硫酸,其原因是_________________。
③用B装置制取甲烷的化学方程式为CH3COONa+NaOH CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是____________________________________。
CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是____________________________________。
(2)乙组同学利用甲组制得的CH4和SO2进行实验,并验证产物中除单质硫外还含有CO2。为进行验证,选用甲组实验中的装置A、B和下图所示的装置进行实验,发现G中有淡黄色固体生成,C中澄清石灰水变浑浊。

①乙组同学的实验装置中,依次连接的合理顺序为A、B→H→_____→ → → → 。
②E装置的作用是________________,G装置的作用是_______________。
③F装置中发生反应的化学方程式为____________________。
-
某实验小组欲制取氯酸钾,并测定其纯度。制取装置如图甲所示。请回答:

(1)Ⅱ中玻璃管a的作用为__________。
(2)为了提高KOH的利用率,可将上述实验装置进行适当改进,其方法是__________。
(3)反应完毕经冷却后,Ⅱ的大试管中有大量KClO3晶体析出.图乙中符合该晶体溶解度曲线的是__________(填编号字母);要从Ⅱ的大试管中分离已析出晶体,下列仪器中不需要的是__________(填仪器编号字母)。
A.铁架台 B.长颈漏斗 C.烧杯 D.蒸发皿 E.玻璃棒 F.酒精灯
(4)上述制得的晶体中含少量KClO、KCl杂质.
已知:碱性条件下,ClO-有强氧化性,ClO3-很稳定;酸性条件下,ClO-、ClO3-都具有较强的氧化性.
为测定KClO3的纯度,进行如下实验:
步骤1:去上述晶体3.00g,溶于水配成100mL溶液.
步骤2:取20.00mL溶液于锥形瓶中,调至pH=10,滴加双氧水至不再产生气泡,煮沸.
步骤3:冷却后,加入足量KI溶液,再逐渐滴加入足量稀硫酸.
发生反应:ClO3-+I-+H+→Cl++I2+H2O(未配平)
步骤4:加入指示剂,用0.5000mol•L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液48.00mL,发生反应:2S2O32-+I2═S4O62-+2I-.
①步骤2中用双氧水除去溶液中残留ClO-的离子方程式为__________。
②该晶体中KClO3的质量分数为__________。
③若步骤2中未进行煮沸,则所测KClO3的质量分数__________(填“偏低”、“偏高”或“无影响”)
-
(15分)硫酸亚铁铵又称莫尔盐,是浅绿色晶体。它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂。某实验小组利用工业废铁屑制取莫尔盐,并测定其组成,他们进行了以下实验。
Ⅰ.莫尔盐的制取

(把图中“一定实验步骤”换成“加热蒸发、浓缩结晶”)
请回答下列问题。
(1)废铁屑中含氧化铁,无需在制备前除去,理由是__________________(用离子方程式回答),实验前都需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。从以下仪器中选择组装,完成该操作必需的仪器有________(填编号)。
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥漏斗 ⑦酒精灯
(2)步骤2中加热方式 (填“直接加热”﹑“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是 。
II.莫尔盐组成的测定
①将摩尔盐低温烘干后,称取7.84 g加热至100℃失去结晶水,质量变为5.68 g。
②选择下图所示的部分装置连接起来,检查气密性后,将上述5.68g固体放入A装置的锥形瓶中,再向锥形瓶中加入足量NaOH浓溶液,充分吸收产生的气体并测出气体质量为0.68 g。
③向A中加入适量3%的H 2 O 2 溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6 g。

根据上述实验回答下列问题。
(3)步骤②中,选择的装置是A接_______接_______(填代号),A装置中未使用分液漏斗的理由是______________。
(4)向锥形瓶中加入NaOH溶液的操作方法是_______;吸收A中产生的气体所用试剂应是_______。实验小组的同学为保证A中产生的气体被完全吸收以准确测量其质量,他们在A中反应停止后再进行的操作是______________。
(5)根据上述实验数据计算,摩尔盐中 =_______。
=_______。
-
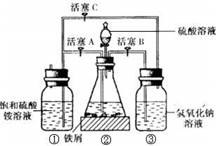
摩尔盐[(NH4)2SO4•FeSO4•6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
(1)用30%的NaOH溶液和废铁屑(含少量油污、铁锈、FeS等)混合、煮沸、冷却、分离,将分离出的NaOH溶液装入③中.
(2)利用容器②的反应,向容器①中通入氢气,应关闭活塞______,打开活塞______(填字母).向容器①中通入氢气的目的是______.
(3)待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部.在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
(4)为了确定产品中亚铁离子的含量,研究小组用滴定法来测定.若取产品24.50g配成100mL溶液,取出10.00mL用0.1000mol•L-1KMnO4酸性溶液滴定,消耗KMnO4溶液10.00mL.
①试配平反应的离子方程式:
______MnO4-+______Fe2++______H+=______Mn2++______Fe3++______H2O
②滴定时,将KMnO4溶液装在______(酸式或碱式)滴定管中,判断反应到达滴定终点的现象为______.
③产品中摩尔盐的质量分数______.
-
某实验小组利用甲酸钠(HCOONa)制备Na2S2O4并测定产品的纯度,实验装置(夹持、加热仪器略)如图
将反应液分离提纯得到Na2S2O4产品,取产品mg溶于水,并定容为100mL,取25.00mL加入锥形瓶中,加入NaOH溶液及指示剂,用cmol·mol-1的K3[Fe(CN)6]标准溶液进行滴定{4K3[Fe(CN)6]+2Na2S2O4+8NaOH=3K4[Fe(CN)6]+4Na2SO3+Na4[Fe(CN)6]+4H2O},滴定至终点时,消耗标准液VmL。则产品的纯度为________(写出计算式)。
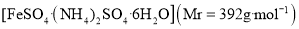 又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
摩尔盐的制取:
,打开
、
和仪器a活塞,装置B中有气体产生,该气体的作用是______________。反应一段时间后,欲使摩尔盐在装置A中生成的对应操作为___________。
摩尔盐纯度测定:取
硫酸亚铁铵样品配制成
溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
甲
方案一:取
硫酸亚铁铵溶液用
的酸性
溶液进行三次滴定。
乙
方案二:


丙
方案三:实验设计图如图所示:

的体积为
已折算为标准状况下
,计算摩尔盐的纯度________。
计算结果保留一位小数














 =_______。
=_______。
