-
某同学用图示装置进行铁与稀硝酸反应的实验并进行相关的实验探究。(共计13分)
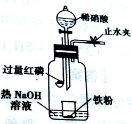
实验步骤:
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的
纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好橡胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向小
烧杯中滴入一定量的4mol/L的稀硝酸,铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性?
(2)燃烧红磷的目的是
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究
(1)提出合理假设
假设1:产物中只有+2价铁元素;假设2: ;
假设3:产物中既有+2价铁元素,又有+3价铁元素.
(2)设计实验方案,证明假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+)︰n(Fe3+)=3︰1时,则相应反应的离子方程式为 。
-
(16分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。(相对原子质量Fe:56)
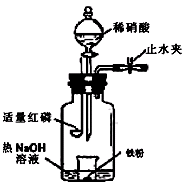
a.向广口瓶内注入足量热NaOH溶液,将盛有a g纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入200mL 6mol/L的稀硝酸,铁粉恰好完全溶解。
(一)气体产物成分探究
①实验前如何检查该装置的气密性________。
②燃烧红磷的目的是________。
③为证明气体产物为NO,步骤c后还缺少的一步主要操作是___________________。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物只有+3价铁;
假设2:________;
假设3:________。
(2)设计实验:分别取小烧杯中反应后溶液装入两支试管甲、乙,在甲试管中滴加酸性高锰酸钾溶液;在乙试管中滴加KSCN溶液,观察现象。推测实验现象与结论:
①若现象为:________,则假设1正确;
②若现象为:________,则假设2正确;
③若现象为:________,则假设3正确。
(3)a值范围为________。
-
(14分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
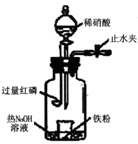
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸人瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中缓慢滴入一定量的4mol·L-1的稀硝酸,
铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性? 。
(2)燃烧红磷的目的是 。
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;假设2: ,假设3:产物中既有+2价铁,又有+3价铁。
(2)设计实验方案,验证假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1时,则对应的离子反应方程式为 。
-
某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
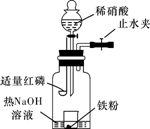
a.向广口瓶内注入足量热NaOH溶液,将盛有a g纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入300mL 6mol/L的稀硝酸,铁粉恰好完全溶解。
(一)气体产物成分探究:
(1)燃烧红磷的目的是 。
(2)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物只有+3价铁;
假设2: ;
假设3: 。
(2)设计实验:分别取小烧杯中反应后溶液装入两支试管甲、乙,在甲试管中滴加酸性高锰酸钾溶液;在乙试管中滴加KSCN溶液,观察现象。推测实验现象与结论:
①若现象为: ,则假设1正确;
②若现象为: ,则假设2正确;
③若现象为: ,则假设3正确。
(3)a值范围为 。
-
某同学用下列实验装置探究硝酸的性质。根据图示判断下列结论不正确的是
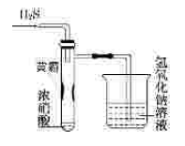
A.试管内壁上“黄霜”的成分是硫
B.该实验探究说明浓硝酸既有氧化性,又有挥发性
C.烧杯内的NaOH溶液的作用是除去尾气,防止尾气污染环境
D.H2S用SO2代替,将无明显反应现象
-
某同学看到“利用零价铁还原 脱除地下水中硝酸盐”的相关资料后,利用如下装
脱除地下水中硝酸盐”的相关资料后,利用如下装
置探究铁粉与 溶液的反应。实验过程如下:
溶液的反应。实验过程如下:
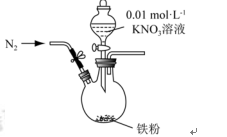
i.打开弹簧夹,缓慢通入 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行;
氛围中进行;
ii.加入pH 已调至2.5 的 0.01mol· 酸性溶液100mL,一段时间后铁粉部分溶解,
酸性溶液100mL,一段时间后铁粉部分溶解,
溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物
质附着;
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在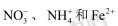 。
。
(1)通入 并保持后续反应均在2 N 氛围中进行的实验目的是_________。
并保持后续反应均在2 N 氛围中进行的实验目的是_________。
(2)白色物质是_________,用化学方程式解释其变为红褐色的原因:_________。
(3)用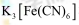 检验滤液中
检验滤液中 的实验方案是_________。
的实验方案是_________。
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液
呈红色。溶液变成红色的原因是_________。
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳。他用上述 溶液继续
溶液继续
设计如下实验,探究碳粉的作用。
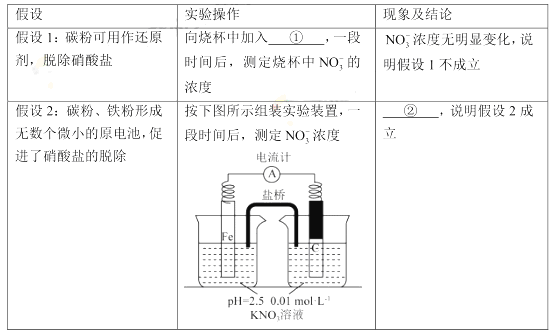
③关于碳粉的作用,还可以提出的假设是 。
-
某同学利用如图装置制NO并进行相关实验探究。
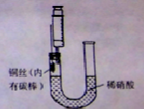
(1)写出制备NO的反应方程式
(2)收集的气体与空气混合后变红色,这说明NO具有_____性。
(3)制备NO的步骤如下:
1按图所示连接好装置;
2取下注射器,通过U型长管加入稀硝酸至接近U型短管的铜丝
3在针头上安装好注射器,抽出U型短管中的所有空气;然后拔出注射器,并排尽注射器中的空气。
4待硝酸与铜丝分离后,用已排除空气的注射器抽出生成NO,将注射器针头插入橡皮塞中以封口。
在上述操作中遗漏的一个步骤是 ,在步骤3中可以观察到的现象为 。
(4)在铜丝上绑上石墨的作用是 。
(5)若将稀硝酸换成浓硝酸,则可制取NO2气体。请你用注射器收集NO2气体并完成“外界因素对化学平衡移动影响”实验探究,相关内容填在下面表格。(只完成一个影响因素的探究,其他实验用品自选)已知
2NO2(g)  N2O4(g) △H <0;N2O4为无色气体。
N2O4(g) △H <0;N2O4为无色气体。
| 实验步骤 | 实验现象 | 实验结论 |
| ①分别用两支注射器收集NO2,并将注射器针头插入橡皮塞中以封口。 ②_____________________ _______________________ ________________________ _______________________ ________________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ |
-
某同学看到利用零价铁还原NO3-脱除地下水中硝酸盐”的相关报道后,利用如下装置探究铁粉与KNO3溶液的反应。实验过程如下:
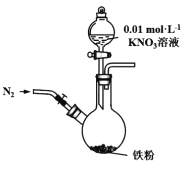
ⅰ.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进行;
ii.加入pH已调至2.5的0.01mol·L-1KNO3酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
ⅲ.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在NO3-、NH4+和Fe2+。
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________。
(2)用化学方程式解释其变为红褐色的原因:_________________________________。
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是(写出具体操作、现象及结论)___________。
(4)取少量滤液,向其中加入几滴KSCN溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是_________________________________。
(5)该同学进一步査阅文献发现,用铁粉、碳粉混合物脱除硝酸盐,效果更佳。他用上述KNO3溶液继续设计如下实验,探究碳粉的作用。
| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原剂,脱除硝酸盐 | 向烧杯中加入①_______,一段时间后,测定烧杯中NO3-的浓度 | NO3-浓度无明显变化,说明假设1不成立 |
| 假设2:碳粉、铁粉形成无数个微小的原电池,促进了硝酸盐的脱除 | 按如图所示组装实验装置,一段时间后,测定NO3-浓度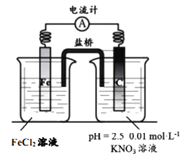 | ②___________,说明假设2成立 |
③关于碳粉的作用,还可以提出的合理假设是_________________________________。
-
某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。
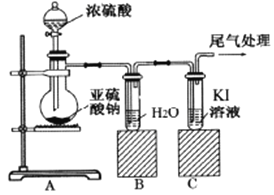
步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二 :打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C 试管中溶液的pH。
结合上述实验,回答以下问题:
(1) 甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质。该物质发生电离,其电离方程式为___________。
(2) 乙同学认为C瓶中pH可能更小,因为C中二氧化硫会像氧化硫化氢一样与碘离子发生氧化还原反应。通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是____________。测定结果如下:
| 第1次实验 | 第2次实验 | 第3 次实验 |
| B 瓶中pH | 2.15 | 2.10 | 2. 17 |
| C 瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现: C瓶中溶液的酸性始终比B瓶中的酸性强。
(3) 通过仔细观察,C瓶中溶液从无色变成浅黄色同时出现黄色浑浊,继续通入气体溶液又逐渐变为无色。其中溶液变黄且出现浑浊的过程对应的离子方程式为________,为了检验产物,中间取出少许溶液加入______,溶液变蓝,证明乙同学判断正确;黄色溶液又逐渐变为无色对应的化学反应方程式为_______________。
(4) 最终结论:
①B瓶中溶液呈弱酸性是由于__________。
②C瓶中溶液呈强酸性是由于生成了_________,该过程中体现出二氧化硫哪些化学性质_____。
-
某小组对碳与浓硝酸的反应进行探究。已知:2NaOH+2NO2=NaNO3+NaNO2+H2O,2NaOH+NO2+NO=2NaNO2+H2O。请回答下列问题:
I.甲同学设计如图所示装置制备并收集NO。
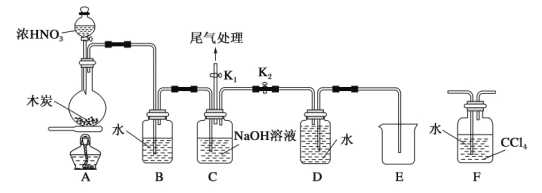
(1)碳与浓硝酸反应的化学方程式为___________。
(2)装置C的作用为__________。
(3)乙同学认为用装置F代替B更合理,理由为_______。
II.探究NO与Na2O2反应。
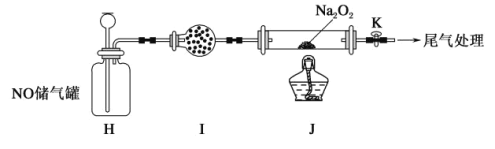
已知:NaNO2既有氧化性,又有还原性;J处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
(4)检验上图装置气密性的方法为_________。
(5)实验结束后,设计实验证明J处硬质玻璃管中有NaNO2生成__________。(可供选择的试剂:蒸馏水、KI-淀粉溶液、KMnO4溶液、NaOH溶液、BaCl2溶液、稀硫酸)






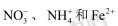 。
。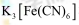 检验滤液中
检验滤液中





