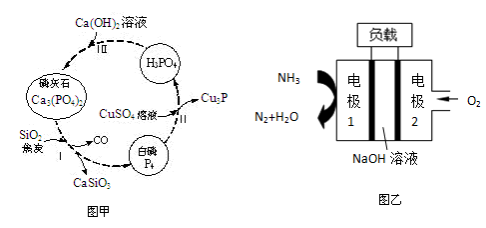-
(16分)氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为: 7.1×10-4, 2.98×10-8。将0.1mol/L的亚硝酸稀释100倍,c(H+)将 (填“不变”、“增大”、“减小”);Ka值将(填“不变”、“增大”、“减小”) 。写出HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的离子方程式 。
(2)羟胺(NH2OH) 可看成是氨分子内的l 个氢原子被羟基取代的产物,常用作还原剂,其水溶液显弱碱性。已知NH2OH 在水溶液中呈弱碱性的原理与NH3在水溶液中相似,请用电离方程式表示其原因 。
(3)亚硝酸钠与氯化钠都是白色粉末,且都有咸味,但亚硝酸盐都有毒性,通常它们可以通过加入热的白醋鉴别,亚硝酸钠遇到白醋会产生一种红棕色刺激性气味气体和一种无色刺激性气味气体,该反应的离子方程式为 。
(4)磷及部分重要化合物的相互转化如图所示。
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 。
(5)若处理后的废水中c(PO43-)=4×10-7 mol·L-1,溶液中c(Ca2+)= mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
(6)某液氨-液氧燃料电池示意图如下,该燃料电池的工作效率为50%,现用作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液中NaOH的浓度为0.3 mol·L-1,则该过程中消耗氨气的质量为 。(假设溶液电解前后体积不变)
-
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为:7.1×10-6,2.98×10-9。HNO2的酸性比HClO_______(填“强”、“弱”);将0.1mol/L的亚硝酸加水稀释100倍,c(H+)_______(填“不变”、“增大”或“减小”),Ka值________(同上)
(2)NaNO2与NaCl都是白色粉末且都有咸味,但NaNO2有毒,具有致癌性。通常它们可以通过加入热的白醋(CH3COOH)鉴别,NaNO2遇到白醋会产生一种红棕色气体和一种无色气体,它们的组成元素相同。该反应的离子方程式为____________。
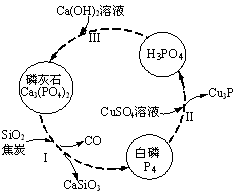
(3)磷及部分重要化合物的相互转化如图甲所示。
①“步骤Ⅰ”为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,焦炭的作用是__________。
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,“步骤Ⅱ”涉及的反应中氧化剂是_________。
(4)若处理后的废水中c(PO43-)=4×10-7mol/L,则溶液中c(Ca2+)不会超过________mol/L。(Ksp[Ca2(PO4)3]=2×10-29)
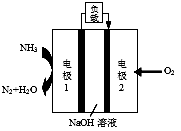
(5)某“液氨—液氧”燃料电池装置示意图如图乙所示,该燃料电池以NaOH为电解质。该电池在工作时,“电极2”为_______极(填“正”或“负”);“电极1”表面发生的电极反应式为_________。
-
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为:7.1×10-6,2.98×10-9。HNO2的酸性比HClO_______(填“强”、“弱”);将0.1mol/L的亚硝酸加水稀释100倍,c(H+)_______(填“不变”、“增大”或“减小”),Ka值________(同上)
(2)NaNO2与NaCl都是白色粉末且都有咸味,但NaNO2有毒,具有致癌性。通常它们可以通过加入热的白醋(CH3COOH)鉴别,NaNO2遇到白醋会产生一种红棕色气体和一种无色气体,它们的组成元素相同。该反应的离子方程式为____________。
(3)磷及部分重要化合物的相互转化如图甲所示。
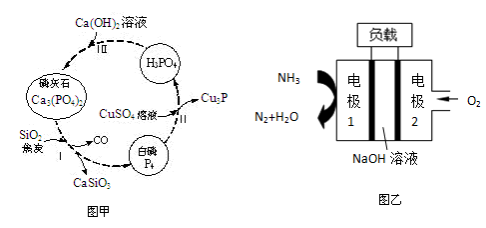
①“步骤Ⅰ”为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,焦炭的作用是__________。
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,“步骤Ⅱ”涉及的反应中氧化剂是_________。
(4)若处理后的废水中c(PO43-)=4×10-7mol/L,则溶液中c(Ca2+)不会超过________mol/L。(Kap[Ca2(PO4)3]=2×10-29)
(5)某“液氨——液氧”燃料电池装置示意图如图乙所示,该燃料电池以NaOH为电解质。该电池在工作时,“电极2”为_______极(填“正”或“负”);“电极1”表面发生的电极反应式为_________。
-
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,浓度均为0.1mol/L的亚硝酸(HNO2)、次氯酸两种溶液,它们的电离常数Ka分别为:7.1×10﹣4、2.98×10﹣8。将0.1mol/L的亚硝酸稀释,c(H+)将 (填“不变”、“增大”、“减小”);Ka值将(填“不变”、“增大”、“减小”) 。写出涉及HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的化学方程式 。
(2)羟胺(NH2OH)可看成是氨分子内的l个氢原子被羟基取代的产物,常用作还原剂,其水溶液显弱碱性。已知NH2OH在水溶液中呈弱碱性的原理与NH3在水溶液中相似,请用电离方程式表示其原因 。
(3)磷及部分重要化合物的相互转化如图1所示。
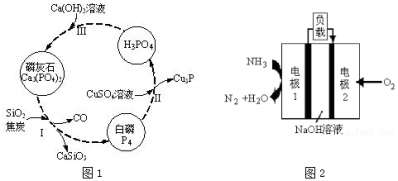
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 mol。
(4)若处理后的废水中c(PO43﹣)=4×10﹣7 mol•L﹣1,溶液中c(Ca2+)= mol•L﹣1。(已知Ksp[Ca3(PO4)2]=2×10﹣29)
(5)某液氨﹣液氧燃料电池示意图如图2,该燃料电池的工作效率为50%,现用作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液中NaOH的浓度为0.3mol•L﹣1,则该过程中需要氨气的质量为 g。(假设溶液电解前后体积不变)
-
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为: 7.1× 10-4、 2.98× 10-8。将0.1mol/L的亚硝酸稀释100倍,c(H+)将 (填“不变”、“增大”、“减小”);Ka值将 (填“不变”、“增大”、“减小”)。写出HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的离子方程式 。
(2)羟胺(NH2OH)可看成是氨分子内的l个氢原子被羟基取代的产物,常用作还原剂,其水溶液显弱碱性。已知NH2OH在水溶液中呈弱碱性的原理与NH3在水溶液中相似,请用电离方程式表示其原因 。
(3)亚硝酸钠与氯化钠都是白色粉末,且都有咸味,但亚硝酸盐都有毒性,通常它们可以通过加入热的白醋鉴别,亚硝酸钠遇到白醋会产生一种红棕色刺激性气味气体和一种无色刺激性气味气体,该反应的离子方程式为 。
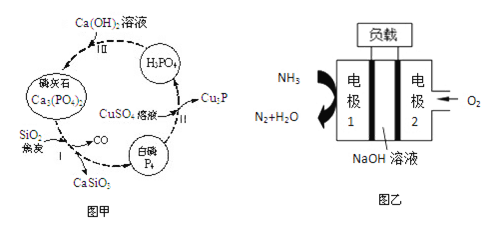
(4)磷及部分重要化合物的相互转化如下图所示。
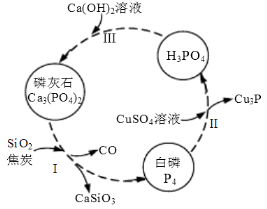
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 。
(5)若处理后的废水中c(PO43-)=4×10-7 mol·L-1,溶液中c(Ca2+)= mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
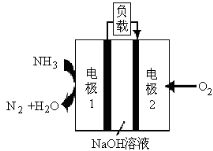
(6)某液氨-液氧燃料电池示意图如下,该燃料电池的工作效率为50%,现用作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液中NaOH的浓度为0.3 mol·L-1,则该过程中消耗氨气的质量为 (假设溶液电解前后体积不变)。
-
(14分)氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)某课外学习小组欲制备少量NO气体,写出铁粉与足量稀硝酸反应制备NO的离子方程式: 。
(2)LiFePO4是一种新型动力锂电池的电极材料。
①下图为某LiFePO4电池充、放电时正极局部放大示意图,写出该电池放电时正极反应方程式: 。
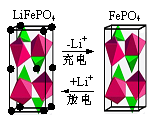
②将LiOH、FePO4·2H2O(米白色固体)与还原剂葡萄糖按一定计量数混合,在N2中高温焙烧可制得锂电池正极材料LiFePO4。焙烧过程中N2的作用是 ;实验室中以Fe3+为原料制得的FePO4·2H2O有时显红褐色,FePO4·2H2O中混有的杂质可能为 。
(3)磷及部分重要化合物的相互转化如图所示。
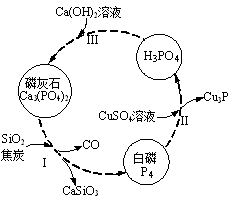
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1molCuSO4所能氧化的白磷的物质的量为 。
③步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有 。
-
(14分)氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)某课外学习小组欲制备少量NO气体,写出铁粉与足量稀硝酸反应制备NO的离子方程式: 。
(2)LiFePO4是一种新型动力锂电池的电极材料。
①下图为某LiFePO4电池充、放电时正极局部放大示意图,写出该电池放电时正极反应方程式: 。
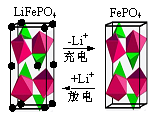
②将LiOH、FePO4·2H2O(米白色固体)与还原剂葡萄糖按一定计量数混合,在N2中高温焙烧可制得锂电池正极材料LiFePO4。焙烧过程中N2的作用是 ;实验室中以Fe3+为原料制得的FePO4·2H2O有时显红褐色,FePO4·2H2O中混有的杂质可能为 。
(3)磷及部分重要化合物的相互转化如图所示。
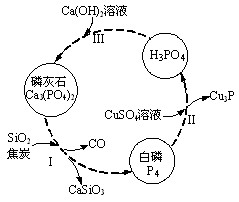
①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 。
③步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有 。
-
亚硝酸(HNO2)是一元弱酸,不稳定,只能存在于较低温度的稀溶液中。室温时,亚硝酸(HNO2)的电离平衡常数Ka=5.1×10-4,H2CO3的电离平衡常数Ka1=4.2×10-7、Ka2=5.61×10-11。亚硝酸及其盐在实验和工业生产中有重要应用。请回答:
(1)在酸性条件下,NaNO2与KI按物质的量1︰1恰好完全反应,I-被氧化为I2,写出该反应的离子方程式________________。
(2)NaNO2溶液呈_____性(填“酸”“碱”或“中”),原因是________(用离子方程式表示)。要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用______(填序号)。
a.稀H2SO4 b.CO2 c.SO2
(3)若用电解法将废水中NO2-转换为N2除去,N2将在__________(填电极名称)生成。
(4)向含1 mol Na2CO3的溶液中加入1 mol HNO2后,c(CO32-)、c(HCO3-)、c(NO2-)由大到小的顺序为________________。
(5)25℃时,用0.100mol•L-1NaOH溶液滴定20.0mL某浓度的HNO2溶液,溶液的pH与NaOH溶液体积(V)的关系如图所示,(在该条件下HNO2不分解)
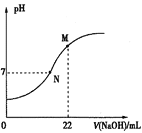
已知:M点对应溶液中,c(OH-)=c(H+)+c(HNO2)。则:
①原溶液中c(HNO2)为_________。
②下列关于N点对应溶液的说法正确的是______(填选项字母)。
A.溶质只有NaNO2
B.水电离出来的c(H+)=1×10-7 mol•L-1
C.溶液中:c(Na+)<c(OH-)
D.溶液中离子浓度:c(Na+)= c(NO2-)
-
亚硝酸(HNO2)是一元弱酸,不稳定,只能存在于较低温度的稀溶液中。室温时,亚硝酸(HNO2)的电离平衡常数Ka=5.1×10-4,H2CO3的电离平衡常数Ka1=4.2×10-7、Ka2=5.61×10-11。亚硝酸及其盐在实验和工业生产中有重要应用。请回答:
(1)在酸性条件下,NaNO2与KI按物质的量1︰1恰好完全反应,I-被氧化为I2,写出该反应的离子方程式________________。
(2)NaNO2溶液呈_____性(填“酸”“碱”或“中”),原因是________(用离子方程式表示)。要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用______(填序号)。
a.稀H2SO4 b.CO2 c.SO2
(3)若用电解法将废水中NO2-转换为N2除去,N2将在__________(填电极名称)生成。
(4)向含1 mol Na2CO3的溶液中加入1 mol HNO2后,c(CO32-)、c(HCO3-)、c(NO2-)由大到小的顺序为________________。
(5)25℃时,用0.100mol•L-1NaOH溶液滴定20.0mL某浓度的HNO2溶液,溶液的pH与NaOH溶液体积(V)的关系如图所示,(在该条件下HNO2不分解)
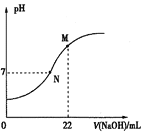
已知:M点对应溶液中,c(OH-)=c(H+)+c(HNO2)。则:
①原溶液中c(HNO2)为_________。
②下列关于N点对应溶液的说法正确的是______(填选项字母)。
A.溶质只有NaNO2
B.水电离出来的c(H+)=1×10-7 mol•L-1
C.溶液中:c(Na+)<c(OH-)
D.溶液中离子浓度:c(Na+)= c(NO2-)
-
氮是地球上含量丰富的原子元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)25℃时,0.1mol/LNH4NO3溶液中水的电离程度________(填“大于”、“等于”或“小于”) 0.1mol/L NaOH溶液中水的电离程度。
(2)若将0.1mol/L NaOH溶液和0.2mol/LNH4NO3溶液等体积混合,混合溶液中2c(NH4+)>c(NO3-),所得溶液中离子浓度由大到小的顺序是________。
(3)发射火箭时肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。经测定16g气体在上述反应中放出284kJ的热量。则该反应的热化学方程式是________。
(4)下图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图。
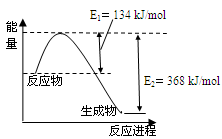
已知:N2(g)+O2(g)=2NO(g) △H=+180kJ/mol
2NO (g)+O2(g)=2NO2(g) △H=-112.3kJ/mol
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g)的△H是________。
N2(g)+2CO2(g)的△H是________。