-
工业上以乙苯催化脱氢制取苯乙烯的反应如下: (g)
(g)

 。现将xmol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强
。现将xmol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强 恒定
恒定 在某催化剂作用下,乙苯的平衡转化率随温度变化如下图所示。已知:气体分压
在某催化剂作用下,乙苯的平衡转化率随温度变化如下图所示。已知:气体分压 气体总压
气体总压 体积分数。不考虑副反应,下列说法正确的是( )
体积分数。不考虑副反应,下列说法正确的是( )

A.  时,向体系中通入水蒸气,
时,向体系中通入水蒸气, 正
正 、
、 逆
逆 均减小,且乙苯转化率降低
均减小,且乙苯转化率降低
B.  时,向体系中通入乙苯、苯乙烯、氢气各
时,向体系中通入乙苯、苯乙烯、氢气各 mol,平衡不移动
mol,平衡不移动
C.  时,用平衡分压代替平衡浓度表示的化学平衡常数
时,用平衡分压代替平衡浓度表示的化学平衡常数
D.  时平衡体系中苯乙烯的体积分数是
时平衡体系中苯乙烯的体积分数是 时的3倍
时的3倍
-
乙苯催化脱氢制苯乙烯反应:
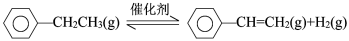
(1)已知:

计算上述反应的△H=________ kJ·mol-1。
(2)维持体系温度和总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=___________(用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)如右图所示:

①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实 。
②控制反应温度为600℃的理由是 。
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工艺——乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有_________(填编号)。
① CO2与H2反应,使乙苯脱氢反应的化学平衡右移
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利于CO2资源利用
-
反应

 在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.体积不变,增加水蒸气的量
B.将容器的体积缩小一半
C.保持体积不变,充入 使体系压强增大
使体系压强增大
D.压强不变充入 使容器体积增大
使容器体积增大
-
反应C(s)+H2O(g) CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.在密闭容器中通入水蒸气
B.升温
C.保持体积不变,充入氦气使体系压强增大
D.保持压强不变,充入氦气使容器体积增大
-
反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,达到平衡,下列条件能使平衡移动的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,达到平衡,下列条件能使平衡移动的是( )
A.增加C的量
B.加催化剂
C.保持体积不变,充入氮气使体系压强增大
D.保持压强不变,充入氮气使容器体积增大
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g) 2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
(1)若平衡时,容器体积为aL,写出该反应的平衡常数为:K=__________(用含a的代数式表示)
(2)反应进行到t1时,SO2的体积分数为_______________;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将________(填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量____2.1mol(填“<”、“>”或“=”),简单说明原因:____________。
(5)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆________v正 (填“<”、“>”或“=”)。
(6)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
| 容器1 | 容器2 | 容器3 |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 4 mol SO3 | 2 mol SO2、1 mol O2 |
| 平衡v正(SO2)/ mol·L-1·s-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
用“<”、“>”或“=”填入下列横线上:
c2______2c1,v1______v2;K1_____K3,p2____2p3;α1(SO2)_____α3(SO2);α2(SO3)+α3(SO2)_______1
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g) 2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
(1)若平衡时,容器体积为aL,写出该反应的平衡常数为:K=__________(用含a的代数式表示)
(2)反应进行到t1时,SO2的体积分数为_______________;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将________(填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量____2.1mol(填“<”、“>”或“=”),简单说明原因:____________。
(5)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆________v正 (填“<”、“>”或“=”)。
(6)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
| 容器1 | 容器2 | 容器3 |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 4 mol SO3 | 2 mol SO2、1 mol O2 |
| 平衡v正(SO2)/ mol·L-1·s-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
用“<”、“>”或“=”填入下列横线上:
c2______2c1,v1______v2;K1_____K3,p2____2p3;α1(SO2)_____α3(SO2);α2(SO3)+α3(SO2)_______1
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g) 2SO3(g);△H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol。试回答下列问题:
2SO3(g);△H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol。试回答下列问题:
(1)反应进行到t1时,SO2的体积分数为__;
(2)若在t1时充入一定量的氩气(Ar),SO2的物质的量将__(填“增大”、“减小”或“不变”);
(3)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量_2.1mol(填“<”、“>”或“=”),简单说明原因:__。
(4)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆_v正(填“<”、“>”或“=”)
-
在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气) xC(气)+yD(气)达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则x、y的值分别为
xC(气)+yD(气)达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则x、y的值分别为
A.x=3 y=1 B.x=4 y=1 C.x=5 y =1 D.x=8 y=2
-
(10分)将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)  2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)反应进行到t1时,SO2的体积分数为 ;
(2)若在t1时充入一定量的氩气(Ar),SO2的物质的量将 (填“增大”、“减小”或“不变”);
(3)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量 2.1mol(填“<”、“>”或“=”),简单说明原因 ;
(4)若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线。
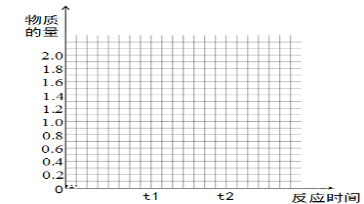
(g)
。现将xmol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强
恒定
在某催化剂作用下,乙苯的平衡转化率随温度变化如下图所示。已知:气体分压
气体总压
体积分数。不考虑副反应,下列说法正确的是( )

时,向体系中通入水蒸气,
正
、
逆
均减小,且乙苯转化率降低
时,向体系中通入乙苯、苯乙烯、氢气各
mol,平衡不移动
时,用平衡分压代替平衡浓度表示的化学平衡常数
时平衡体系中苯乙烯的体积分数是
时的3倍



