-
工业上用木炭粉和水蒸气在高温条件下反应制取H2,同时生成CO2。某学习小组在实 验室中模拟H2的工业生产过程并测定其产率,实验装置如下所示。
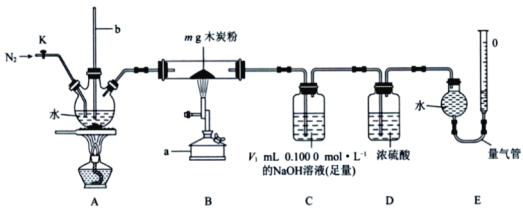
(1)仪器a的名称为_______________。仪器b的作用为____________________________。
(2)实验步骤:连接好装置,检查装置的气密性;______________________(按顺序填入下列步骤的序号)。
①向装置A、B、C、D中分别加入相应试剂,打开活塞K,通入一段时间N2。
②加热装置B处硬质玻璃管。
③关闭活塞K,连接盛有适量水的量气管。
④点燃装置A处酒精灯。
⑤待装置B处木炭粉完全反应后,停止加热。
(3)装置B处硬质玻璃管中发生的所有反应的化学方程式为______________________。
(4)读取B气管读数时,应注意的事项为冷却至室温、___________、视线与凹液面最低点相切;若仰视读取初始读数,则导致所测气体的体积___________(填“偏大”或“偏小”)。
(5)实验后所域取的气体体积为V2 mL标准状况);取装置C中液体,加入足量BaCl2溶液,过滤、洗涤,将滤液和洗涤液合并,以甲基橙为指示剂,用0.1000mol•L-1的盐酸标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为V3mL。
①达到滴定终点时的现象为____________________________________________。
②H2的产率为______________________(列出代数式即可)。
③还可通过___________,得出装置C中所吸收产物的物质的量。
(6)从安全角度考虑,该实验装置的缺陷为_________________________________。
-
工业上用木炭粉和水蒸气在高温条件下反应制取H2,同时生成CO2。某学习小组在实验室中模拟H2的工业生产过程并测定其产率,实验装置如下所示。
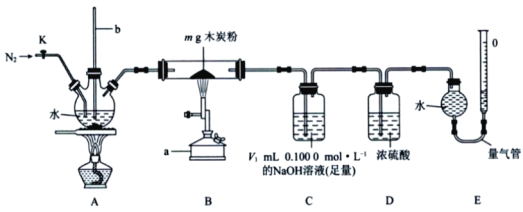
(1)仪器a的名称为_______________。仪器b的作用为________________。
(2)实验步骤:连接好装置,检查装置的气密性;___________(按顺序填入下列步骤的序号)。
①向装置A、B、C、D中分别加入相应试剂,打开活塞K,通入一段时间N2。
②加热装置B处硬质玻璃管。
③关闭活塞K,连接盛有适量水的量气管。
④点燃装置A处酒精灯。
⑤待装置B处木炭粉完全反应后,停止加热。
(3)装置B处硬质玻璃管中发生的所有反应的化学方程式为________________。
(4)读取B气管读数时,应注意的事项为冷却至室温、____、视线与凹液面最低点相切;若仰视读取初始读数,则导致所测气体的体积_____(填“偏大”或“偏小”)。
(5)实验后所得气体体积为V2 mL(标准状况);取装置C中液体,加入足量BaCl2溶液,过滤、洗涤,将滤液和洗涤液合并,以甲基橙为指示剂,用0.1000 mol·L−1的盐酸标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为V3mL。
①达到滴定终点时的现象为____________________。
②H2的产率为______________________(列出代数式即可)。
③还可通过___________,得出装置C中所吸收产物的物质的量。
(6)从安全角度考虑,该实验装置的缺陷为___________________。
-
工业上用空气氧化(NH4)2SO3的方法制取(NH4)2SO4,某研究小组用如图装置模拟该过程,并通过测定反应后溶液中SOT的浓度来计算该反应的转化率。
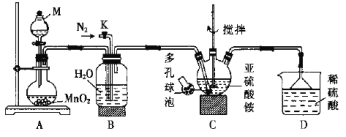
实验步骤如下:
①按图连接好装置,检查装置气密性;
②取200 mL 0.5000 mol•L-1(NH4)2SO3溶液(调节pH = 8)装入三颈烧瓶中,加入催化剂,控制气体流速为300 L•h-1,在温度为50℃下进行实验;
③反应2.5 h后,测定反应后溶液中SO32-的浓度。
回答下列问题:
(1)仪器M的名称为_____,仪器M中装有H2O2溶液,则装置A中发生反应的化学方程式为_______。
(2)实验中通如N2的目的是_____。
(3)装置B的作用是_____(任答一条)。
(4)装置C中采用多孔球泡的目的是_____,已知亚硫酸铵溶液的pH小于8,要调节装置C中溶液的pH=8,应向该溶液中加入一定量的_____(填标号
a NH3 • H2O b Ba(OH)2 c 澄清石灰水
(5)该实验缺少的装置是_____。
(6)取VmL反应后的溶液(反应前后体积不变)于碘量瓶中,滴入3滴淀粉溶液,用a mol•L-1的标准碘溶 液滴定至终点时,消耗碘水的体积为b mL,则(NH4 )2SO3的转化率为_____。
-
工业上用无机矿物资源生产部分材料。下列有关说法不正确的是
A.制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO
B.生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应
C.粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D.黄铜矿(CuFeS2)冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料
-
(14分)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ |
| CO | H2O | CO2 | H2 |
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
| | | | | | | |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、
“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为________%。
(3)计算容器②中反应的平衡常数K=________。
(4)下列叙述正确的是 ________(填字母序号)。
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q > 65.6 kJ
c.反应开始时,两容器中反应的化学反应速率相等
 d.容器①中,化学反应速率为:
d.容器①中,化学反应速率为:
(5)已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:________。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)________。
-
(14分)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ |
| CO | H2O | CO2 | H2 |
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
| | | | | | | |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为________%。
(3)计算容器②中反应的平衡常数K=________。
(4)下列叙述正确的是 ________(填字母序号)。
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q > 65.6 kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:
(5)已知:2H2 (g) + O2 (g) ="=" 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:________。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用
200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)________。
-
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ |
| CO | H2O | CO2 | H2 |
| ① | 1 | 4 | | | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | | | t2 | 放出热量:Q |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量.
(2)容器①中反应达平衡时,CO的转化率为________%.
(3)计算容器②中反应的平衡常数K=________.
(4)下列叙述正确的是________(填字母序号).
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q>65.6kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:
(5)已知:2H2(g)+O2(g)═2H2O (g)△H=-484kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:________.
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6mol.若用200mL 5mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)________.
-
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41kJ/mol
某小组研究在相同温度下该反应过程中的能量变化.他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应.相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ |
| CO | H2O | CO2 | H2 |
| ① | 1 | 4 | | | t1 | 放出热量:32.8 kJ |
| ② | 2 | 8 | | | t2 | 放出热量:Q |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量.
(2)容器①中反应达平衡时,CO的转化率为________%.
(3)下列叙述正确的是________(填字母序号).
A、平衡时,两容器中H2的体积分数相等
B、容器②中反应达平衡状态时,Q>65.6kJ
C、反应开始时,两容器中反应的化学反应速率相等 D、容器①中,化学反应速率为
D、容器①中,化学反应速率为
(4)已知:2H2(g)+O2(g)=2H2O (g)△H=-484kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:________.
(5)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6mol.若用200ml、5mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)________.
-
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ /mol
CO2(g)+H2(g) △H=-41kJ /mol
某小组研究在相同温度下该反应过程中的能量变化。他们分別在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器 编号 | 起始时各物质物质的M/mol | 达到平衡的时间/min | 达平衡时体系能量 的变化/kJ |
| CO | H2O | CO2 | H2 |
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量: 32.8 kJ |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q |
| | | | | | |
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量________(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为__________%。
(3)计算容器②中反应的平衡常数K=___________。
(4)下列叙述正确的是________(填字母序号)。
A.平衡时,两容器中H2的体积分数相等
B.容器②中反应达平衡状态时Q>65.6kJ
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时两容器中正反应速率相等
(5)容器①中反应进行到tmin时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)____________。
-
(10分)工业上用固体硫酸亚铁制取Fe2O3,反应原理是: 2FeSO4 Fe2O3 +SO2 ↑+SO3 ↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
Fe2O3 +SO2 ↑+SO3 ↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
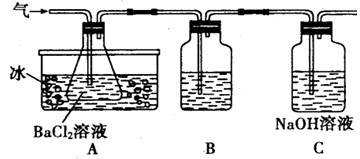
请回答相关问题:
(1)Fe2O3俗称为 ________ 不溶于水而易溶于酸,Fe2O3与稀盐酸反应的离子方程式为 ________
(2)A瓶所盛试剂的作用是________C瓶所盛试剂的作用是________
________,用冷水冷却的原因是________;B瓶所盛的试剂是________
(3)将此反应生成的气体通入A瓶的BaCI2溶液中,下列说法正确的是________ (填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀 C.逸出SO3气体 D.逸出SO2气体
理由是
(4)在用固体硫酸亚铁制取Fe2O3的反应中,还原产物是________ ,标准状况下每生成11. 2L SO2气体,转移电子的物质的量为________ mol.



