-
(10分)工业上用固体硫酸亚铁制取Fe2O3,反应原理是: 2FeSO4 Fe2O3 +SO2 ↑+SO3 ↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
Fe2O3 +SO2 ↑+SO3 ↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
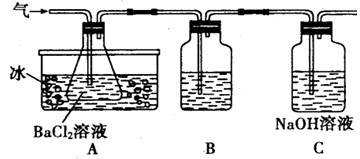
请回答相关问题:
(1)Fe2O3俗称为 ________ 不溶于水而易溶于酸,Fe2O3与稀盐酸反应的离子方程式为 ________
(2)A瓶所盛试剂的作用是________C瓶所盛试剂的作用是________
________,用冷水冷却的原因是________;B瓶所盛的试剂是________
(3)将此反应生成的气体通入A瓶的BaCI2溶液中,下列说法正确的是________ (填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀 C.逸出SO3气体 D.逸出SO2气体
理由是
(4)在用固体硫酸亚铁制取Fe2O3的反应中,还原产物是________ ,标准状况下每生成11. 2L SO2气体,转移电子的物质的量为________ mol.
-
(10分)工业上用固体硫酸亚铁制取Fe2O3,反应原理是: 2FeSO4 Fe2O3 +SO2 ↑+SO3 ↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)
Fe2O3 +SO2 ↑+SO3 ↑某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)

请回答相关问题:
(1)Fe2O3俗称为 ________ 不溶于水而易溶于酸,Fe2O3与稀盐酸反应的离子方程式为 ________
(2)A瓶所盛试剂的作用是________C瓶所盛试剂的作用是________
________,用冷水冷却的原因是________;B瓶所盛的试剂是________
(3)将此反应生成的气体通入A瓶的BaCI2溶液中,下列说法正确的是________ (填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀 C.逸出SO3气体 D.逸出SO2气体
理由是________
(4)在用固体硫酸亚铁制取Fe2O3的反应中,还原产物是________ ,标准状况下每生成11. 2L SO2气体,转移电子的物质的量为________ mol.
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:2FeSO4
 Fe2O3+SO2↑+SO3↑.
Fe2O3+SO2↑+SO3↑.
某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量.
(SO2沸点为-10.02℃)请回答相关问题:
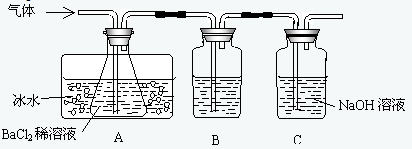
(1)A瓶所盛试剂的作用是______;B瓶所盛的试剂是______;C瓶所盛试剂的作用是______;
(2)A瓶要用冷水冷却的原因是______;
(3)将此反应生成的气体通入A瓶BaCl2溶液中,则______;(填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀 C.逸出SO3气体 D.逸出SO2气体
理由是______;
(4)反应后若用A瓶内的混合物来测定已分解的FeSO4的质量,其实验操作的第一步是(简述操作步骤)______.
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:

2FeSO4 Fe2O3 + SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、(II)x溶液、(III)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
A.(I)中会生成BaSO3、BaSO4两种沉淀
B.可将(I)中的BaCl2溶液改为Ba(NO3)2溶液
C.(III)的作用是检验生成的SO2气体
D.(II)所盛x应为品红溶液
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4 Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。
Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。
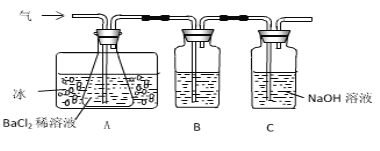
(1)B中盛放的溶液可以是_________________。
(2)A中放冰的作用是_______________________。
(3)设计一个简单的实验方案探究A中得到的沉淀的成分。___________________________________。
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:
2FeSO4Fe2O3+SO2↑+SO3↑
某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)x溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是
A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀
B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液
C.(Ⅱ)所盛x应为品红溶液
D.(Ⅲ)的作用是检验生成的SO2气体
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)X溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是
A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀
B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液
C.(Ⅱ)所盛X应为品红溶液
D.(Ⅲ)的作用是吸收有毒的SO2气体
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)X溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀
B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液
C.(Ⅱ)所盛X应为品红溶液
D.(Ⅲ)的作用是检验生成的SO2气体
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有(Ⅰ)BaCl2溶液、(Ⅱ)X溶液、(Ⅲ)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
A.(Ⅰ)中会生成BaSO3、BaSO4两种沉淀
B.可将(Ⅰ)中的BaCl2溶液改为Ba(NO3)2溶液
C.(Ⅱ)所盛X可为品红溶液
D.(Ⅲ)的作用是吸收有毒的SO2气体
-
工业上用固体硫酸亚铁制取颜料铁红,反应原理是:2FeSO4  Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
A.(I)中会生成 BaSO3、BaSO4两种沉淀
B.可将(I)中的 BaCl2溶液改为 Ba ( NO3 )2溶液
C.(II)所盛 x应为品红溶液
D.( III)的作用是检验生成的SO2 气体
Fe2O3 +SO2 ↑+SO3 ↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量(已知SO2沸点为- 10. 02℃)



