-
完成下列氧化还原反应相关问题:
I.配平下面的氧化还原方程式:___ Na2SO3+____ KIO3+____ H2SO4 =____ Na2SO4+____ K2SO4+____ I2+____H2O。
II.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为
2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥表示)_______________。
(2)浓盐酸在反应中显示出来的性质是________(填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
若标准状况下产生4.48L Cl2,则参加反应的KClO3的质量为_______g,被氧化的盐酸的物质的量为________mol,转移电子的物质的量为________mol。
(3)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。(提示:ClO2与Cl2消毒时氯元素都被还原为最低价)
高二化学综合题困难题查看答案及解析
-
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X.下列说法中正确的是
A.该未知物X为NaI
B.该反应中氧化剂与还原剂的物质的量之比为5:2
C.该反应中,发生氧化反应的过程是KIO3→I2
D.由反应可知还原性强弱顺序为:Na2SO3>I2
高二化学选择题简单题查看答案及解析
-
制高效消毒剂ClO2的反应如下:2NaClO3+Na2SO3+H2SO4=2Na2SO4+2ClO2↑+H2O。下列有关该反应的说法正确的是
A. Na2SO3是氧化剂 B. H2SO4被还原
C. Na2SO3发生还原反应 D. 每消耗1 mol NaClO3转移6.02×1023个电子
高二化学单选题中等难度题查看答案及解析
-
请用氧化还原反应相关知识回答下列问题:
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是_____.
②KBrO3在反应中生成单质 X,则X的化学式为_____.
③根据上述反应可推知_____.
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
高二化学综合题中等难度题查看答案及解析
-
反应2NaClO3+Na2SO3+H2SO4===2ClO2↑+2Na2SO4+H2O可制备高效消毒剂ClO2。对于该反应的说法正确的是
A. NaClO3被氧化 B. Na2SO3是还原剂
C. H2SO4是氧化剂 D. 每生成1 mol ClO2转移2 mol电子
高二化学选择题中等难度题查看答案及解析
-
(9分)亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是:
Na2SO3+KIO3+H2SO4 ==Na2SO4+K2SO4+I2+H2O,
(1)其中氧化剂是________,若反应中有5mol电子转移,则生成碘是________mol。
该反应过程和机理较复杂,一般认为分为以下几步:
①IO3-+SO32-→IO2-+SO42-(慢) ②IO2-+ SO32-→IO-+SO42-(快)
③5I-+6H++ IO3-→3I2+3H2O(快) ④I2+ SO32-+ H2O→2I-+ SO42-+2H2(快)
(2)根据上述条件推测,此反应的总的反应速率由________步反应决定。
高二化学填空题简单题查看答案及解析
-
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。回答下列问题:
(1)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为________。
(2)用如图装置可以测定混合气中ClO2的含量:
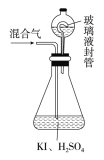
Ⅰ.在锥形瓶中加入足量的碘化钾,用50mL水溶解后,再加入3mL稀硫酸;
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中;
Ⅴ.用0.1000mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为__________,反应中ClO2为_______剂(氧化或还原)。
②玻璃液封装置的作用是__________。
③Ⅴ中加入的指示剂通常为________,滴定至终点的现象是___________。
④测得混合气中ClO2的质量为________g。
(3)用ClO2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是________(填标号)。
a明矾b碘化钾c盐酸d硫酸亚铁
高二化学实验题中等难度题查看答案及解析
-
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
A.该未知物X为Na2SO4
B.该反应的氧化剂是KIO3
C.该反应中,发生氧化反应的过程是KIO3→I2
D.由反应可知还原性强弱顺序为:Na2SO3>I2
高二化学选择题中等难度题查看答案及解析
-
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
A.该未知物X为Na2SO4
B.该反应的氧化剂是KIO3
C.该反应中,发生氧化反应的过程是KIO3→I2
D.由反应可知还原性强弱顺序为:Na2SO3>I2
高二化学选择题中等难度题查看答案及解析
-
高锰酸钾广泛用作氧化剂。现有一个氧化还原反应的体系中共有KMnO4、MnSO4、H2O、Fe2(SO4)3、
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):____________。
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。
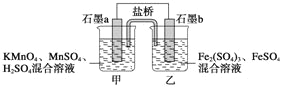
回答下列问题:
(1)此原电池的正极是石墨__________(填“a”或“b”),发生________反应。
(2)电池工作时,盐桥中的SO42-移向________(填“甲”或“乙”)烧杯。
(3)乙烧杯中的电极反应式分别为__________________。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
高二化学简答题困难题查看答案及解析