铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如表所示:
则NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A. I2、H2O2、KMnO4、NaBiO3 B. H2O2、I2、NaBiO3、KMnO4
C. NaBiO3、KMnO4、H2O2、I2 D. KMnO4、NaBiO3、I2、H2O2
高二化学单选题中等难度题
铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如表所示:

则NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A. I2、H2O2、KMnO4、NaBiO3 B. H2O2、I2、NaBiO3、KMnO4
C. NaBiO3、KMnO4、H2O2、I2 D. KMnO4、NaBiO3、I2、H2O2
高二化学单选题中等难度题
铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如表所示:

则NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A. I2、H2O2、KMnO4、NaBiO3 B. H2O2、I2、NaBiO3、KMnO4
C. NaBiO3、KMnO4、H2O2、I2 D. KMnO4、NaBiO3、I2、H2O2
高二化学单选题中等难度题查看答案及解析
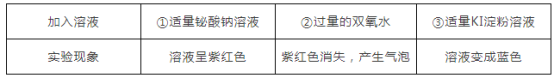
铋(Bi)位于元素周期表中ⅤA族,其价态为+3价较稳定,铋酸钠(NaBiO3)溶液呈无色,取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如下表所示:
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI-淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
关于NaBiO3、KMnO4、I2、H2O2的氧化性由强到弱的顺序为( )
A.I2、H2O2、KMnO4、NaBiO3
B.H2O2、I2、NaBiO3、KMnO4
C.NaBiO3、KMnO4、H2O2、I2
D.KMnO4、NaBiO3、I2、H2O2
高二化学选择题困难题查看答案及解析
(6分)(1)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
NaBiO3 + MnSO4 + H2SO4===Na2SO4 + Bi2(SO4)3 + NaMnO4 + H2O
①上述反应中还原产物是________,若有2mol氧化剂在该反应中被还原,则生成的MnO4-被还原为Mn2+时,能将________ molHCl氧化成Cl2;
② 写出NaBiO3固体溶于浓盐酸产生黄绿色气体的化学反应方程式________。
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(S)+2H+(aq)=== Cu2+(aq)+H2(g) ΔH=64.39kJ·mol-1
2H2O2(L)===2H2O(L)+O2(g) ΔH=-196.46kJ·mol-1
H2(g)+ O2(g)===H2O(L) ΔH=-285.84kJ·mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 ________ 。
高二化学填空题简单题查看答案及解析
运用元素周期律分析下面的推断,其中错误的是( )
①硒化氢(H2Se)是无色,有毒,比H2S稳定的气体
②铊(T既能与盐酸作用产生氢气,又有跟Na0H溶液反应放出氢气
③砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸
④锂在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤硫酸锶(SrSO4)是难溶于水的白色固体
A.①②③④ B.①②④ C.①③⑤ D.②④⑤
高二化学单选题中等难度题查看答案及解析
Fe、Cu都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)Fe位于元素周期表的_____区,Fe2+的价层电子排布图为_____。
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。含该离子的配合物的化学式是____。
②铁的另一种配合物铁氰化钾K3[Fe(CN)6]俗称赤血盐,可用于检验Fe2+,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理_____,该赤血盐其配体的电子式为:_____。
(3)Cu的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
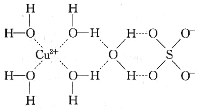
0.5mol该化合物中含有σ键的个数为_____。Cu2+与NH3还可形成[Cu(NH3)4]2+配离子,该配离子的立体构型为____。
高二化学解答题中等难度题查看答案及解析
已知:氧化性:KMnO4>HNO3;Bi 元素+3价较稳定,Na3BiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的Na3BiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为___________________________;
(2)实验④中的现象为:________________________________________________;
(3)实验②反应的离子方程式是:
__________________________________________________________________;
(4)实验③反应的离子方程式是:________________________________________。
高二化学填空题简单题查看答案及解析
硫的多种化合物在工业中有重要的应用。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为__________。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为___________(填化学式)。
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2。该反应的化学方程式为____________________。
(2)铬会造成环境污染.某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为____________。
②处理后的废水中Cr3+的物质的量浓度为__________mol·L-1。
高二化学简答题困难题查看答案及解析
硫的多种化合物在工业中有重要的应用。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为__________。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为___________(填化学式)。
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2。该反应的化学方程式为____________________。
(2)铬会造成环境污染.某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为____________。
②处理后的废水中Cr3+的物质的量浓度为__________mol·L-1。
高二化学简答题困难题查看答案及解析
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
A. X与Y形成化合物时,X可以显负价,Y显正价
B. 在元素周期表中X可能位于Y的右面
C. 第一电离能X一定大于Y
D. Y的气态氢化物的稳定性小于X的气态氢化物的稳定性
高二化学单选题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析