下列有关实验原理或实验操作正确的是( )
A. 将氯化铁固体溶于稀盐酸配制FeCl3溶液
B. 利用下图装置定量测定H2O2的分解速率
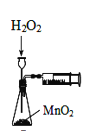
C. 如下图所示,关闭弹簧夹检查装置的气密性
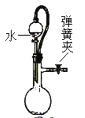
D. 称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol/L的NaOH溶液
高二化学单选题中等难度题
下列有关实验原理或实验操作正确的是( )
A. 将氯化铁固体溶于稀盐酸配制FeCl3溶液
B. 利用下图装置定量测定H2O2的分解速率

C. 如下图所示,关闭弹簧夹检查装置的气密性

D. 称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol/L的NaOH溶液
高二化学单选题中等难度题
下列有关实验原理或实验操作正确的是( )
A. 将氯化铁固体溶于稀盐酸配制FeCl3溶液
B. 利用下图装置定量测定H2O2的分解速率

C. 如下图所示,关闭弹簧夹检查装置的气密性

D. 称取4.0gNaOH,放入100mL容量瓶中,加水稀释,配制1.0mol/L的NaOH溶液
高二化学单选题中等难度题查看答案及解析
下列有关实验原理或实验操作正确的是
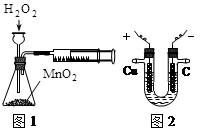
A.利用右图1装置定量测定H2O2的分解速率
B.利用右图2装置模拟工业上电解饱和食盐水
C.配制FeCl3溶液时加入少量盐酸,以防止溶液浑浊
D.用HNO2溶液做导电性实验,灯光较暗,说明HNO2是弱电解质
高二化学选择题简单题查看答案及解析
下列实验操作能达到目的是 ( )
A.配制FeSO4溶液时,将FeSO4固体溶于浓盐酸中,然后稀释至所需浓度
B.将FeCl3溶液加热蒸干灼烧获得Fe2O3固体
C.向明矾溶液中加入一定量NaOH,制备Al(OH)3胶体
D.室温下,测得pH=5的 NaHSO4溶液与pH=9的 NaHCO3溶液中水的电离程度相等
高二化学单选题中等难度题查看答案及解析
(16分)
(1)下列有关实验操作或结果的说法中错误的是
A.实验室在配制FeCl3溶液时,先将FeCl3溶于一定量的浓盐酸中,再加蒸馏水稀释至所需浓度
B.用广泛pH试纸测量Na2S溶液的pH时,得pH=10.5
C.滴定管洗净后经蒸馏水润洗后,即可注入标准液进行中和滴定实验
D.电解盐酸溶液后(盐酸过量),再通入一定量HCl气体时,电解质溶液可恢复到和原来一样
(2)氢氧化铝的酸式电离方程式:________
(3)向明矾溶液中逐滴加入氢氧化钡溶液至铝离子刚好沉淀完全时,离子反应总方程式为:________
(4)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)________。
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH―)减小
(5)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),________和________两种粒子的物质的量之和比OH―多0.05mol。
高二化学填空题中等难度题查看答案及解析
下列有关盐类水解的应用不正确的是
A.明矾、氯化铁晶体可用于净水
B.实验室通常可使用热的纯碱溶液去除油污
C.实验室配制FeCl3溶液时可加入少量盐酸
D.直接加热CuCl2溶液能得到CuCl2固体
高二化学单选题中等难度题查看答案及解析
下列有关盐类水解的应用不正确的是
A. 明矾、氯化铁晶体可用于净水
B. 实验室通常可使用热的纯碱溶液去除油污
C. 实验室配制FeCl3溶液时可加入少量盐酸
D. 直接加热CuCl2溶液能得到CuCl2固体
高二化学选择题中等难度题查看答案及解析
下列说法正确的是( )
A.配制FeCl3溶液时,将FeCl3固体溶于适量盐酸中,然后再用水稀释到所需的浓度
B.为绘制中和滴定曲线,在滴定过程中,每隔相同时间用pH计测定一次锥形瓶中溶液的pH
C.测定溶液的pH时,应先将pH试纸润湿,然后进行检测
D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等
高二化学单选题中等难度题查看答案及解析
为达到预期的实验目的,下列操作中正确的有( )
①配制FeCl3溶液时,将FeCl3固体溶于盐酸中,然后再用水稀释到所需的浓度
②用10 mL的量筒量取4.80 mL的浓硫酸
③蒸发溶液时,边加热边搅拌,直至蒸发皿中的液体蒸干
④向无色溶液中加入BaCl2溶液,生成白色沉淀,再加稀硝酸,沉淀不消失,由此确定该溶液中一定含有SO
⑤为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量
⑥中和热测定的实验中使用的玻璃仪器只有2种
⑦实验室可利用浓氨水和碱石灰混合的方法制取少量氨气
⑧除去NO中混有的NO2气体可通过水洗,再干燥后用向上排空气法收集
A. 5项 B. 4项
C. 3项 D. 2项
高二化学单选题中等难度题查看答案及解析
某研究小组用下图装置进行SO2 与FeCl3溶液反应的相关实验(夹持装置已略去)。
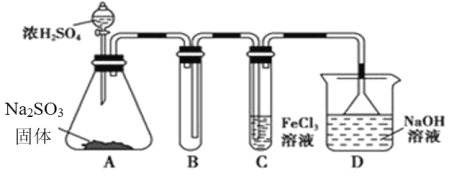
(1)配制氯化铁溶液时,需先把氯化铁晶体溶解在盐酸中,再加水稀释,这样操作的目的是___。
(2)通入足量SO2时,装置C中观察到的现象为_______________。
(3)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式____________;
②检验有Fe2+生成的方法是____________;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42 -,该做法不合理,理由是____________。
(4)D装置中倒置漏斗的作用是____________。
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有____________(填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
高二化学实验题中等难度题查看答案及解析
为达到预期的实验目的,下列操作中正确的是
A.用玻璃棒蘸取待测液滴在润湿的pH试纸上,测得其pH为12
B.制FeCl3溶液时,将FeCl3固体溶于盐酸中,然后再用水稀释到所需的浓度
C.中和热测定的实验中使用的玻璃仪器只有2种
D.在滴定时,左手操作锥形瓶,右手操作滴定管开关
高二化学单选题中等难度题查看答案及解析