-
碳、氮、氧、磷、硫、铁,锌、铜等都是组成蛋白质的重要元素。回答下列问题:
(1)Fe的基态原子的核外电子排布式为_________,3d能级上的未成对电子数为____。
(2)在C、N、O、P、S五种元素中,第一电离能最大的元素是_____(填元素符号,下同),电负性最大的元素是______
(3)氨基乙酸(H2NCH2COOH)是蛋白质完全水解的产物之一,其中C原子的杂化轨道类型为______;1molH2NCH2COOH中含有 键的数目为_____NA。
键的数目为_____NA。
(4)蛋白质在体内部分被氧化生成尿素[CO(NH2)2]、二氧化碳、水等排出体外。
①CO2、H2O分子的空间构型分别为_____、_____。
②尿素的熔点为132.7℃,其固体属于_____晶体。
③尿素易溶于水,其原因除都是极性分子外,还有_________。
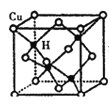
(5)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为____。若该晶体的密度为ρg·cm—3,阿伏加德罗常数的值为NA,则该晶胞的棱长为_____nm(用含ρ和NA的式子表示)
-
已知X、Y、Z、L四种元素是组成蛋白质的基础元素且原子序数依次增大。回答下列问题:
(1)L的元素符号为________ ;Y元素原子核外电子中,未成对电子数与成对电子数之比为______;四种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3可构成分子A,A的电子式为________;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物。已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5 %,且该分子结构中只有单键。则B的结构式为____________。若64 g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000 kJ的热量,写出该反应的热化学方程式________。
(3)硒(Se)是人体必需的微量元素,与元素L同一主族,该族第2 ~5周期元素单质分别与H2反应生成l mol气态氢化物产生的热量数据如下,其中能表示生成1 mol硒化氢所产生的热量的是__________(选填字母编号)。
a.—99.7 kJ b.—29.7 kJ c.+20.6 kJ d.+241.8 kJ
-
碳元素以C—C键构成了有机界,硅元素以 键构成了整个矿物界,锗元素是重要的国家战略资源。碳族元素组成了有机界、无机界和当代工业。回答下列问题:
键构成了整个矿物界,锗元素是重要的国家战略资源。碳族元素组成了有机界、无机界和当代工业。回答下列问题:
(1)基态锗( )原子的核外电子排布式为
)原子的核外电子排布式为 _____;
_____; 分子空间构型是__________。
分子空间构型是__________。
(2) 发生水解的机理如图:
发生水解的机理如图:
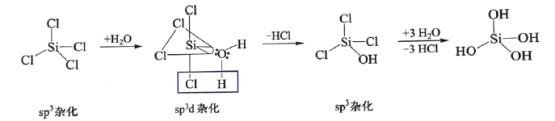
 不能按照上述机理发生水解反应,原因是____________________。
不能按照上述机理发生水解反应,原因是____________________。
(3)金刚石熔点为4440℃,晶体硅熔点为1410℃,金刚石熔点比晶体硅高的原因是_______。
(4)C和 经常形成原子晶体,原子晶体的配位数普遍低于离子晶体,原因是_____。
经常形成原子晶体,原子晶体的配位数普遍低于离子晶体,原因是_____。
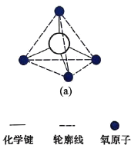
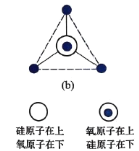
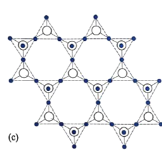
(5)在硅酸盐中, 四面体[如图(a)和(b)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(c)为片层状结构的多硅酸根,其中
四面体[如图(a)和(b)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(c)为片层状结构的多硅酸根,其中 原子的杂化方式为______,化学式为_______。
原子的杂化方式为______,化学式为_______。
(6)铝硅酸盐分子筛在化工领域有重要的应用。铝硅酸盐结构中 价铝部分地置换
价铝部分地置换 四面体结构中
四面体结构中 价的硅。从结构角度分析
价的硅。从结构角度分析 价铝能够置换
价铝能够置换 价硅的原因是_________。
价硅的原因是_________。
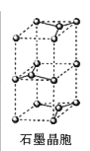
(7)石墨采取六方最密堆积方式,晶胞结构如图。晶胞参数为底边长 ,高
,高 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则石墨晶体的密度为_______
,则石墨晶体的密度为_______ 。
。
-
材料是人类文明进步的阶梯,第ⅢA、ⅣA、VA族元素是组成特殊材料的重要元素。请回答下列问题:
(1)基态Ge原子的价层电子排布图为___________;基态As原子核外能量最高能级的电子云形状为___________。
(2)Si、P、S、Cl的第一电离能由大到小的顺序为___________。
(3M与Ga位于同周期,M3+的一种配合物组成为[M(NH3)5(H2O)]Cl3。
①下列有关NH3、H2O的说法正确的是___________(填字母)。
a分子空间构型相同 b中心原子杂化类型相同 c.键角大小相同
②1mol[M(NH3)5(H2O)]3+含___________molσ键。
③配合物T与[M(NH3)5(H2O)]Cl3组成元素相同,中心离子的配位数相同。1molT溶于水,加入足量AgNO3溶液可生成2 mol AgCl。则T的化学式为______________________。
(4)碳和钨组成一种晶体,其熔点为2870℃,硬度接近金刚石,其晶胞结构如图甲所示,则其化学式为______________________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图乙所示,该晶胞中B原子所处空间类型为___________(填“立方体”“正四面体”或“正八面体”),空间的填充率为___________。
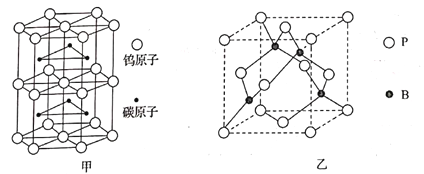
已知该晶体的密度为ρg·cm-3,NA是阿伏加德罗常数的值。BP晶胞中面心上6个P原子相连构成正八面体,该正八面体的边长为___________pm(列式即可)。
-
氨、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物用途广泛。回答下列问题:
(1)基态P原子的核外电子排布式为_____, 磷及其同周期相邻元素第一电离能由大到小的顺序是______________________。
(2)NH3比PH3易液化的原因是______________________。
(3)自然固氨现象发生的一系列化学变化:N2→NO→NO2→HNO3→NO3- 解释了民谚“雷雨发庄稼”的原理。
①N2分子结构中。σ键和π键之比为_________,己知N N的键能为946kJ·mol-1,远大于N—N的键能(193 kJ·mol-1) 的三倍,原因是______________________。
N的键能为946kJ·mol-1,远大于N—N的键能(193 kJ·mol-1) 的三倍,原因是______________________。
②NO3-中N原子采取___________杂化方式,其空间构型为__________,写出它的一种等电子体的化学式_____________________。
③已知酸性: HNO3>HNO2,下列相关见解合理的是_________________。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.HNO3中氮元素的正电性更高,在水溶液中更易电离出H+,酸性强于HNO2
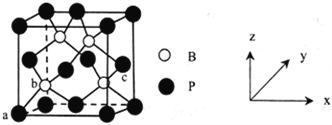
(4)磷化硬(BP) 是一种超硬耐磨涂层材料,其晶胞结构如图所示,图中a点和b点的原子坐标参数依次为(0,0,0)、( ,
,  ,
,  ),则c 点的原子坐标参数为_______。已知该晶体密度为ρg·cm-3,则B-P键的键长为_____pm (阿伏加德罗常数用NA表示,列出计算式即可)。
),则c 点的原子坐标参数为_______。已知该晶体密度为ρg·cm-3,则B-P键的键长为_____pm (阿伏加德罗常数用NA表示,列出计算式即可)。
-
氨、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物用途广泛。回答下列问题:
(1)基态P原子的核外电子排布式为_____, 磷及其同周期相邻元素第一电离能由大到小的顺序是______________________。
(2)NH3比PH3易液化的原因是______________________。
(3)自然固氨现象发生的一系列化学变化:N2→NO→NO2→HNO3→NO3- 解释了民谚“雷雨发庄稼”的原理。
①N2分子结构中。σ键和π键之比为_________,己知N N的键能为946kJ·mol-1,远大于N—N的键能(193 kJ·mol-1) 的三倍,原因是______________________。
N的键能为946kJ·mol-1,远大于N—N的键能(193 kJ·mol-1) 的三倍,原因是______________________。
②NO3-中N原子采取___________杂化方式,其空间构型为__________,写出它的一种等电子体的化学式_____________________。
③已知酸性: HNO3>HNO2,下列相关见解合理的是_________________。
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.HNO3中氮元素的正电性更高,在水溶液中更易电离出H+,酸性强于HNO2
(4)磷化硬(BP) 是一种超硬耐磨涂层材料,其晶胞结构如图所示,图中a点和b点的原子坐标参数依次为(0,0,0)、( ,
,  ,
,  ),则c 点的原子坐标参数为_______。已知该晶体密度为ρg·cm-3,则B-P键的键长为_____pm (阿伏加德罗常数用NA表示,列出计算式即可)。
),则c 点的原子坐标参数为_______。已知该晶体密度为ρg·cm-3,则B-P键的键长为_____pm (阿伏加德罗常数用NA表示,列出计算式即可)。

-
蛋白质是构成生物体的基本物质,蛋白质的组成元素主要有氢、碳、氮、氧、硫,同时还有微量元素铁、锌等。回答下列问题:
(1)在基态 原子中,核外电子占据的最高能级的电子云轮廓图为________形。
原子中,核外电子占据的最高能级的电子云轮廓图为________形。
(2)常见的含氮微粒有 、
、 、
、 等。与
等。与 互为等电子体的分子为________(写出一种)。根据价层电子对互斥理论,可推知
互为等电子体的分子为________(写出一种)。根据价层电子对互斥理论,可推知 的空间构型为________,
的空间构型为________, 比
比 更容易液化的原因是________。
更容易液化的原因是________。
(3)将足量的氨水逐滴加入到 溶液中,先生成沉淀,然后沉淀溶解生成配合物
溶液中,先生成沉淀,然后沉淀溶解生成配合物 ,该配合物中的阳离子结构式为________;
,该配合物中的阳离子结构式为________; 中的硫原子杂化方式为________;用价层电子对互斥理论解释
中的硫原子杂化方式为________;用价层电子对互斥理论解释 的键角大于
的键角大于 :________。
:________。
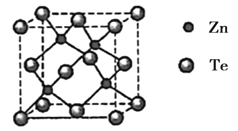
(4)碲化锌晶体有两种结构,其中一种晶胞结构如图:晶胞中与Zn原子距离最近的Te原子围成________形;与Te原子距离最近的Te原子有________个;若与Zn原子距离最近的Te原子间距为apm,则晶体密度为________ (列出计算式即可)。
(列出计算式即可)。
-
组成生命的最基本元素之一是碳,其单质及化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子价电子原子轨道表示式为________,其核外有________种空间运动状态的电子.
(2) 有机物中都含有碳原子,这和碳原子电子云的成键特点有关,试解释有机物种类繁多的原因________ 。
(3) 比较下列碳酸盐在一定温度下会发生分解的温度和对应的阳离子半径,分析其变化规律及原因_____________。
| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离了半径/pm | 66 | 99 | 112 | 135 |
(4)1828 年,德国化学家乌勒(F·Wohler)冲破了生命力学说的束缚,在实验室里将无机物氰酸铵(NH4CNO)溶液蒸发,得到了有机物尿素[CO(NH2)2]。尿素中C、N、O第一电离能大小顺序为____________。
(5) 碳的同素异形体有多种,其中一种为石墨,系平面层状结构。同一层内每个碳原子与其它三个碳原子以C -C 键相连构成平面正六边形,且层间可以滑动,它的结构如图所示。其中碳原子的杂化方式为_______,层间存在的作用力为__________。
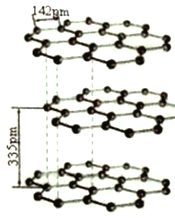
(6)石墨晶体二维结构的特殊性。
①同一层面内的平面六元并环结构(见上图)。在含lmolC原子的石墨中,有_____个平面正六边形。
②已知石墨层间距为335pm,C-C键长为142pm,其密度______g/cm3(已知:lpm=10-10cm。列出计算式即可)
-
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为______________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是_____________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是______________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为____,C原子的杂化形式为______。
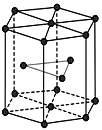
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______。
-
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________I1(Cu)(填“大于”或“小于”)。原因是______________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是__________________________________________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________,C原子的杂化形式为___________________。
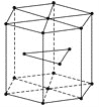
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为____________________。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为________g·cm-3(列出计算式)。
键的数目为_____NA。












