盐酸芬氟拉明的分子结构如图所示,它是目前国内上市的减肥药主要化学成分,因患者在临床使用中出现严重不良反应已停用。下列关于盐酸芬氟拉明的说法不正确的是
A. 不属于苯的同系物 B. 该物质可发生加成反应
C. 苯环上的一氯取代物有4种 D. 其分子式为C12H16NF3Cl
高二化学单选题中等难度题
盐酸芬氟拉明的分子结构如图所示,它是目前国内上市的减肥药主要化学成分,因患者在临床使用中出现严重不良反应已停用。下列关于盐酸芬氟拉明的说法不正确的是
A. 不属于苯的同系物 B. 该物质可发生加成反应
C. 苯环上的一氯取代物有4种 D. 其分子式为C12H16NF3Cl
高二化学单选题中等难度题
盐酸芬氟拉明的分子结构如图所示,它是目前国内上市的减肥药主要化学成分,因患者在临床使用中出现严重不良反应已停用。下列关于盐酸芬氟拉明的说法不正确的是
A. 不属于苯的同系物 B. 该物质可发生加成反应
C. 苯环上的一氯取代物有4种 D. 其分子式为C12H16NF3Cl
高二化学单选题中等难度题查看答案及解析
2010年10月30日曲美减肥胶囊全国下架,主要成分在欧美被禁。其主要成分盐酸西布曲明的结构如右图所示,有关说法错误的是( )
A.分子式:C17H26ClN
B.水解产物之一可用FeCl3溶液检验
C.该物质共平面的原子不少于12个
D.属于芳香烃类,可与3 mol H2加成,不溶于水
高二化学选择题困难题查看答案及解析
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”。某研究性学习小组拟对融雪氯盐(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究。
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |
该小组设计流程如图

(1)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入___溶液(填化学式),看是否有沉淀生成。
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成。下列三种溶液,其沉淀效果最好的是__。
A.0.1mol·L-1Na2CO3溶液 B.0.1mol·L-1Na2SO3溶液 C.0.1mol·L-1Na2C2O4溶液
(2)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在____以下。
(3)对溶液B加热并不断滴加6mol·L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C。该操作的目的是___。
(4)溶液C倒入蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到有大量固体析出时停止加热。
高二化学实验题中等难度题查看答案及解析
2015年冬季,雾霾天气严重影响了我国北方地区。国内电力行业和供暖部门引进先进脱硫工艺以减少污染。目前脱硫工艺涉及的主要反应有:①H2S(g)+O2(g)===SO2(g)+H2O(g) ΔH1
②S(g)+O2(g)===SO2(g) ΔH2
③S(g)+H2(g)===H2S(g) ΔH3
则“2H2(g)+O2(g)===2H2O(g) ΔH4”中ΔH4的正确表达式为( )
A. ΔH4= (ΔH1+ΔH2-ΔH3) B. ΔH4=2(ΔH1-ΔH2+ΔH3)
C. ΔH4=(ΔH1-ΔH2+ΔH3) D. ΔH4=ΔH1-2(ΔH2-ΔH3)
高二化学选择题简单题查看答案及解析
2015年冬季,雾霾天气严重影响了我国北方地区。国内电力行业和供暖部门引进先进脱硫工艺以减少污染。目前脱硫工艺涉及的主要反应有:①H2S(g)+O2(g)===SO2(g)+H2O(g) ΔH1
②S(g)+O2(g)===SO2(g) ΔH2
③S(g)+H2(g)===H2S(g) ΔH3
则“2H2(g)+O2(g)===2H2O(g) ΔH4”中ΔH4的正确表达式为( )
A. ΔH4= (ΔH1+ΔH2-ΔH3) B. ΔH4=2(ΔH1-ΔH2+ΔH3)
C. ΔH4=(ΔH1-ΔH2+ΔH3) D. ΔH4=ΔH1-2(ΔH2-ΔH3)
高二化学选择题简单题查看答案及解析
【化学——选修3:物质结构与性质】目前半导体生产展开了一场“铜芯片”革命—在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
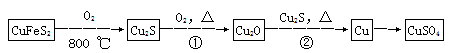
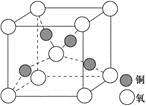
(1)基态铜原子的外围电子排布式为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是___,其立体结构是____。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液蓝色沉淀
沉淀溶解,得到深
蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式______;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
(4)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。((用含d和NA的式子表示)。
高二化学填空题极难题查看答案及解析
【化学——选修3:物质结构与性质】目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
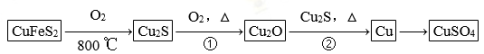
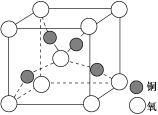
(1)基态铜原子的外围电子排布式为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、②中均生成有相同的气体分子,该分子的中心原子杂化类型是____,其立体结构是______。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液蓝色沉淀
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ___;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
(4) 铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。 (用含d和NA的式子表示)。
高二化学简答题极难题查看答案及解析
“结晶玫瑰”是具有强烈玫瑰香气的结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。其化学名称为“乙酸三氯甲基苯甲酯”,目前国内工业上主要使用以下路径来合成结晶玫瑰:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶政瑰”。
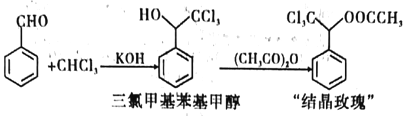
已知:
| 三氯甲基苯基甲醇 | 相对分子质量: 225.5。无色液体。不溶于水,密度比水大,溶于乙醇 |
| 乙酸酐 | 无色液体。与水反应生成乙酸,溶于乙醇 |
| “结晶玫瑰” | 相对分子质量: 267.5。白色晶体。熔点: 88℃。不溶于水,溶于乙醇 |
具体实验步骤如下:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
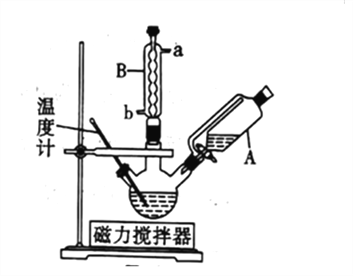
步骤一: 装置如图所示。依次将苯甲醛、氯仿加入三颈烧瓶中,仪器A 中加入KOH和助溶剂。滴加A中试剂并搅拌,开始反应并控制在一定温度下进行。
步骤二: 反应结束后,将混合物依次用5%的盐酸、蒸馏水洗涤。
步骤三: 将洗涤后的混合物蒸馏,除去其他有机杂质,加无水琉酸镁,过滤。滤液即为粗制三氯甲基萃基甲醇。
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶玫瑰”。
步骤四: 向另一三颈瓶中加入制备的三氯甲基苯基甲醇、乙酸酐,并加入少量浓硫酸催化反应,加热控制反应温度在90℃~110℃之间。
步骤五: 反应完毕后,将反应液倒入冰水中,冷却结晶获得“结晶玫瑰”。
请回答下列问题:
(1)仪器A 的名称是_________。实验装置B中,冷凝水应从_____口进(填“a”或“b”)。
(2)步骤二中,用5%的盐酸洗涤的主要目的是___________。在洗涤、分液操作中,应充分振荡,然后静置,待分层后有机层应___________ (填序号)。
A.直接从上口倒出
B.先将水层从上口倒出,再将有机层从下口放出
C.直接从下口放出
D.先将水层从下口放出,再将有机层从下口放出
(3)步骤三中,加入无水硫酸镁的目的是___________。若未加入无水硫酸镁,直接将蒸馏所得物质进行后续反应,会使“结晶玫瑰”的产率偏______(填“高”或“低”),其原因是___________ (利用平衡移动原理解释)。(已知Ⅱ的具体反应如图所示)

(4)步骤四中,加料时,应先加入三氯甲基苯基甲醇和乙酸酐,然后慢慢加入浓硫酸并搅拌,主要是为了__________。加热反应时,为较好的控制温度,最适宜的加热方式为_____(填“水浴加热”或“油浴加热”)。
(5)22.55g三氟甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰21.40g,则产率是_____。
高二化学实验题中等难度题查看答案及解析
(10分)2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为:
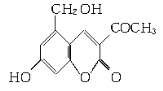
它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
(1)“亮菌甲素”的分子式为________。
(2)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。 写出其属于醇类的同分异构体的结构简式___________________________________________________。
(3)下列有关“亮菌甲素”的叙述正确的是________(填字母)。
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素”分子中含氧官能团只有2种
D.1 mol“亮菌甲素”最多与3 mol NaOH反应
(4)核磁共振氢谱分析,发现二甘醇分子中有3个吸收峰,其峰面积之比为2∶2∶1。又知二甘醇中C、O元素的质量分数相同,且H的质量分数为9.4%,1 mol二甘醇与足量金属钠反应生成1 mol H2。写出二甘醇与乙酸(按物质的量之比1∶1)反应的化学方程式 。
高二化学填空题困难题查看答案及解析
苯乙烯是生产塑料和合成橡胶的重要基本有机原料,乙苯催化脱氢法是目前国内外生产苯乙烯的主要方法,其化学方程式为:
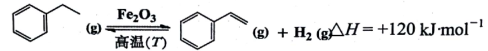
(1)升高反应温度,其转化率________,反应速率________(填“增大”、“减小”或“不变”)。
(2)等温、等压下,通入惰性气体(如水蒸气)能提高反应的转化率,其原因是________。
(3)通入水蒸气可延续催化剂Fe2O3被还原而失活,其原因是________(用化学平衡原理解释)。
(4)一定条件下,在体积不变的密闭容器中,反应过程中各物质浓度随时间变化的关系如下图所示。在t1时刻加入H2,t2时刻再次达到平衡。回答下列问题:
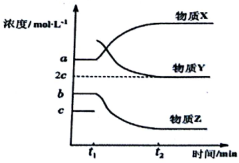
①物质X为__________,判断理由是__________;
②t2时刻,苯乙烯的浓度为______mol•L-1;
③t1-t2时间段内,乙苯的反应速率为_______mol•L-1•min-1;
(5)温度T下,已知H2和苯乙烯的燃烧热△H分别为-290kJ•mol-1和-4400kJ•mol-1,则乙苯的燃烧热为△H_______kJ•mol-1。
高二化学填空题简单题查看答案及解析