-
有一瓶无色澄清溶液,其中可能含有Na+、Mg2+、Ba2+、Cl-、SO42-、CO32-离子.现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入NaOH溶液,使溶液由酸性变成碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生.
(1)根据上述事实确定:该溶液中肯定存在的离子有______;肯定不存在的离子有______;可能存在的离子有______.
(2)写出③中发生反应的离子方程式______.高一化学解答题中等难度题查看答案及解析
-
有一瓶无色澄清溶液,其中可能含有Na+、Mg2+、Ba2+、Cl-、SO
42-、CO32-离子。现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入NaOH溶液
,使溶液由酸性变成碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(1)根据上述事实确定:
该溶液中肯定存在的离子有
;
肯定不存在的离子有 ;
可能存在的离子有
。
(2)写出③中发生反应的离子方程式 。
(3)检验该溶液中所含的阴离子的试剂是 (填名称)。
高一化学填空题困难题查看答案及解析
-
(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl−、SO42−、CO32−离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有_________________________;
肯定不存在的离子有___________________________。
②写出C中发生反应的离子方程式________________________________。
(2)①还原铁粉与高温水蒸气反应的化学方程式:_____________________________;
②除去Mg粉中的Al粉的试剂是__________________,反应的离子方程式为:___________________________________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+_____ _______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;
当有2mol H3PO4生成,转移的电子的物质的量为__________________.
高一化学综合题中等难度题查看答案及解析
-
(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl−、SO42−、CO32−离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有_________________________;
肯定不存在的离子有___________________________。
②写出C中发生反应的离子方程式________________________________。
(2)①还原铁粉与高温水蒸气反应的化学方程式:_____________________________;
②除去Mg粉中的Al粉的试剂是__________________,反应的离子方程式为:___________________________________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+_____ _______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;
当有2mol H3PO4生成,转移的电子的物质的量为__________________.
高一化学综合题中等难度题查看答案及解析
-
有一瓶无色澄清溶液,其中可能含有H+、Na+、Mg2+、Ba2+、Cl-、SO42-、CO32-离子。现进行以下实验:
A.用pH试纸检验溶液,发现溶液呈强酸性;
B.取部分溶液逐滴加入NaOH 溶液,使溶液由酸性变为碱性,无沉淀产生;
C.取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(1)根据上述事实确定:该溶液中肯定存在的离子有__________;肯定不存在的离子有__________。
(2)写出C 中发生反应的离子方程式____________________________________。
高一化学推断题中等难度题查看答案及解析
-
(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl−、SO42−、CO32−离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有_________________________;
肯定不存在的离子有___________________________。
②写出C中发生反应的离子方程式________________________________。
(2)①还原铁粉与高温水蒸气反应的化学方程式:_____________________________;
②除去Mg粉中的Al粉的试剂是__________________,反应的离子方程式为:___________________________________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+_____ _______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;
当有2mol H3PO4生成,转移的电子的物质的量为__________________.
高一化学综合题中等难度题查看答案及解析
-
(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl−、SO42−、CO32−离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有_________________________;
肯定不存在的离子有___________________________。
②写出C中发生反应的离子方程式________________________________。
(2)①还原铁粉与高温水蒸气反应的化学方程式:_____________________________;
②除去Mg粉中的Al粉的试剂是__________________,反应的离子方程式为:___________________________________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+_____ _______
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;
当有2mol H3PO4生成,转移的电子的物质的量为__________________.
高一化学综合题中等难度题查看答案及解析
-
(1)有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、NH4+、Ba2+、Cl−、SO42-、CO32-离子。现进行以下实验:
A.用pH试纸检验溶液,发现溶液呈强酸性;
B.取部分溶液逐滴加入浓NaOH溶液,使溶液由酸性变为碱性,无沉淀产生,产生了能使湿润的红色石蕊试纸变蓝的气体;
C.取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有__;肯定不存在的离子有__。
②写出B中发生反应的离子方程式__。
(2)某化学学习小组模拟侯德榜制碱法制取Na2CO3的过程如下:
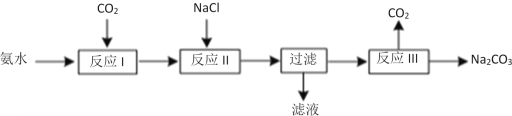
已知:a.反应Ⅰ的化学方程式为:NH3+H2O+CO2=NH4HCO3
b.滤液含NH4Cl等溶质
①反应Ⅱ为复分解反应,写出该反应的化学方程式___。
②验证滤液中含Cl-离子的实验方法和现象为___。
高一化学推断题中等难度题查看答案及解析
-
有一瓶无色澄清溶液,其中仅可能含有H+、Na+、Mg2+、Ba2+、Cl—、SO42—、CO32—离子。现进行如下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入稀NaOH溶液,使溶液从酸性变为碱性,无沉淀生成;
③取少量②中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
根据上述实验事实确定:该溶液中肯定存在的离子有 ,肯定不存在的离子有 ;可能存在的离子有
高一化学填空题中等难度题查看答案及解析
-
在一瓶无色澄清的溶液中,可能含有Cl-、Cu2+、SO42-、CO32-、Na+、Mg2+、Ba2+这七种离子中的某几种,对此进行实验:①向少量该溶液中加入NaOH溶液,产生白色沉淀;②取少量原溶液,加入BaCl2溶液产生白色沉淀.
(1)该溶液中一定含有的离子是______;一定不含有的离子是______.
(2)为检验可能存在的阴离子,需要进行的实验是______.高一化学解答题中等难度题查看答案及解析