-
海水的综合利用可以制备金属钠和镁,请根据下列工艺生产流程回答问题。
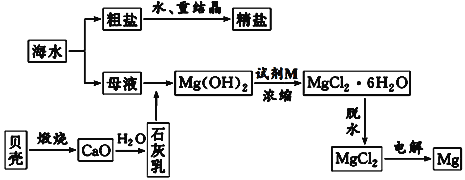
(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___。
(2)母液中加入石灰乳反应的离子方程式为__。
(3)若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,而MgO的熔沸点非常高,达到熔融状态需要消耗很多能源。所以,用电解法制取金属镁时,需要无水氯化镁。写出用电解法制取金属镁的化学方程式___。
(4)在以上提取镁的过程中,没有涉及的化学反应类型是__。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
-
海水的综合利用可以制备金属镁,其流程如图所示:

(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___________________________________________。
(2)母液中加入石灰乳反应的离子方程式为______。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:_____________________________,
过滤时:_____________________________,
蒸发时:_____________________________。
(4)除去粗盐溶液中含有的 、
、 、
、 ,可依次加入
,可依次加入 溶液、NaOH溶液、________,最后加入_________调节pH至中性。
溶液、NaOH溶液、________,最后加入_________调节pH至中性。
(5)写出金属镁在空气中燃烧的化学方程式____________________________。
-
海水的综合利用可以制备金属镁,其流程如下图所示:

(1)完成下列方程式:
煅烧贝壳(化学方程式): ;
Mg(OH)2加盐酸(离子方程式):
(2)电解熔融MgCl2的反应化学方程式是 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
溶解时: 。
过滤时: 。
蒸发时: 。
(4)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl和HCl,写出相应反应的化学方程式: 。
-
(2015秋•烟台期末)海水中有非常丰富的化学资源,从海水中可提取多种化工原料.某工厂对海水资源综合开发利用的部分工艺流程图如下.回答下列问题:
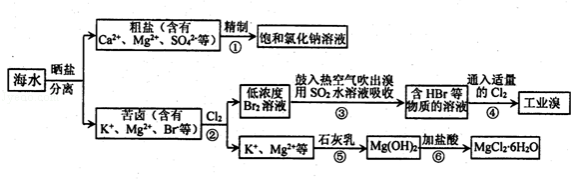
(1)化学实验中常用到与海水晒盐原理相同的操作名称是 ,必需的仪器有铁架台(含铁圈)、 、 、 .
(2)精制食盐水时下列物质中,不必用到的有 .
①NaOH溶液②盐酸③K2CO3溶液④BaCl2溶液⑤硫酸⑥Na2CO3溶液⑦Ba(NO3)2溶液
(3)下列说法错误的是
A.海水中的镁、溴、碘元素都处于化合态
B.步骤②④中通入Cl2能制得单质溴,因为Cl2的氧化性比Br2强
C.步骤③中鼓入热空气分离出Br2,利用了Br2的挥发性
D.步骤⑤发生反应的离子方程式为:Mg2++2OH﹣═Mg(OH)2↓
(4)步骤②中已获得Br2,步骤③中又将Br2还原为Br,其目的为 .
(5)步骤③反应的离子方程式为 ;该步骤也可以采用纯碱吸收,反应方程式:3Br2 + 6Na2CO3 + 3H2O ═ 5NaBr + NaBrO3 + 6NaHCO3,当转移3.01×1023个电子时,吸收Br2的物质的量为 .
(6)若步骤⑤所得Mg(OH)2沉淀中混有Ca(OH)2杂质,写出除去杂质的实验步骤 .
-
在海水综合利用中,下列叙述不正确的是( )
A.海水经过蒸发结晶得到粗盐
B.海水中提取镁单质的方法是海水 Mg(OH)2
Mg(OH)2 Mg
Mg
C.海水提镁的工艺中用贝壳为原料生产石灰乳
D.海水中提取溴单质可以用氯气将海水中的Br-氧化
-
在海水综合利用中,下列叙述不正确的是( )
A.海水经过蒸发结晶得到粗盐
B.海水中提取溴单质可以用氯气将海水中的Br-氧化
C.海水提镁的工艺中用贝壳为原料生产石灰乳
D.海水中提取镁单质的方法是海水 Mg(OH)2
Mg(OH)2 Mg
Mg
-
综合利用海水制备金属镁的流程如图所示,请据图回答下列问题:
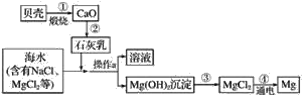
(1)贝壳主要成分的化学式是__。
(2)第②步是用生石灰和水反应制取石灰乳(主要成分是氢氧化钙)请写出制取石灰乳的化学方程式:__,基本反应类型是__。
(3)第③步是将沉淀出的氢氧化镁与盐酸反应生成氯化镁,写出该反应的化学方程式:__,该反应基本类型是__。
(4)第④步是无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式:___,反应基本类型是__。
(5)要使海水中MgCl2完全转化为沉淀Mg(OH)2,加入石灰乳的量应过量,确定海水中的MgCl2已全部转化为Mg(OH)2的方法:取上层清液少量,向其中加入氢氧化钠溶液,观察到__。
(6)海水中本来就有氯化镁,请分析从海水中制取MgCl2时,要经历“MgCl2→Mg(OH)2→MgCl2”的转化原因:__。
-
从海水制备金属镁的流程如图所示:

(1)为了节约成本,充分利用海滩资源,用贝壳经过一系列反应可以制得石灰乳,请写出有关反应的化学方程式:__________;__________。
(2)向石灰乳中加入MgCl 溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
(3)从熔点与硬度方面来看,镁合金与镁相比较,其特点有__________。
-
从海水制备金属镁的流程如图所示:

(1)为了节约成本,充分利用海滩资源,用贝壳经过一系列反应可以制得石灰乳,请写出有关反应的化学方程式:__________;__________。
(2)向石灰乳中加入MgCl2溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
(3)从熔点与硬度方面来看,镁合金与镁相比较,其特点有__________。
-
海水的综合利用可以制备金属镁,其流程如图所示:

(1)写出下列反应的化学方程式。
①石灰乳与母液反应___;
②Mg(OH)2中加入盐酸的离子方程式:__;
③MgCl2 Mg:___。
Mg:___。
(2)在海水提取镁的过程中,没有涉及的化学反应类型__
A.分解反应 B.化合反应 C.复分解反应 D.置换反应 E.氧化还原反应







