-
短周期主族元素X、Y、Z、W的原子序数依次增大。X与W同主族,X、W的单质在标准状况下的状态不同。Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构。下列说法正确的是( )
A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.化合物X2Z2与W2Z2所含化学键类型完全相同
高二化学单选题中等难度题查看答案及解析
-
原子序数依次增大的X、Y、Z、M、W五种短周期元素,其中X是周期表中原子半径最小的元素,Y、Z同周期,X、M同主族;X、Y、W的最外层电子数之和为12;Z的单质为空气中含量最高的成分,W的最高价和最低价代数和为6.下列说法中正确的是( )
A. 根据价层电子对互斥理论知化合物ZX3的空间构型为三角锥形
B. Y的电负性比Z的电负性强
C. W的氧化物对应的水化物一定是强酸
D. 原子半径:W>M>Z>Y
高二化学选择题简单题查看答案及解析
-
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13;B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素.试回答以下问题:
(1)写出D与E以1:1的原子个数比形成的化合物的电子式_________________;F的原子结构示意图为_________________;(2)B、D形成的化合物BD2中存在的化学键为__________键(填“离子”或“共价”,下同).A、C、F三种元素形成的化合物CA4F为_______化合物;
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性.则甲、乙反应的离子方程式为_________________;
(4)A、C、D、E的原子半径由大到小的顺序是_________________(用元素符号表示);
(5)元素B和F的非金属性强弱,B的非金属性____________于F(填“强”或“弱”),并用化学方程式证明上述结论_________________;
高二化学填空题困难题查看答案及解析
-
A、B、C、D、E、F为原子序数依次增大的前四周期元素,A元素原子最外层电子数是其内层电子数的2.5倍,B元素是地壳中含量最高的元素,C元素的最高化合价和最低化合价的代数和等于0,D元素的单质可用于自来水消毒杀菌,E元素位于周期表的ⅥB族,F的基态原子中有4个未成对电子。
(1)A元素单质的结构式为___________;B元素原子中的未成对电子数为_______________________。
(2)在A的氢化物A2H4分子中,A原子轨道的杂化类型是______;A与B形成的AB2-的空间构型为___________________________。
(3)A、B、C三种元素的第一电离能从大到小的顺序为_______________(用元素符号表示)。
(4)基态F3+的核外电子排布式是_____________________;F3+与SCN-络合得到多种配合物,其中配位数为5的配合物的化学式为__________________;化合物FD3是棕色固体、易潮解,100℃左右时升华,FD3的晶体类型是__________________________。
(5)铁在不同温度范围有不同的晶体结构。室温下铁是简单立方,称为α铁(α-Fe)。当温度升高到912℃,α铁转变为面心立方,称为γ铁(γ-Fe)。当温度继续升高到1394 ℃,γ铁转变为体心立方。称为δ铁(δ-Fe)。
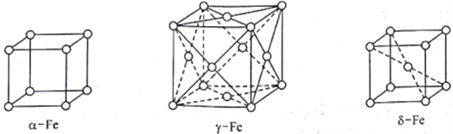
①γ铁晶体中铁原子配位数是____________________。
②δ铁晶体密度为dg·cm-3,则其晶胞参数(边长)为__________cm(阿伏加德罗常数用NA表示)。
高二化学综合题中等难度题查看答案及解析
-
A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为______,D在元素周期表中的位置______。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为________;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程__________________。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为________________。
(4)E元素的非金属性强于D元素,用原子结构解释原因:同周期元素随着原子序数的递增,______________________________,非金属性增强。
(5)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为__________________。
高二化学填空题中等难度题查看答案及解析
-
X、Y、Z、W是原子序数依次增大的周期表前20号元素中的四种元素,且分别位于第二、三、四周期。X与Z位于同一主族,Y是地壳中含量最高的金属元素,Z的单质可用于制造半导体芯片,W的原子序数等于X和Y原子序数之和。下列说法正确的是
A.原子半径:r(W)>r(Y)>r(Z)>r(X)
B.简单气态氢化物的热稳定性:Z>X
C.最高价氧化物对应水化物的碱性:Y>W
D.工业上可以用电解W的氯化物的水溶液的方法来制取W的单质
高二化学单选题中等难度题查看答案及解析
-
A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A 的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E 的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为___________。
(2)A 的某种氢化物A2H2分子中含有________个σ键和_____个π键。
(3)B 的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_______。
(4) E 的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是_______。
高二化学综合题中等难度题查看答案及解析
-
已知短周期元素甲、乙、丙、丁的原子序数依次增大,甲是地壳含量最多元素,乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应,丁的P轨道有两个未成对电子。下列说法错误的是
A. 元素丙的单质可用于冶炼金属 B. 甲与丁形成的分子中有非极性分子
C. 简单离子半径:丁>乙>丙 D. 甲与乙形成的化合物均有强氧化性
高二化学单选题简单题查看答案及解析
-
R、Q、X、Y、Z是原子序数依次增大的五种短周期元素,R与Q形成的气态化合物,在标准下的密度为0.76 g/L,X、Y、Z三种元素族序数之和为10,Y是地壳中含量最多的金属元素,Y单质能强碱溶液反应,Z元素原子最外层电子数是电子层数的两倍。
(1)X在周期表中的位置______________;X、Y、Z三种元素形成的简单离子半径由大到小的顺序是_____________________。(用离子符号回答)
(2)X和R两种元素按原子个数比1:1组成的化合物的电子式为___________,推测这种化合物具有较强的_________________。(填“氧化性”或“还原性”)
(3)写出Y、Z两种元素最高价氧化物对应的水化物相反应的离子方程式:____________。
(4)水的沸点远高于Z元素的氢化物的沸点,原因是_______________________________。
(5)Q4是一种Q元素的新单质,可用作推进剂或炸药,推算其分子中含有________________________对共用电子。
(6)由R、Q两元素组成的一种液态化合物W常用作还原剂,W分子中含有18个电子,W分子的结构式为____________________。W与氢氧化铜悬浊液反应生成氧化亚铜,同时产生一种稳定的气态单质,该反应的化学方程式为____________________________。
高二化学填空题中等难度题查看答案及解析
-
已知短周期的主族元素X、Y、Z、W、M的原子序数依次增大,X是空气中含量最
多的元素,其单质的化学性质非常稳定,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W元素形成的单质为淡黄色的固体,M元素形成的单质为黄绿色气体.请回答以下问题:
(1)X元素的符号是 ,它在周期表的位置为 ;
(2)Z的氧化物晶体类型为 ,化学式是: ;
(3)X与Y能形成离子化合物,该化合物的电子式为 ;
(4)X的最高价氧化物的水化物与Y的氧化物反应的化学方程式为 ;
(5)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为 ;
(6)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱(用方程式书写或文字说明) 。
高二化学填空题中等难度题查看答案及解析