氢能将成为21世纪的主要能源。太阳能光伏电池电解水可制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

(1)制H2时,连接________(填“K1”或“K2”),产生H2的电极反应式是____________,溶液pH___________(填“增大”、“减小”或“不变”)。
(2)改变开关连接方式,可得O2,此时电极3的反应式为:__________________。
高二化学填空题简单题
氢能将成为21世纪的主要能源。太阳能光伏电池电解水可制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

(1)制H2时,连接________(填“K1”或“K2”),产生H2的电极反应式是____________,溶液pH___________(填“增大”、“减小”或“不变”)。
(2)改变开关连接方式,可得O2,此时电极3的反应式为:__________________。
高二化学填空题简单题
氢能将成为21世纪的主要能源。太阳能光伏电池电解水可制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

(1)制H2时,连接________(填“K1”或“K2”),产生H2的电极反应式是____________,溶液pH___________(填“增大”、“减小”或“不变”)。
(2)改变开关连接方式,可得O2,此时电极3的反应式为:__________________。
高二化学填空题简单题查看答案及解析
氢能源是最具应用前景的能源之一,高纯氢的制备时目前的研究热点。某工艺利用电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2.下列有关描述不合理的是

A.制H2时,产生H2的电极反应式:2H2O+2e-=H2↑+2OH-
B.制O2时,电极3要连接K2
C.若没有电极3,K1和K2直接相连,一样可以得到H2和O2
D.上述过程,若用酸性电解质一样可以实现上述过程
高二化学单选题中等难度题查看答案及解析
图中装置通过控制开关连接K1或K2,可利用太阳能电池电解水制高纯氢。下列说法错误的是( )
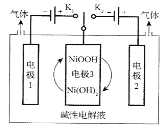
A.制H2时,连接K1
B.制O2时,电极3的反应式:NiOOH+H2O+e-=Ni(OH)2+OH-
C.交替连接K1和K2,可使电极3得以循环使用
D.上述过程,若用酸性电解质一样可以实现上述过程
高二化学单选题中等难度题查看答案及解析
建设资源节约型、环境友好型社会是政府的工作目标,以下措施中不能体现这一思想
的是
A.在电解铝工业中添加冰晶石
B.开发太阳能、风能、氢能等清洁能源
C.收集废弃的秸杆等生产沼气
D.为防止电池中的重金属污染土壤,将废旧电池深埋地下
高二化学选择题简单题查看答案及解析
下列关于能源的说法或做法不合理的是
A. 氢能属于绿色能源,可利用电解水的方法获取廉价的氢能
B. 乙醇属于可再生能源,可用作燃料
C. 提高燃料利用率已成为国际能源研究的热点课题
D. 应开发太阳能、风能、生物质能等新的能源
高二化学单选题中等难度题查看答案及解析
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是____(任答一点)。
(2)在101 kPa下,1 g氢气完全燃烧生成气态水放出120.9 kJ的热量,请回答下列问题:
①该反应的反应物总能量______生成物总能量。(填“>、=、<”)
②该反应的热化学方程式为______。
③已知H-O键能为463.4 kJ/mol,O=O键能为498kJ/mol,计算H-H键能为___kJ/mol。
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ/mol;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ/mol;Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)ΔH3,则ΔH3=_____ kJ/mol。
高二化学填空题中等难度题查看答案及解析
下列叙述正确的是 ( )
A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C.废电池需回收,主要是要利用电池外壳的金属材料
D.升高温度可降低活化能
高二化学选择题简单题查看答案及解析
下列叙述正确的是
A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C.废电池需回收,主要是要利用电池外壳的金属材料
D.升高温度可降低活化能
高二化学选择题简单题查看答案及解析
下列叙述正确的是
A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C.废电池需回收,主要是要利用电池外壳的金属材料
D.升高温度可降低活化能
高二化学选择题中等难度题查看答案及解析
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是________________(任答一点)
(2)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为______________
③该反应的热化学方程式为__________________________________________________
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________kJ·mol-1
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________kJ·mol-1
高二化学简答题困难题查看答案及解析