-
元素及其化合物在生活及生产中有很多重要用途。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)基态碳原子价电子的电子轨道表达式为____,第一电离能Ga____As(填“>”、 “<”、“=”)。
(2)BN和GaAs都是原子晶体,它们的硬度和熔点BN>GaAs,原因是________________。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。 (CN)2分子中氮原子的轨道杂化类型为_____,σ 键与 π 键数目之比为_______; (SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H—N=C=S),其原因是_________。
(4)①卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为_____________;②一定条件下(SCN)2可氧化为CO32—和SO32—等离子,其中SO32—的立体构型为_________。
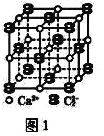
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图1 所示),CaC2 晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。写出与C22﹣互为等电子体的微粒符号________、_______;此晶体中 1 个 C22﹣周围距离最近的Ca2+为______个;若该晶胞的边长为a、a、b(nm),则该晶体的密度为______ g·cm-3(写出表达式)。

高三化学简答题中等难度题查看答案及解析
-
SiC、GaN、GaP、GaAs等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射的应用性能而成为半导体领域研究热点。试回答下列问题:
(1)碳的基态原子L层电子轨道表达式为__,砷属于__区元素。
(2)N与氢元素可形成一种原子个数比为1:1的粒子,其式量为60,经测定该粒子中有一正四面体构型,判断该粒子中存在的化学键__。
A.配位键 B.极性共价键 C.非极性共价键 D.氢键
(3)CaC2晶体的晶胞结构与NaCl晶体的相似(如图1所示),但CaC2晶体中含有的哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为__。
高三化学填空题中等难度题查看答案及解析
-
(10分)请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有 种。
(2)第ⅢA、ⅤA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为 。在GaN晶体中,每个Ga原子与 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为 。在四大晶体类型中,GaN属于 晶体。
(3)在极性分子NCl3中,N原子的化合价为-3,Cl原子的化合价为+1,请推测
NCl3水解的主要产物是 (填化学式)。
高三化学选择题简单题查看答案及解析
-
(12分) “物质结构与性质”
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于 晶体。
(2)铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有的原子或离子
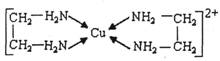
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
① H、N、O三种元素的电负性由大到小的顺序是。
②SO2分子的空间构型为。与SnCl4互为等电子体的一种离子的化学式为。
③乙二胺分子中氮原子轨道的杂化类型为。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是。
④⑶中所形成的配离子中含有的化学键类型有。
a.配位键 b.极性键 c.离子键 d.非极性键
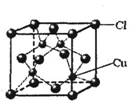
⑤CuCl的晶胞结构如右图所示,其中Cl原子的配位数为。
高三化学填空题中等难度题查看答案及解析
-
[化学--物质结构与性质]
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似.Ga原子的电子排布式为______.在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为______.在四大晶体类型中,GaN属于______晶体.
(2)NH3分子的空间构型是:______,中心原子N的杂化轨道类型是:______.
(3)NH3与PH3相比,热稳定性更强的是:______,理由是:______.
(4)一定压强,将NH3和PH3混合气体降温时,首先液化的物质是______,理由是:______.
(5)铜、铁元素能形成多种配合物.微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有______的原子或离子.高三化学解答题中等难度题查看答案及解析
-
Ⅰ.第ⅢA、VA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型第三代半导体材料,其晶体结构与单晶硅相似。试回答:
(1)Ga的基态原子的价电子的轨道排布式为________。
(2)下列说法正确的是(选填序号)。
A.砷和镓都属于p区元素 B.GaN、GaP、GaAs均为分子晶体
C.电负性:As>Ga D.第一电离能Ga>As
(3)GaAs是由(CH3)3Ga和AsH3在一定条件下制得,同时得到另一物质,该物质分子是________(填“极性分子”或“非极性分子”)。(CH3)3Ga中镓原子的杂化方式为________。
Ⅱ.氧化钙晶体的晶胞如图所示,试回答:
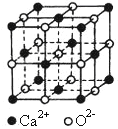
(1)晶体中Ca2+的配位数为________。
(2)已知Ca2+的半径为a cm,O2-的半径为b cm,NA代表阿伏加德罗常数,
该晶体的密度为________g/cm3。(用含a、b、NA的代数式表示)
高三化学填空题中等难度题查看答案及解析
-
(12分)⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为▲ 。在四大晶体类型中,GaN属于▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有▲ 的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:

① H、N、O三种元素的电负性由大到小的顺序是▲ 。
②SO2分子的空间构型为▲ 。与SnCl4互为等电子体的一种离子的化学式为▲
③乙二胺分子中氮原子轨道的杂化类型为▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是▲ 。
④⑶中所形成的配离子中含有的化学键类型有▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
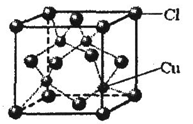
⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为▲ 。
高三化学填空题简单题查看答案及解析
-
⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为▲ 。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为▲ 。在四大晶体类型中,GaN属于▲ 晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有▲ 的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题:
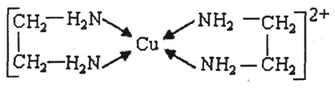
① H、N、O三种元素的电负性由大到小的顺序是▲ 。
②SO2分子的空间构型为▲ 。与SnCl4互为等电子体的一种离子的化学式为▲
③乙二胺分子中氮原子轨道的杂化类型为▲ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是▲ 。
④⑶中所形成的配离子中含有的化学键类型有▲ 。
a.配位键 b.极性键 c.离子键 d.非极性键
⑤CuCl的晶胞结构如右图所示,其中Cl原子的配位数为▲ 。

高三化学填空题中等难度题查看答案及解析
-
ⅢA、VA族元素组成的化合物AlN、AlP、GaAs等是人工合成的新型半导体材料。回答下列问题:
(1)As基态原子的电子占据了___________个能层,最高能级的电子排布式为___________;和As位于同一周期,且未成对电子数也相同的元素还有_____________种。
(2)元素周期表中,与P紧邻的4种元素中电负性最大的是__________(填元素符号);Si、P、S三种元素的第一电离能由大到小的顺序是______________。
(3)已知AlN、AlP等半导体材料的晶体结构与单晶硅相似,则Al原子的杂化形式为________;晶体结构中存在的化学键有____________(填标号)。
A.离子键 B.
键 C.
键 D.配位键
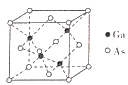
(4)砷化镓(GaAs)是继硅晶体之后研究最深入、应用最广泛的半导体材料,它能直接将电能转变为光能,以其为材料制造的灯泡寿命长、耗能少。已知CaAs的晶胞结构如图,晶胞参数
=0.565nm,则Ga原子与As原子的核间距为____________pm(列式表示)。
高三化学综合题中等难度题查看答案及解析
-
GaN、GaP、GaAs是人工合成的一系列新型半导体材料,其晶体结构均与金刚石相似。铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。回答下列问题:

(1)基态Ga原子价电子的轨道表达式为________________;
(2)熔点:GaN_____GaP(填“>”或“<”);
(3)第一电离能:As_____Se(填“>”或“<”);
(4)Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是______;
a.配位键 b.极性键 c.离子键 d.非极性键
(5)乙二胺分子中氮原子轨道的杂化类型为________,乙二胺和三甲胺[N(CH3)3]均属于胺。但乙二胺比三甲胺的沸点高很多,原因是___________;
(6)Cu的某种晶体晶胞为面心立方结构,晶胞边长为acm,铜原子的半径为rcm。该晶体中铜原子的堆积方式为_______型(填“A1”、“A2”或“A3”),该晶体密度为____g/cm3(用含a和NA的代数式表达),该晶体中铜原子的空间利用率为______(用含a和r的代数式表达)。
高三化学简答题困难题查看答案及解析