-
如图为向25mL 0.1mol·L−1NaOH溶液中逐滴滴加0.2mol·L−1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
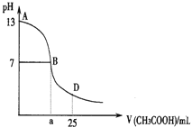
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?(选填“是”或“否”)_________.若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?__________________(若正确,此问不答)
(2)AB区间,c(OH−)>c(H+),则c(OH−)与c(CH3COO−)大小关系是_______________
A.c(OH−)一定大于c(CH3COO−) B.c(OH−)一定小于c(CH3COO−)
C.c(OH−)一定等于c(CH3COO−) D.c(OH−)大于、小于或等于c(CH3COO−)
(3)在D点时,溶液中c(CH3COO−)+c(CH3COOH)_________2c(Na+)(“>”、“<”或“=”)
(4)常温下,将VmL、0.1000mol·L−1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L−1醋酸溶液中,充分反应。回答下列问题.(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值____________20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO−)、c(H+)、c(OH−)的大小关系为________________________.
②如果V=40.00,则此时溶液中c(OH−)−c(H+)−c(CH3COOH)=__________________mol·L−1
-
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法不正确的是
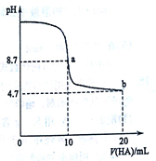
A.在逐滴加入HA溶液至20mL时,NaOH溶液中水的电离程度先增大后减小
B.b点所示溶液中c(A-)>c(HA)
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.该酸是弱酸
-
室温下,在25 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1CH3COOH溶液,pH与滴加CH3COOH溶液体积的关系曲线如下图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
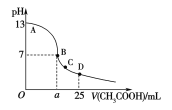
A. 在A、B间任一点,溶液中一定都c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
B. 在B点:a>12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
C. 在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. 在D点:c(CH3COO-)+c(CH3COOH)=0.1mol·L-1
-
室温下,在25 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1CH3COOH溶液,pH与滴加CH3COOH溶液体积的关系曲线如下图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
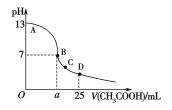
A.在A、B间任一点,溶液中一定都c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
B.在B点:a>12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
C.在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=0.1mol·L-1
-
室温下,向20 mL N mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示。下列说法中,正确的是
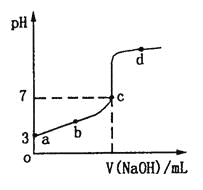
A.a点c(CH3COOH)=10-3mol·L-1
B.b点溶液中离子浓度大小满足关系: c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c点溶液中离子浓度大小满足关系: c(Na+)+c(OH-)=c(H+)+c(CH3COO-)
D.滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
-
常温下,用0.1000mol·L1NaOH溶液滴定20.00mL0.1000mol · L1CH3COOH溶液,滴定过程中溶液pH随NaOH溶液体积的变化见下图。则以下说法正确的是
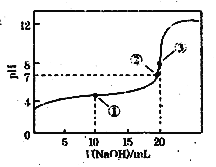
A. 点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO―)
B. 点①所示溶液中:c(CH3COO―)+c(OH―)=c(CH3COOH)+c(H+)
C. 点③所示溶液中:c(Na+)>c(OH―)>c(CH3COO―)>c(H+)
D. 滴定过程中不可能出现:c(CH3COOH)>c(CH3COO―)>c(H+)>c(Na+)>c(OH―)
-
(一)室温下,在25 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,曲线如下图所示,回答下列问题:
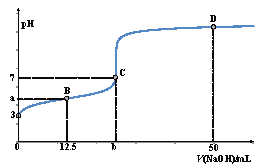
(1)写出CH3COOH的电离方程式__________________________。
(2)下列说法不正确的是___________________。
A. 0.1 mol/L CH3COOH溶液中, CH3COOH电离度约为1%
B. B点满足: c(CH3COO-)-c(CH3COOH)=2c(OH-)-2c(H+)
C. C点时的离子浓度关系为:c(CH3COO-)= c(Na+)> c(H+)= c(OH-)
D. D点时的离子浓度关系为: c(Na+)> c(CH3COO-)> c(OH-)> c(H+)
(3)室温下,试计算CH3COOH电离平衡常数为____________(用含b的表达式表示)。
(二)实验室为测定食醋中CH3COOH的浓度,取25mL食醋置于250mL容量瓶中,加水稀释至刻度并摇匀。用酸式滴定管量取25.00mL稀释后的醋酸溶液放入锥形瓶中,加指示剂,然后用0.1000 mol·L-1NaOH标准溶液进行滴定。
(4)指示剂应为________。
A.甲基橙 B.甲基红 C.酚酞 D.石蕊
(5)滴定终点的判断方法为____________________________________________________。
(6)为提高测定的准确度,重复上述实验三次,0.1000 mol·L-1NaOH标准溶液滴定前后的读数如下表所示,则该食醋中CH3COOH的浓度为_________mol·L-1。
| 实验次数 | 稀释后的醋酸溶液体积/ mL | NaOH滴定前读数/ mL | NaOH滴定后读数/ mL |
| 第1次 | 25.00 | 0.10 | 24.00 |
| 第2次 | 25.00 | 0.50 | 22.50 |
| 第3次 | 25.00 | 0.20 | 24.30 |
(7)用0.1000 mol·L-1NaOH标准溶液进行滴定,下列操作会导致测定结果偏高的是_______。
A.碱式滴定管内滴定后产生气泡
B.读取标准液读数时,滴定前俯视,滴定到终点后仰视
C.配制0.1000 mol·L-1NaOH溶液时,固体NaOH中含有结晶水
D.碱式滴定管未润洗就装入标准液进行滴定
-
室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)
-
室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是
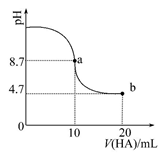
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相 同
同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
-
室温下向10 mL 0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
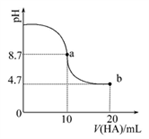
A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. b点所示溶液中c(A-)>c(HA)









