利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
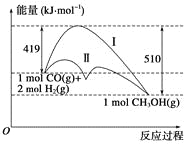
A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
高一化学单选题中等难度题
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )

A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
高一化学单选题中等难度题
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g) 反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
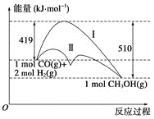
A.生成1mol CH3OH(g)时,该反应吸收的热量为91 kJ。
B.加入催化剂可以减少反应最终放出的热量
C.1mol CO(g)与2molH2(g)的总能量大于1mol CH3OH(g)的总能量
D.如果该反应生成CH3OH (l),则放出的能量会减少
高一化学单选题简单题查看答案及解析
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
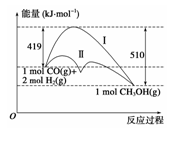
A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH减小
高一化学选择题中等难度题查看答案及解析
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
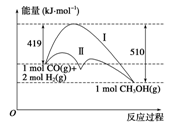
A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH减小
高一化学选择题中等难度题查看答案及解析
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )

A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
高一化学单选题中等难度题查看答案及解析
利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知:CO(g) + 2H2(g)CH3OH(g)是合成甲醇(CH3OH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )

A. CO(g)与H2(g)反应生成1mol CH3OH(g)释放出91kJ的能量
B. 用碳制备原料气CO、H2的反应属于放热反应
C. 反应物总键能高于生成物的总键能
D. 若该反应生成液态CH3OH,则放出的能量更少
高一化学单选题简单题查看答案及解析
利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知:CO(g) + 2H2(g)CH3OH(g)过程能量情况如下图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )

A.加入催化剂,该反应的ΔH变小 B.该反应的ΔH=+91kJ·mol-1
C.反应物的总能量大于生成物的总能量 D.如果该反应生成液态CH3OH,则ΔH增大
高一化学选择题简单题查看答案及解析
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景。在催化剂作用下可用H2和CO合成甲醇,反应的化学方程式为 2H2(g)+CO(g)CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图所示。
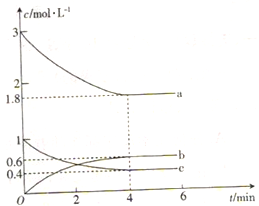
回答下列问题:
(1)代表H2浓度变化的曲线为_______(填“a”、“b”或“c”)。
(2)提出一条可以加快反应速率的措施:______________________________。
(3)0〜4 min内,CH3OH的平均反应速率为_________________。
(4)我国某高校化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
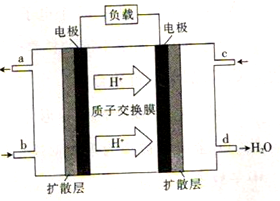
①该电池工作时,c口通入的物质为_____________,该电极为____(填“正极”或“负极”)。
②该电池工作一段时间后,,当6.4 g甲醇完全反应生成CO2时,消耗的氧气的体积为_____L(标准状况下)。
高一化学填空题中等难度题查看答案及解析
开发、使用清洁能源发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)CH3OH(g) △H= -90.8kJ•mol-1。
①某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____,以CH3OH表示该过程的反应速率v(CH3OH)=______。
②要提高反应2H2(g)+CO(g)⇌CH3OH(g)中CO的转化率,可以采取的措施是_______。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2 e.加入惰性气体 f.分离出甲醇
(2)①氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是____________。
②科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为__________。
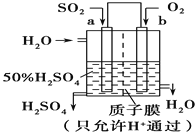
高一化学综合题中等难度题查看答案及解析
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)CH3OH(g),反应过程中的能量变化情况如图所示。

(1)曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。该反应是________(填“吸热”或“放热”)反应。计算当反应生成1.5 mol CH3OH(g)时,能量变化是________kJ。
(2)选择适宜的催化剂________(填“能”或“不能”)改变该反应的反应热。
(3)推测反应CH3OH(g)CO(g)+2H2(g)是________(填“吸热”或“放热”)反应。
高一化学综合题中等难度题查看答案及解析
乙醇(C2H5OH)是生活中常见燃料,可以通过:
方法一,植物中淀粉类或者糖类物随采用发酵方式生产;
方法二,石油化学工业使用乙烯为原料合成。回答下列问题
(1)生物质能是人类解决能源危机的重要途径之· ,下列有关生物质能的说法正确的是______
A.利用生物质能就是间接利用太阳能
B.生物质能是可再生能源
C.生物质能的缺点是严重污染环境
D.生物质能是解决农村问题的重要途径
(2)乙醇可以直接用作燃料,也可以设计乙醇一空气燃料电池,以氢氧化钾溶液做电解质,写出负极的电极反应__________;若以熔融的碳酸盐做电解质,写出负极的电极反应式______;
(3)已知乙醇的燃烧热为1366.8kJ/mol,根据下列反应的反应热:
C(s)+O2(g)═2CO2(g) △H=-393.5kJ·mol-1
H2(g)+1/2O2(g)=H2O(1) △H=-285.8 kJ/mol
则理论上以C(s)、H2(g)、O2(g)为原料合成C2H5OH(1)的反应的热化学方程式为_________。
高一化学选择题困难题查看答案及解析