-
央视报道《王者归“铼”》:中国发现超级金属“铼”,飞机火箭上天全靠它,有望打破美国垄断。
(1)铼(Re)被称为类锰元素,与锰的外围电子结构数相同,已知Mn的外围电子排布式为3d54s2,写出75Re的外围电子排布式:______,其最高价氧化物的化学式为_______。
(2)铢合金可作为醇脱氢反应的催化剂:CH3OH HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______和_______。C、H、O三种元素中,电负性最大的是______(填元素符号)。
HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______和_______。C、H、O三种元素中,电负性最大的是______(填元素符号)。
(3)实验中常用过硫酸盐氧化法测定钢铁中锰的含量,反应原理为2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。
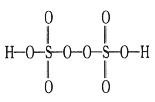
上述反应中S2O82-断裂的共价键类型为___(填“σ键”或“π键”),每生成0.3molMnO4-,过硫酸根中断裂的共价键数目为_____NA。
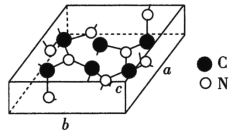
(4)科学家研制出一种新型的超硬材料,类似于金刚石的结构,但硬度比金刚石大,该晶体元素组成为C和N,其晶胞如图所示(图示原子都包含在晶胞内),则该晶胞所含氮原子的个数为____。已知晶胞参数分别为a nm、b nm、c nm,,该晶体的摩尔质量为Mg·mol-1,密度为ρg·cm-3,则阿伏加德罗常数的数值为___(用含a、b、c、ρ、M的代数式表示)。
-
CCTV 在“新闻30分”中介绍:王者归“铼”,我国发现超级铼矿,飞机上天全靠它。铼的稳定硫化物有ReS2,稳定的氧化物有 Re2O7。工业上,常从冶炼铜的废液中提取铼,其简易工艺流程如图(部分副产物省略,铼在废液中以ReO4-形式存在):

回答下列问题:
(1)铼不溶于盐酸,可溶于稀硝酸生成高铼酸。高铼酸组成与高氯酸相似,写出反应的化学方程式:______。
(2)操作 A的名称是_____。 “萃取”中萃取剂应具有的性质:_______(填代号)。
①萃取剂难溶于水
②萃取剂的密度大于水
③ReO4-在萃取剂中的溶解度大于在水中的溶解度
④萃取剂不和 ReO4-发生反应
(3)在“反萃取”中,加入氨水、水的目的是_____。
(4)在高温下高铼酸铵分解生成 Re2O7,用氢气还原 Re2O7,制备高纯度铼粉。
①写出高铼酸铵分解生成 Re2O7的化学方程式_______。
②工业上,利用氢气还原 Re2O7制备铼,根据生成铼的量计算氢气量,实际消耗 H2量大于理论计算量,其原因是______。
(5)工业上,高温灼烧含 ReS2的矿粉,可以制备 Re2O7。以含 ReS2 的矿石原料生产 48.4tRe2O7, 理论上转移_____mol电子。
-
2011年3月9日,美国“发现”号航天飞机结束它的最后一次飞行使命,于佛罗里达肯尼迪航天中心着陆,未来的航天科技又将翻开新的篇章,胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得:101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量.下列说法或热化学方程式书写正确的是( )
A.胶状液氢的标准燃烧热比甲烷要高
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890.3kJ•mol-1
C.一般H2加压后以液态形式保存,且液氢燃烧效果比氢气要好,释放热量更多
D.2H2(g)+O2(g)═2H2O(l);△H=-285.8kJ
-
据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可
能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
A.离子键 B.共价键 C.一种静电引力 D.一种静电斥力
-
下列有关化学与生活说法正确的是( )
A.“歼-20”飞机上使用的碳纤维被誉为“新材料之王”,是我国打破其他国家技术垄断,自主研发和生产的一种新型有机高分子材料
B.硫酸亚铁与维生素C混用有利于铁元素吸收
C.我国海洋开发走向深蓝,大型舰船的底部常镶嵌锌块做正极,防止船底腐蚀
D.白砂糖的主要成分是蔗糖,蔗糖属于高分子化合物
-
据悉:2007年9月,美国科学家宣称发现了普通盐水在无线电波照射下可燃烧,这很可能是21世纪人类最伟大的发现之一,有望解决用水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是( )
A.极性共价键 B.氢键
C.非极性共价键 D.分子间作用力
-
2007年9月,美国科学家宣称:普通盐水在无线电波照射下可燃烧,这项伟大的发现,有望解决用水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是( )
A.分子间作用力 B.氢键
C.非极性共价键 D.极性共价键
-
美国科学家宣称发现了普通盐水在无线电波照射下可燃烧,有望解决用水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该种频率下持续燃烧。上述中“结合力”实质是( )
A.分子间作用力 B.氢键
C.非极性共价键 D.极性共价键
-
(12分)氮元素可以形成多种氢化物,如NH3、N2H4等。
(1)据报道,2016年中国将发射“天宫二号”空间实验室,并发射“神舟十一号”载人飞船和“天舟一号”货运飞船,与“天宫二号”交会对接。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4作氧化剂。已知
N2(g)+O2(g)=2NO(g)△H=+180.7kJ•mol-1
2NO(g)+O2(g)=2NO2(g)△H=-113.0kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ•mol-1
2NO2(g) N2O4(g)△H=-52.7kJ•mol-1
N2O4(g)△H=-52.7kJ•mol-1
写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式:______________.
(2)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g),该反应的平衡常数和温度关系如下所示:
CO(NH2)2(l)+H2O(g),该反应的平衡常数和温度关系如下所示:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①该反应的△H 0(填“>”或“<”)。
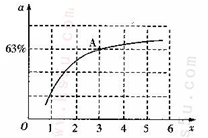
②已知原料气中的氨碳比 为x,CO2的平衡转化率为a,在一定温度和压强下,a与x的关系如下图所示。a随着x的增大而增大的原因是__________。图中A点处,NH3的平衡转化率为__________。
为x,CO2的平衡转化率为a,在一定温度和压强下,a与x的关系如下图所示。a随着x的增大而增大的原因是__________。图中A点处,NH3的平衡转化率为__________。
(3)①在氢水加水稀释的过程中,NH3·H2O的电离程度____(填“增大”、“减小”或“不变”,下同),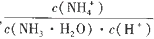 的值__________。
的值__________。
②室温下,amol/L的(NH4)2SO4溶液的pH=5,原因是__________________(用离子方程式表示),该反应的平衡常数为__________(用含a的数学表达式表示)。
-
第ⅢA元素也称为硼族元素,除硼外其余均为金属元素。硼的应用非常广泛,可用于原子反应堆和高温技术,甚至可用来制作火箭中所用的某些结构材料。
(1)硼元素位于元素周期表第__________周期。铝与氢氧化钠溶液反应的离子方程式为_________________________。
(2)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂(主要成分为Na2B4O7·10H2O)为起始物,经过一系列反应可以得到BN、B和BF3等。

①反应a的化学方程式为________,为了加快反应a的化学反应速率可采取的措施有_____________(回答一条即可)。
②生成BN的化学反应_________(填“是”或“不是”)氧化还原反应。
③由B2O3制硼时所得到的产品不纯,主要含有的杂质为____________。
(3)有一类硼烷形似鸟巢,故称为巢式硼烷,如下有三种巢式硼烷的结构:

①根据五硼烷和六硼烷的化学式,推测十硼烷的化学式为_____________ 。
②已知:B6H10+O2→B2O3+H2O(未配平),每1 mol B6H10完全燃烧时转移__________mol电子。
(4)NaBH4被称为“万能还原剂”,近年来常用NaBH4与过氧化氢构建一种新型碱性电池,如图所示;则该电池放电时的负极反应式为___________,正极附近溶液的pH会___________。(填“增大”、“减小”或“不变”)。

HCHO+H2↑,上述反应两种有机物中碳原子的杂化形式分别是______和_______。C、H、O三种元素中,电负性最大的是______(填元素符号)。
2MnO4-+10SO42-+16H+。已知H2S2O8的结构简式如图所示。




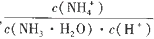 的值__________。
的值__________。

