-
“转化”是化学研究的重要范畴之一。请回答下列有关问题。
Ⅰ. 沉淀转化在科研和生产中具有重要的应用价值。当容器壁上沉积一厚层BaSO4时,是很难直接除去的。除去的方法是向容器壁内加入Na2CO3溶液,使BaSO4转化为BaCO3,然后加盐酸洗去沉淀物。已知常温Ksp(BaCO3)=5.1×10-9,Ksp(BaSO4)=1.1×10-10。
(1)Na2CO3俗称纯碱,被广泛应用于生活和工业生产中。Na2CO3溶液呈碱性,用水解离子方程式解释其呈碱性的原因______________________________。
(2)要使BaSO4转化成BaCO3,Na2CO3溶液的浓度应大于_______mol/L。(设定: ≈1)
≈1)
Ⅱ. 合成是转化的一种应用,甲醇作为一种可再生能源,工业上一般采用下列两种反应合成甲醇:
反应一:CO(g)+2H2(g)  CH3OH(g) ∆H1
CH3OH(g) ∆H1
反应二:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ∆H2
CH3OH(g)+H2O(g) ∆H2
(1)相同条件下,反应:CO2(g)+H2(g)  CO(g)+H2O(g) ∆H3,则∆H3=_____(用∆H1和∆H2表示)。
CO(g)+H2O(g) ∆H3,则∆H3=_____(用∆H1和∆H2表示)。
(2)下表所列数据是反应CO(g)+2H2(g)  CH3OH(g) ∆H1在不同温度下的化学平衡常数(K)
CH3OH(g) ∆H1在不同温度下的化学平衡常数(K)
| 温度/℃ | 250 | 300 | 350 |
| 平衡常数(K) | 2.04 | 0.27 | 0.012 |
①此反应的∆H1______0,∆S______0。(填“>”、“=”或“<“)
②某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2 mol/L,则CO的转化率是____,此时的温度是_____。
③要提高CO的转化率,可以采取的措施是____________
A.升温 B.恒容充入CO C.恒容充入H2 D.恒压充入惰性气体 E.分离出甲醇
-
化学变化中的能量转换对于生产具有重大意义和研究价值。回答下列问题:
(l)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22的表面将CO2转化为烷烃,其过程如图。
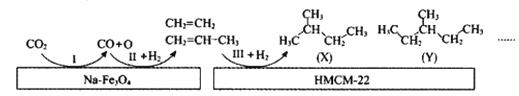
①过程Ⅰ能量__(填“释放”或“吸收”。
②已知:CO2(g)+H2(g)═CO(g)+H2O(g) △H═+41kJ•mol-1:
2CO2(g)+6H2(g)═C2H4(g)+4H2O(g) △H═-128kJ•mol-1:
3CO2(g)+9H2(g)═C3H6(g)+6H2O(g) △H═+157.5kJ•mol-l
C2H4(g)+C3H6(g)+H2(g)═C5H12(异戊烷,g) △H=+267.6kJ•mol-1。
则5CO(g)+11H2(g)═C5H12(异戊烷,g)+5H2O(g)△H=__kJ•mol-1。
(2)一种铜版画雕刻用的酸性蚀刻液的有效成份是CuCl2,蚀刻反应为:Cu2++Cu+6Cl-═2CuCl32-。工业上用电解法将CuCl32-转化为Cu2+,使蚀刻液再生并回收金属Cu。装置如图(电极不参与反应)。
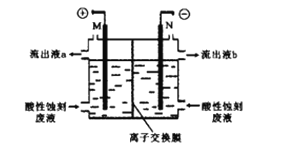
①再生的CuCl2蚀刻液为流出液__(填“a”或“b”)。
②写出N极的电极反应:__。
③装置中使用___离子交换膜(填“阳”或“阴”)。若电解池工作前,阴极室和阳极室中电解液质量相等,当转移0.1mol电子,流出液未流出时,两侧电解液的质量差为__g。
-
氮元素可形成多种化合物,在工业生产中具有重要价值。请回答下列问题:
(1)一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行合成氨反应。
①下列描述能说明该可逆反应达到化学平衡状态的有__。
A.容器内气体的密度不变
B.c(N2):c(H2):c(NH3)=1:3:2
C.容器内的压强不变
D.相同时间内有3molH-H键断裂,有6molN-H键形成
E.3v正(H2)=2v逆(NH3)
F.容器内气体的平均相对分子质量不变
②恒温恒压条件下,为提高合成氨反应中N2和H2的利用率,可采用的方法__(一种即可)。
(2)一定温度下,2L密闭容器中充入0.40molN2O4,发生反应:N2O4(g) 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①20s内,v(NO2)=__,该温度下反应的化学平衡常数数值为__。
②升高温度时,气体颜色加深,则正反应是__(填“放热”或“吸热”)反应。
③相同温度下,若开始向该容器中充入0.40mo1NO2,则达到平衡后:c(NO2)__0.15mol/L(填“>”、“=”或“<”)
-
化学反应原理在生产和科研中有重要的应用,请利用相关知识回答下列问题。
I.常温下I2O5(s)可用于检测CO,反应原理为:5CO(g)+I2O5(s)  5CO2(g)+I2(s) △H<0.一定温度下,向2L恒容密闭容器中加入足量I2O5(s),并通入1molCO。反应中CO2的体积分数φ(CO2)随时间的变化如图所示:
5CO2(g)+I2(s) △H<0.一定温度下,向2L恒容密闭容器中加入足量I2O5(s),并通入1molCO。反应中CO2的体积分数φ(CO2)随时间的变化如图所示:
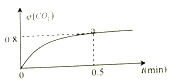
(1)该反应的平衡常数表达式K=__________;
(2)0~0.5min内的平均反应速率v(CO)=_________;
(3)下列叙述能说明反应达到平衡的是( )
A.容器内压强不再变化
B.CO的质量不再变化,CO2的转化率不再增大
C.CO2的生成速率等于CO的消耗速率,反应物不再转化为生成物
D.混合气体的平均相对分子质量不再改变
(4)保持温度和体积不变,若开始加入CO(g)的物质的量是原来的2倍,则下列说法正确的是( )
A.平衡时生成I2的质量为原来的2倍
B.达到平衡的时间为原来的2倍
C.平衡时混合气体的物质的量为原来的2 倍
D.平衡时混合气体的密度不变
II.一定条件下在密闭容器中加入NH4I发生反应:A.NH4I(s) NH3(g)+HI(g),
NH3(g)+HI(g),
B.2HI(g)  H2(g)+I2(g)。达到平衡后,扩大容器体积,反应b 的移动方向___________(填正向、逆向或不移动);
H2(g)+I2(g)。达到平衡后,扩大容器体积,反应b 的移动方向___________(填正向、逆向或不移动);
III.己知:2NO2 N2O4 △H<0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )
N2O4 △H<0,将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )

A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若反应在一绝热容器中进行,则b、c两点的平衡常数Kb>Kc
D.d点:v(正)>v(逆)
-
化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) 2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
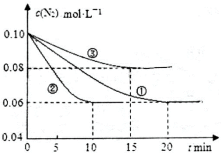
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=_______________;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项 中的______________、_____________(填字母编号)。
中的______________、_____________(填字母编号)。
A增大压强 B减小压强 C升高温度 D降低温度 E使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g) N2O4(g)。
N2O4(g)。
T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)=0.05 mol/L,则该反应的平衡常数K=_______________;
-
如图表示各物质之间的转化关系,其中A、B、C、G为单质.②为工业生产中常见反应,E是一种具有漂白作用的盐,Y易潮解,M是一种两性化合物,L是一种白色沉淀.

试完成下列有关问题:
(1)M的化学式为______.Y在实验室中的用途有______(列举一列)
(2)X的熔点为801℃,实际工业冶炼中常常加入一定量的Y共熔,猜想工业上这样做的目的:______;工业生产中,还常常惰性电极电解X和F的混合物,该反应的阳极电极反应式为______.
(3)反应②的化学方程式是______.
(4)反应④的离子方程式是______.
-
端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应.

该反应在研究新型发光材料、超分子化学等方面具有重要价值 下面是利用Glaser反应制备化合物E的一种合成路线:
下面是利用Glaser反应制备化合物E的一种合成路线:
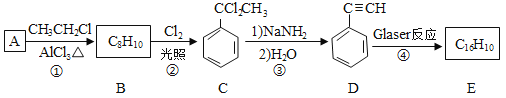
回答下列问题:
(1)D的分子式为______.
(2)③和④的反应类型分别为______、______.
(3) 的结构简式为_____,
的结构简式为_____,
(4)写出②反应的化学方程式______.
(5)B的一氯代物有____________________种。
-
(13分)铜(Cu)是重要金属,铜的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)向CuSO4浓溶液中滴入浓氨水,直至产生的沉淀恰好溶解,可得到深蓝色的透明溶液。再向其中加入适量乙醇,可析出深蓝色的Cu(NH3)4SO4•H2O晶体。
①沉淀溶解的离子方程式为_______________________________________________。
②乙醇的作用是_________________________________________________________。
③[Cu(NH3)4]2+具有对称的立体构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的立体构型为____________________,其中N原子的杂化轨道类型是________。
(2)金(Au)与铜为同族元素,铜与金可形成具有储氢功能的合金。
①合金中,原子间的作用力是_______________。已知Au为第六周期元素,则基态Au原子的价电子排布式为________,Au的原子序数为________。
②该储氢合金为立方最密堆积结构,晶胞中Cu原子位于面心、Au原子位于顶点,储氢时,H原子进入由Cu原子与Au原子构成的四面体空隙中,则该晶体储氢后的化学式为_______________。
-
铜(Cu)是重要金属,铜的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)向CuSO4浓溶液中滴入浓氨水,直至产生的沉淀恰好溶解,可得到深蓝色的透明溶液。再向其中加入适量乙醇,可析出深蓝色的Cu(NH3)4SO4•H2O晶体。
①沉淀溶解的离子方程式为_______________________________________________。
②[Cu(NH3)4]2+具有对称的立体构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的立体构型为_________________(用文字表述),其中N原子的杂化轨道类型是________。
(2)金(Au)与铜为同族元素,铜与金可形成具有储氢功能的合金。
①合金中,原子间的作用力是_______________。已知Au为第六周期元素,则基态Au原子的价电子排布式为________。
②该储氢合金为立方最密堆积结构,晶胞中Cu原子位于面心、Au原子位于顶点,储氢时,H原子进入由Cu原子与Au原子构成的四面体空隙中,则该晶体储氢后的化学式为_______________。
-
沉淀溶解平衡在生产、科研和环保等领域有着许多应用。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是______。(已知lg5=0.7)
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
| 操作步骤 | 现象 |
| 步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液 | 溶液变为红色 |
| 步骤3:向步骤2的溶液中继续加入5滴3 mol·L-1 AgNO3溶液 | 现象a,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变为红色的离子方程式:____________________。
②步骤3中现象a是____________________________。
③用化学平衡原理解释步骤4中的实验现象:_________________________________。
≈1)
CH3OH(g) ∆H1
CH3OH(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H3,则∆H3=_____(用∆H1和∆H2表示)。
CH3OH(g) ∆H1在不同温度下的化学平衡常数(K)






