298K时,向体积均为15.0mL,浓度均为1.00mol/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列有关叙述正确的是
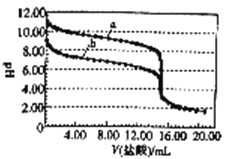
A.曲线a是NaHCO3溶液的滴定曲线
B.当V(盐酸)=4.00mL时,c(HCO3-)>c(NH4+)>c(CO32-)
C.当V(盐酸)=15.00mL时,c(Na+)=c(NH4+)
D.两个滴定过程均可选择酚酞作指示剂
高二化学单选题中等难度题
298K时,向体积均为15.0mL,浓度均为1.00mol/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列有关叙述正确的是

A.曲线a是NaHCO3溶液的滴定曲线
B.当V(盐酸)=4.00mL时,c(HCO3-)>c(NH4+)>c(CO32-)
C.当V(盐酸)=15.00mL时,c(Na+)=c(NH4+)
D.两个滴定过程均可选择酚酞作指示剂
高二化学单选题中等难度题
298K时,向体积均为15.0mL,浓度均为1.00mol/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列有关叙述正确的是

A.曲线a是NaHCO3溶液的滴定曲线
B.当V(盐酸)=4.00mL时,c(HCO3-)>c(NH4+)>c(CO32-)
C.当V(盐酸)=15.00mL时,c(Na+)=c(NH4+)
D.两个滴定过程均可选择酚酞作指示剂
高二化学单选题中等难度题查看答案及解析
298K时,在20.0mL0.10 mol L–1氨水中滴入0.10 mol L–1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol L–1氨水的电离度为1.32%,下列有关叙述正确的是
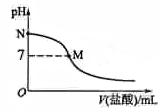
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
高二化学选择题困难题查看答案及解析
298K时,在20.0mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
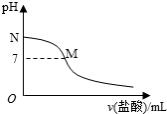
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为20.0mL
C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D.N点处的溶液中pH<12
高二化学选择题中等难度题查看答案及解析
298K时,在20.0ml0.10mol/L氨水中滴入0.10mol/L的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol/L氨水的电离度为1.32%,下列有关叙述不正确的是
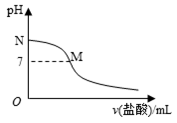
A.该滴定过程应该选择甲基橙作为指示剂
B.M点对应的盐酸体积为20.0 mL
C.M点处的溶液中c(NH4+)=c(Cl-)>c(H+)=c(OH-)
D.N点处的溶液中pH<13
高二化学选择题困难题查看答案及解析
298K 时,在 20.0mL0.l0mol•L-1 氨水中滴入 0.l0mol•L-1 的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.l0mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
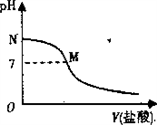
A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M 点处的溶液中 c(NH4+) =C(C1-)=C(H+) =c(OH-)
D. N点处的溶液中pH <12
高二化学选择题困难题查看答案及解析
(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。
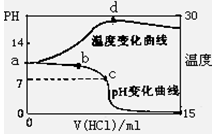
(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | pH>7 | / | |
| ② | NH4Cl | / | ||
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | pH<7 | / |
高二化学填空题简单题查看答案及解析
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | ______ | pH>7 | / |
| ② | NH4Cl | / | ______ | |
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | ______ | pH<7 | / |

高二化学解答题中等难度题查看答案及解析
室温下,用0.10mol/L的盐酸分别滴定20.00mL浓度均为0.10mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。
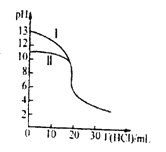
下列说法不正确的是
A. Ⅱ表示的是滴定氨水的曲线,当V(HC1)=20mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且c(NH4+)=c(Cl-)
C. 滴定氢氧化钠溶液,V(HCl) >20 mL 时一定有: c(Cl-) >c(Na+) >c(H+) >c(OH-)
D. 当滴定氨水消耗V(HC1)=10 mL 时,有: 2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
高二化学单选题中等难度题查看答案及解析
常温下,向20 mL 0.1 mol•L-1氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。
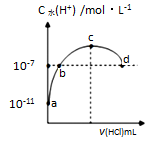
则下列说法正确的是
A. 常温下,0.1mol•L-1氨水的电离常数K约为1×10-5mol•L-1
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)=c(Cl-)
D. d点代表两溶液恰好完全反应
高二化学选择题困难题查看答案及解析
常温下,向20 mL某浓度的盐酸中逐滴加入0.1 mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示。下列叙述正确的是
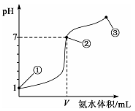
A.盐酸的物质的量浓度为l mol/L
B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-)
C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20
D.在点③所示溶液中:由水电离出的c(OH-)>l0-7mol/L
高二化学选择题中等难度题查看答案及解析