-
NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃时,1 L pH=1的HCl溶液中,由水电离的H+的个数为0.1NA
B. 25℃时,浓度为0.1 mol/L NaHCO3溶液中含有HCO3-数小于0.1NA
C. 标准状况下,NA个HF分子所占有的体积约为22.4 L
D. 1 mol (NH4)2Fe(SO4)2·6H2O晶体中含有离子总数为5NA
高二化学单选题中等难度题查看答案及解析
-
NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.25℃时,1L pH=1的HCl溶液中,由水电离的H+的个数为0.1NA
B.25℃时,浓度为0.1mol/L NaHCO3溶液中含有HCO3-数小于0.1NA
C.标准状况下,NA个HF分子所占有的体积约为22.4L
D.1mol (NH4)2Fe(SO4)2·6H2O晶体中含有离子总数为5NA
高二化学选择题中等难度题查看答案及解析
-
NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃时,1LpH=l的HCl溶液中,由水电离的H+的个数为0.1NA
B. 25℃时,0.1mol/LNaHCO3溶液中含有HCO3-数小于0.1NA
C. 标准状况下,NA个H2O分子所占有的体积约为22.4L
D. lmol(NH4)2Fe(SO4)2·6H2O固体中含有离子总数为5NA
高二化学选择题中等难度题查看答案及解析
-
若NA表示阿伏加德罗常数,则下列说法正确的是( )
A.100℃时水的Kw=1×10-12,此时水电离产生的H+和OH-个数之和为2×10-6NA
B.1L0.1mol/L的盐酸中含有的HCl分子数为0.1NA
C.1LpH=1的H2SO4溶液中含有的SO2-4为0.05NA
D.1molN2和3molH2在有催化剂加热的条件下充分反应生成2NA个NH3高二化学选择题中等难度题查看答案及解析
-
用0.1 mol/L的NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol/L的HCl溶液和HX溶液,溶液的pH随加入 NaOH溶液体积的变化如图所示。下列说法正确的是
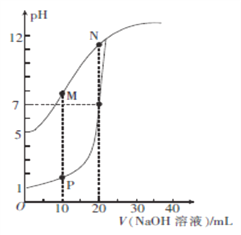
A. HX的电离平衡常数Ka约为1×10-5
B. M点对应溶液中:c(HX)< c (X-)
C. P点对应溶液中: c(Cl-)=0.05mol/L
D. N点对应溶液中:c(Na+)>c(X-)>c(OH-) >c(H+)
高二化学单选题中等难度题查看答案及解析
-
设 NA为阿伏加德罗常数的值,下列说法正确的是( )
A.足量铜与 100mL 18mol/L 的浓硫酸在一定条件下反应转移的电子数目为1.8 NA
B.常温下,pH=13 的氢氧化钠溶液中由水电离出的H+的数目为 10-13NA
C.标准状况下,2.24 L CCl4含有的共价键数为 0.4NA
D.加热条件下,16g O2、O3的混合气体与足量镁粉充分反应转移的电子数目为 2NA
高二化学单选题中等难度题查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3
2HNO3+4N2↑+9H2O反应,生成28gN2时,转移的电子数目为3.75NA
高二化学单选题中等难度题查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
B.常温下,1L pH=10的氨水溶液中,发生电离的水分子数为1×10-10NA
C.电解精炼铜时,阴极增重3.2g,电路中转移电子数为0.05NA
D.将0.1mol O2与0.2mol NO在密闭容器中充分反应,反应后容器内分子数为0.2NA
高二化学单选题中等难度题查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,4.48L的Cl2通入水中反应转移的电子数为0.2NA
B.常温下pH=3的FeCl3溶液中由水电离出的H+的数目为0.001NA
C.273K、101kPa下,22.4L甲烷充分燃烧后,所得气体产物的分子总数为NA
D.1L0.1mol⋅L−1氢氧化钠溶液中含有的H-O键的数目为0.1NA
高二化学单选题中等难度题查看答案及解析
-
设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 2L 0.5mol/L亚硫酸溶液中含有的H+离子数为2NA
B. 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g
D. 某密闭容器中盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目小于0.6NA
高二化学单选题简单题查看答案及解析