-
电池有广泛的用途。
Ⅰ.依据氧化还原反应:Cu+2Ag+===Cu2++2Ag设计的原电池如图所示。请回答下列问题:
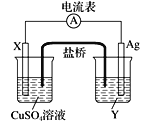
(1)电极X的材料是________________,电解质溶液Y是____________。
(2)银电极的电极反应式是______________________________。
(3)外电路中的电子是从_____极流向_____极。(填“正”或“负”)
(4)该原电池的正极是____________,还可以选用__________________等材料。
Ⅱ.铅蓄电池是化学电源,它工作时的电池总反应为:PbO2+Pb+2H2SO4===2PbSO4+2H2O。试回答:
(5)蓄电池负极的电极材料是_____________________(填“PbO2”或“Pb”)。
(6)工作时该蓄电池正极的电极反应式是___________。
(7)铅蓄电池工作时,电解质溶液的密度________(填“增大”、“减小”或“不变”),负极质量____ (填“增大”、“减小”或“不变”)。
Ⅲ.某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(8)此原电池的正极是石墨________(填“a”或“b”),发生________反应。
(9)电池工作时,盐桥中的SO 移向________(填“甲”或“乙”)烧杯。
移向________(填“甲”或“乙”)烧杯。
(10)甲烧杯中的电极反应式为________________________________。
(11)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
-
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
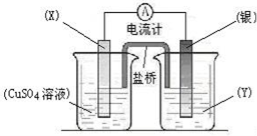
(1)电极X的材料是 (化学式);电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
-
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图。请回答下列问题:
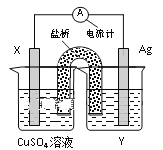
(1)电极X的材料名称是___;电解质溶液Y溶质的化学式是___;
(2)银电极为电池的___极,发生的电极反应为___;
(3)外电路中的电子是从___电极流向___电极。(填电极材料名称)。
(4)当有1.6g铜溶解时,银棒增重___g。
-
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是______;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极.

-
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
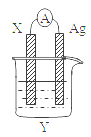
(1)电极X的材料是______;电解质溶液Y是________;
(2)银电极为电池的____极,发生的电极反应式为______; X电极上发生的电极反应为______;(填反应类型)
(3)外电路中的电子是从_______电极流向________电极。Ag+向_______ (填正极或负极)移动。
(4)当有1.6g铜溶解时,银棒增重_________________。
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O; B极:O2+4e-=2O2-。则A极是电池的______极;电子从该极____(填“流入”或“流出”),该电池的总反应为_______。
-
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是______;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极.

-
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是______;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极.
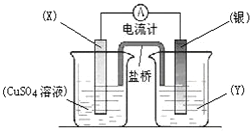
-
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是______;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极.
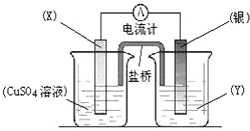
-
依据氧化还原反应:2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
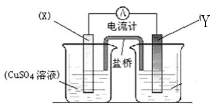
(1)电极X的材料是______ ;电极Y材料是__________ 。
(2)银电极上发生的电极反应为____________;X电极上发生的电极反应为____________。
(3)外电路中的电子是从______电极流向______电极。(填“X”或“Y”)
-
依据氧化还原反应:2Ag+(aq) +Cu(s) =Cu2+(aq) +2Ag(s)设计的原电池如图所示。请回答下列问题:
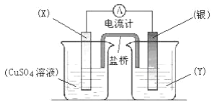
(1)电极 X 的材料是_____; 电解质溶液 Y 是________;
(2)银电极为电池的_____极,发生的电极反应为____________X 电极上发生的电极反应为__________
(3)外电路中的电子是从_____电极流向_____电极。


移向________(填“甲”或“乙”)烧杯。








