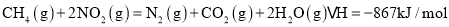-
(14分)目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为: 。
它所对应的化学反应为: 。
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
| | | | | | |
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填选项字母)。
A.=0.8 mol·L-1 B.=1.4 mol·L-1
C.<1.4 mol·L-1 D.>1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平衡时各气体的体积分数与甲容器完全相同的是 (填选项字母)。
A.0.6 mol 1.0 mol 0.5 mol 1.0 mol
B.0.6 mol 2.0 mol 0 mol 0 mol
C.1.0 mol 2.0 mol 1.0 mol 2.0 mol
D.0.25 mol 0.5 mol 0.75 mol 1.5 mol
(3)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S 0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。
若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
-
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为: 。
它所对应的化学反应为: 。
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
| | | | | | |
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填字母)。
A.=0.8 mol·L-1 B.=1.4 mol·L-1 C.<1.4 mol·L-1 D.>1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平衡时各气体的体积分数与甲容器完全相同的是 (填字母)。
A.0.6 mo l 1.0 mol 0.5 mol 1.0 mol
l 1.0 mol 0.5 mol 1.0 mol
B.0.6 mol 2.0 mol 0 mol 0 mol
C.1.0 mol 2.0 mol 1.0 mol 2.0 mol
D.0.25 mol 0.5 mol 0.75 mol 1.5 mol
(3)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S 0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。若以1. 12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
-
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为:__ ___
它所对应的化学反应为:__ ___
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol[ | 达到平衡所需时间/min |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1,2 | 3 |
①T10C时,该反应的平衡常数K=_______
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度_______ (填选项字母)。
A.=0.8 mol·L-1 B.=1.4 mol·L-1 C.<1.4 mol·L-1 D.>1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平 衡时各气体的体积分数与甲容器完全相同的是_______(填选项字母)。
A.0.6 mol、1.0 mol、0.5 mol、1.0 mol
B. 0.6 mol、2.0 mol、0 mol、0 mol
C.1.0 mol、2.0 mol、1.0 mol、2.0 mol
D. 0.25 mol、0.5 mol、0.75 mol、1.5 mol
(3)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,已知CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
(4)将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g)+ 6H2(g) CH3OCH3(g)+ 3H2O(g)
CH3OCH3(g)+ 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2)/ n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S___0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
-
(14分)目前“低碳经济”备受关注。CO2的产生及有效开发利用成为科学家研究的重要课题。试利用所学知识,解决下列问题。
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为:_________________
它所对应的化学反应为:_________________
(2)一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需的时间/min |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
| | | | | | |
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填选项字母).
A.=0.8mol•L﹣1 B.=1.4mol•L﹣1
C.<1.4mol•L﹣1 D.>1.4mol•L﹣1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g),达到平衡时各气体的体积分数与甲容器完全相同的是 (填选项字母).
A.0.6mol、1.0mol、0.5mol、1.0mol
B.0.6mol、2.0mol、0mol、0mol
C.1.0mol、2.0mol、1.0mol、2.0mol
D.0.25mol、0.5mol、0.75mol、1.5mol
(3)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[ ] ] | 500K | 600K | 700K | 800K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S 0(填>、<或=).
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 .若以1.12L•min﹣1(标准状况)的速率向该电池中通入甲醚(沸点为﹣24.9℃),用该电池电解500mL 2mol•L﹣1 CuSO4溶液,通电0.50min后,理论上可析出金属铜 g.
-
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。
(1)一定条下:C(s)+2H2O(g) CO2(g)+2H2(g)已知:C和H2的燃烧热分别为393.5KJ/mol和285.8KJ/mol,且H2O(1)=H2O(g) △H=+44.0KJ/mol.则该反应的△H= 。在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生此反应,其相关数据如下表所示:
CO2(g)+2H2(g)已知:C和H2的燃烧热分别为393.5KJ/mol和285.8KJ/mol,且H2O(1)=H2O(g) △H=+44.0KJ/mol.则该反应的△H= 。在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生此反应,其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | T1 | 2 | 4 | 3.2 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 |
| | | | | |
①T1 T2(填“>”、“=”或“<”).
②若乙容器中达到平衡所需时间为3min,则当反应进行到1.5mol时,H2O(g)的物质的量的浓度 (填选项字母)。
A.=0.8mol/L B.=1.4mol/L C.< 1.4mol/L D.> 1.4mol/L
③T2℃下,乙容器中若起始充入a molCO2和b molH2,反应达到平衡时,测得CO2的转化率大于H2的转化率,则a/b的值需满足的条件为 。
(2)用二氧化碳合成甲醇是碳减排的新方向。将CO2转化为甲醇的热化学方程式为CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H1 取五份等体体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇反应的H1 0(填“>”、“<”或“=”)。
CH3OH(g)+H2O(g) △H1 取五份等体体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇反应的H1 0(填“>”、“<”或“=”)。

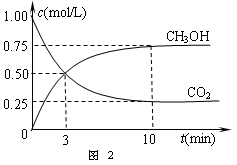
②在容积为1L的恒温密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图2所示。若在上述平衡体系中再充0.5 mol CO2和1.5 mol H2O(g)(保持温度不变),则此平衡将 移动(填“向正反应方向”、“不”或“逆反应方向”)
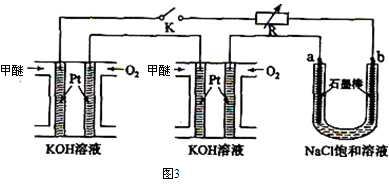
(3)CO2在一定的条件下,还可以转化为甲醚(CH3OCH3)。某研究小组将两个甲醚燃料电池串联后作为电源,电解饱和食盐水,装置如图3所示。
①请写出该甲醚燃料电池负极的电极反应式 。
②若U形管中氯化钠溶液的体积为600mL。闭合K后,若每个电池甲醚用量均为0.0112L(已折算到标准状况),且反应完全,假设产生的气体全部逸出,电解后溶液混合均匀,则电解后U形管中溶液的pH为 。
(4)常温下,用NaOH溶液吸收CO2得到pH=11的Na2CO3溶液,吸收过程中水的电离平衡将 移动(填“正向”、“不”、“逆向”);使计算溶液中 = 。(已知常温下,H2CO3的电离平衡常数为K1=4.4×10-2,K2=4.7×10-11)
= 。(已知常温下,H2CO3的电离平衡常数为K1=4.4×10-2,K2=4.7×10-11)
-
目前,“低碳经济”备受关注, 的产生及有效开发利用成为科学家研究的重要课题.
的产生及有效开发利用成为科学家研究的重要课题.
 向浓
向浓 溶液中通入
溶液中通入 和
和 ,可以制得纳米级碳酸钙
,可以制得纳米级碳酸钙 粒子直径在
粒子直径在 之间
之间 ①向浓
①向浓 溶液中通人
溶液中通人 和
和 气体制纳米级碳酸钙时,应先通入
气体制纳米级碳酸钙时,应先通入 ,后通 入
,后通 入 制备纳米级碳酸钙的离子方程式为 ______ ②判断产品中是否含有纳米级碳酸钙的实验方法为 ______ .
制备纳米级碳酸钙的离子方程式为 ______ ②判断产品中是否含有纳米级碳酸钙的实验方法为 ______ .
 定条件下,
定条件下, 和
和 反应,能生成
反应,能生成 和
和 将
将 和
和 分别 加入甲、乙两个密闭容器中,发生反应:
分别 加入甲、乙两个密闭容器中,发生反应: ,其相关数 据如下表所示:
,其相关数 据如下表所示:
| 容器 | 容积 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 |
| 
| 
| 
|
| 甲 | 2 | 
| 2 | 4 | 
| 8 |
| 乙 | 1 | 
| 1 | 2 | 
| 3 |
① 时,该反应的平衡常数
时,该反应的平衡常数 ______
______
②乙容器中,当反应进行到 时,
时, 的物质的量浓度 ______
的物质的量浓度 ______  填选项字母
填选项字母 .
.
A.



③丙容器的容积为1L, 时,起始充入a mol
时,起始充入a mol  和b mol
和b mol  ,反应达到平衡时,测得
,反应达到平衡时,测得 的转化率大于
的转化率大于 的转化率,则
的转化率,则 的值需满足的条件为 ______ ;
的值需满足的条件为 ______ ;
④丁容器的容积为1L, 时,按下列配比充入
时,按下列配比充入 、
、 、
、 和
和 ,达到平衡时各气体的体积分数与甲容器完全相同的是 ______
,达到平衡时各气体的体积分数与甲容器完全相同的是 ______  填选项字母
填选项字母 .
.
A. 、
、 、
、 、
、
B. 、
、 、O mol、O mol
、O mol、O mol
C. 、
、 、
、 、
、
D. 、
、 、
、 、
、
 在一定条件下可转化为甲醚
在一定条件下可转化为甲醚 用甲醚燃料电池做电源,用惰性电极电 解饱和
用甲醚燃料电池做电源,用惰性电极电 解饱和 溶液可制取
溶液可制取 和KOH,实验装置如图所示
和KOH,实验装置如图所示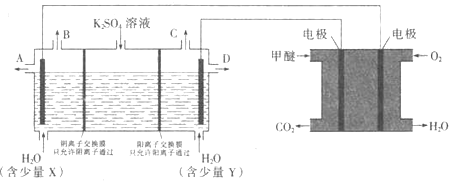
①甲醚燃料电池的负极反应式为 ______
② 口导出的物质为 ______
口导出的物质为 ______  填化学式
填化学式 .
.
③若燃料电池通入 的速率为
的速率为 ,2min时,理论上C口收集 到标准状况下气体的体积为 ______ .
,2min时,理论上C口收集 到标准状况下气体的体积为 ______ .
-
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.
(1)向浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙 粒子直径在1-100nm之间)。①向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入NH3,后通 入CO2,制备纳米级碳酸钙的离子方程式为 ______ ②判断产品中是否含有纳米级碳酸钙的实验方法为 ______.
粒子直径在1-100nm之间)。①向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入NH3,后通 入CO2,制备纳米级碳酸钙的离子方程式为 ______ ②判断产品中是否含有纳米级碳酸钙的实验方法为 ______.
(2)一定条件下,C(s)和H2O(g)反应,能生成CO2(g)和H2(g),将C(s)和H2O(g)分别 加入甲、乙两个密闭容器中,发生反应:C(s)+2H2O(g) CO2(g)+2H2(g)其相关数 据如下表所示:
CO2(g)+2H2(g)其相关数 据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/mol |
| C(s) | H2O(g) | H2(g) |
| 甲 | 2 | 
| 2 | 4 | 
| 8 |
| 乙 | 1 | 
| 1 | 2 | 
| 3 |
①T1℃时,该反应的平衡常数 ______
______
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 ____  填选项字母
填选项字母 .
.
A、=0.8mol·L-1 B、=1.4mol·L-1 C、<1.4mol·L-1 D、>1.4mol·L-1
③丙容器的容积为1L,T2℃时,起始充入a mol CO2(g)和b mol H2(g),反应达到平衡时,测得CO2的转化率大于 的转化率,则
的转化率,则 的值需满足的条件为 ______;
的值需满足的条件为 ______;
④丁容器的容积为1L, 时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g),达到平衡时各气体的体积分数与甲容器完全相同的是 ______
时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g),达到平衡时各气体的体积分数与甲容器完全相同的是 ______ 填选项字母
填选项字母 .
.
A 0.6mol、1.0mol、0.5mol、1.0mol
B 0.6mol、2.0mol、0 mol、0 mol
C 1.0mol、2.0mol、1.0mol、2.0mol
D 0.25mol、0.5mol、0.75mol、1.5mol
(3)CO2在一定条件下可转化为甲醚CH3OCH3用甲醚燃料电池做电源,用惰性电极电 解饱和K2SO4溶液可制取H2SO4和KOH,实验装置如图所示
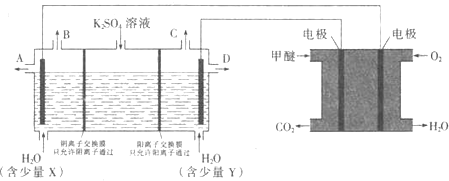
 甲醚燃料电池的负极反应式为 ______
甲醚燃料电池的负极反应式为 ______
 口导出的物质为 ______
口导出的物质为 ______  填化学式
填化学式 .
.
 若燃料电池通入CH3OCH3(g)的速率为0.1mol·L-1·min-1,2min时,理论上C 口收集 到标准状况下气体的体积为 ______.
若燃料电池通入CH3OCH3(g)的速率为0.1mol·L-1·min-1,2min时,理论上C 口收集 到标准状况下气体的体积为 ______.
-
目前“低碳减排”备受关注, 的产生及有效开发利用成为科学家研究的重要课题。
的产生及有效开发利用成为科学家研究的重要课题。
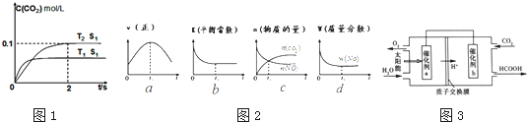
(1)汽车尾气净化的主要原理为 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度
随温度 、催化剂表面积
、催化剂表面积 和时间
和时间 的变化曲线如图1示。据此判断:
的变化曲线如图1示。据此判断:
①该反应的 ______
______ 填“
填“ ”或“
”或“ ”
” 。
。
②在 温度下,
温度下, 内的平均反应速率
内的平均反应速率 ______
______ 。
。
③当固体催化剂的质量一定时,增大其表面积可增大化学反应速率。若催化剂的表面积 ,在答题卡相应图中画出
,在答题卡相应图中画出 在
在 、
、 条件下达到平衡过程中的变化曲线_____。
条件下达到平衡过程中的变化曲线_____。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图如图2正确且能说明反应在进行到 时刻达到平衡状态的是______
时刻达到平衡状态的是______ 填代号
填代号 。
。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用 催化还原
催化还原 可以消除氮氧化物的污染。
可以消除氮氧化物的污染。
例如: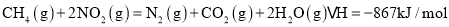

写出 催化还原
催化还原 生成
生成 、
、 和
和 的热化学方程式:______。
的热化学方程式:______。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图3通过人工光合作用,以 和
和 为原料制备HCOOH和
为原料制备HCOOH和 的原理示意图。催化剂b表面发生的电极反应为______
的原理示意图。催化剂b表面发生的电极反应为______
③常温下 的HCOONa溶液pH为10,则HCOOH的电离常数
的HCOONa溶液pH为10,则HCOOH的电离常数 ______
______ 填写最终计算结果
填写最终计算结果 。
。
-
“低碳经济”备受关注,CO2的捕捉、排集、利用成为科学家研究的重要课题。太空舱产生的 CO2用下列反应捕捉,以实现 O2的循环利用。
Sabatier 反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
水电解反应:2H2O(l) 2H2(g)+O2(g)
2H2(g)+O2(g)
(1)将原料气按 n(CO2)∶ n(H2)=1∶4 置于密闭容器中发生 Sabatier 反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
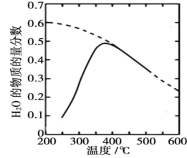
①该反应的平衡常数 K 随温度升高而________(填“增大”或“减小”)。
②温度过高或过低均不利于该反应的进行,原因是________。
③下列措施能提高 CO2 转化效率的是________(填标号)。
A. 适当减压
B. 增大催化剂的比表面积
C. 反应器前段加热,后段冷却
D. 提高原料气中 CO2 所占比例
E. 合理控制反应器中气体的流速
(2)将一定量的 CO2(g)和 CH4(g)通入一恒容密闭容器中发生反应:CO2(g)+CH4(g)⇌2CO(g)+2H2(g) Δ H =+248 kJ·mol-1。
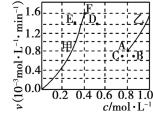
为了探究该反应的反应速率与浓度的关系,起始时向恒容密闭容器中通入CO2 与CH4 ,使其物质的量浓度均为1.0mol·L-1,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线如图, v正~ c(CH4)和 v逆 ~ c(CO)。则与 v正~ c (CH4)相对应曲线是图中________(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度反应重新达到平衡,则此时曲线甲对应的平衡点可能为________(填“D”“E”或“F”)。
(3)用稀氨水喷雾捕集 CO2最终可得产品NH4HCO3。在捕集时,气相中有中间体 NH2COONH4(氨基甲酸铵)生成。现将一定量纯净的氨基甲酸铵置于恒容密闭容器中,分别在不同温度下进行反应:NH2COONH4(s) ⇌2NH3(g)+CO2 (g)。实验测得的有关数据见下表( t1 < t2 < t3 )
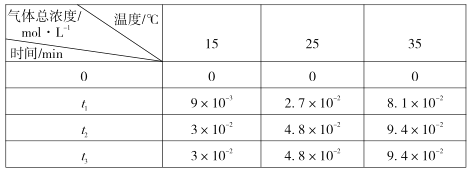
氨基甲酸铵分解反应是________(填“放热”或“吸热”)反应。15℃时此反应的化学平衡常数 K =________。
(4)一种新的循环利用方案是用 Bosch 反应 CO2(g)+2H2(g) ⇌C(s)+2H2O(g)代替 Sabatier 反应。
① 已知 CO2(g)、H2O(g)的生成焓分别为–394 kJ∙mol-1 、–242 kJ∙mol-1 ,Bosch 反应的Δ H =________kJ∙mol-1(生成焓指一定条件下由对应单质生成 1mol 化合物时的反应热)。
②一定条件下 Bosch 反应必须在高温下才能启动,原因是________。
③该新方案的优点是________。
-
目前低碳经济已成为科学家研究的主要课题之一,如何降低大气中 的含量及有效地开发利用
的含量及有效地开发利用 ,引起全世界的关注:
,引起全世界的关注:
(1)用电弧法合成的储氢材料常伴有大量的碳纳米颗粒 杂质
杂质 ,这些杂质颗粒通常用硫酸酸化的锰酸钾氧化除去,在反应中,杂质碳被氧化为无污染气体而除去,Mn元素转变为
,这些杂质颗粒通常用硫酸酸化的锰酸钾氧化除去,在反应中,杂质碳被氧化为无污染气体而除去,Mn元素转变为 ,请写出对应的化学方程式并配平: ______ ;
,请写出对应的化学方程式并配平: ______ ;
(2)将不同量的 和
和 分别通入到体积为2L的恒容密闭容器中,进行反应
分别通入到体积为2L的恒容密闭容器中,进行反应
 ,得到如下两组数据:
,得到如下两组数据:
| 实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所 需时间 |
| 
| CO | 
| CO |
| 1 | 650 | 2 | 4 | 
| 
| 5 |
| 2 | 900 | 1 | 2 | 
| 
| 3 |
①实验2条件下平衡时 体积分数为 ______ ;
体积分数为 ______ ;
②下列方法中可以证明上述已达平衡状态的是 ______ ;
 单位时间内生成n mol
单位时间内生成n mol  的同时生成n mol CO
的同时生成n mol CO
 容器内压强不再变化
容器内压强不再变化  混合气体密度不再变化
混合气体密度不再变化
 混合气体的平均相对分子质量不再变化
混合气体的平均相对分子质量不再变化  的质量分数不再变化
的质量分数不再变化
③已知碳的气化反应在不同温度下平衡常数的对数值 如下表,则反应
如下表,则反应 ,在900K时,该反应平衡常数的对数值
,在900K时,该反应平衡常数的对数值 ______ .
______ .
| 气化反应式 | lgK |
| 700K | 900K | 1200K |
| 
| 
| 
| 
|
| 
| 
| 
| 
|
(3)在高温下一氧化碳可将二氧化硫还原为单质硫.已知:






请写出CO除 的热化学方程式 ______ .
的热化学方程式 ______ .
(4) 时,
时, 和
和 的溶度积常数分别是
的溶度积常数分别是 和
和 ,某含有
,某含有 沉淀的悬浊液中
沉淀的悬浊液中 ,如果加入等体积的
,如果加入等体积的 溶液,若要产生
溶液,若要产生  沉淀,加入
沉淀,加入 溶液的物质的量浓度最小是 ______
溶液的物质的量浓度最小是 ______  .
.
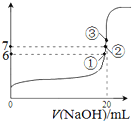
(5) 时,在
时,在 醋酸中加入V
醋酸中加入V  溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 ______ .
溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 ______ .
A. 的
的 溶液和
溶液和 的
的 溶液中,由水电离出的
溶液中,由水电离出的 相等
相等
B.①点时 ,此时溶液中,
,此时溶液中,
C.②点时,溶液中的
D.③点时 ,此时溶液中
,此时溶液中
(6)如图是一种新型燃料电池,它以CO为燃料,一定比例的 和
和 熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电进行粗铜的精炼实验.回答下列问题:
熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电进行粗铜的精炼实验.回答下列问题:
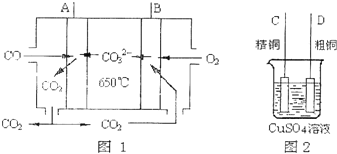
①写出A极发生的电极反应式 ______ ;
②要用燃料电池为电进行粗铜的精炼实验,则B极应该与 ______ 极 填“C”或“D”
填“C”或“D” 相连.
相连.
粒子直径在1-100nm之间)。①向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入NH3,后通 入CO2,制备纳米级碳酸钙的离子方程式为 ______ ②判断产品中是否含有纳米级碳酸钙的实验方法为 ______.
CO2(g)+2H2(g)其相关数 据如下表所示:
______
填选项字母
.
的转化率,则
的值需满足的条件为 ______;
时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g),达到平衡时各气体的体积分数与甲容器完全相同的是 ______
填选项字母
.

甲醚燃料电池的负极反应式为 ______
口导出的物质为 ______
填化学式
.
若燃料电池通入CH3OCH3(g)的速率为0.1mol·L-1·min-1,2min时,理论上C 口收集 到标准状况下气体的体积为 ______.