-
在密闭容器内,使1molN2和3molH2混合发生下列反应:3H2+N2 2NH3△H<0。
2NH3△H<0。
(1)合成氨时选择500℃高温的目的是______________。
(2)当反应达到平衡时,N2和H2的浓度比是_______。
(3)当达到平衡吋,充入氩气,并保持体积不变,平衡将______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将______移动,反应速率将_______。
(5)当达到平衡时,充入N2并保持体积不变,平衡将______移动。
(6)当达到平衡时,保持体积不变,升高温度时,混合气体的平均相对分子质量_______(选填“增大”“减小”或“不变”,后同),密度________。
-
在恒容的密闭容器内,使 1molN2和3molH2 混合发生下列反应:
3H2+N2 2NH3 ∆H<0
2NH3 ∆H<0
(1) 升高温度时,混合气体的密度_____。(填:“变大”或“变小”或“不变”)
(2)当达到平衡时,充入 N2,平衡将_____移动。(填:“正向”或“逆向”或“不”, 下同)
(3)当达到平衡时,充入Ar气,平衡将_____移动。
(4)当达到平衡时,将 c(N2)、c(H2)、c(NH3)同时增大 1 倍,平衡将_____移动。
-
在体积一定的密闭容器中1molN2和3molH2发生反应:N2+3H2 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( )
A.降低温度可以加快反应速率
B.向容器中再加入N2可以加快反应速率
C.达到化学反应限度时,生成2molNH3
D.达到化学平衡时N2、H2、NH3的物质的量之比为1:3:2
-
一定条件下,a L密闭容器中放入1molN2和3molH2发生N2+3H2 2NH3的反应,下列选项中能说明反应已达到平衡状态的是
2NH3的反应,下列选项中能说明反应已达到平衡状态的是
A.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
B.2v(H2)=3v(NH3)
C.单位时间内1个N≡N键断裂的同时,有6个N-H键断裂
D.单位时间消耗0.1molN2的同时,生成0.2molNH3
-
已知299K时,合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.0kJ·mol-1,将此温度下的1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)( )
2NH3(g) ΔH=-92.0kJ·mol-1,将此温度下的1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)( )
A.小于92.0kJ B.大于92.0kJ C.等于92.0kJ D.无法确定
-
(4分)298K时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)  2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1
在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4 kJ是________。
-
(4分)298K时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)  2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1
在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4 kJ是________。
-
将1molN2和3molH2充入某固定体积的密闭容器中,在一定条件下,发生反应N2(g)+3H2(g)⇌2NH3(g)ΔH<0并达到平衡,改变条件,下列关于平衡移动说法中正确的是( )
| 选项 | 改变条件 | 平衡移动方向 |
| A | 使用适当催化剂 | 平衡向正反应方向移动 |
| B | 升高温度 | 平衡向逆反应方向移动 |
| C | 再向容器中充入1molN2和3molH2 | 平衡不移动 |
| D | 向容器中充入氦气 | 平衡向正反应方向移动 |
A.A B.B C.C D.D
-
已知:可逆反应N2(g)+3H2(g) 2NH3(g)△H<0。现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2。下列叙述中正确的是
2NH3(g)△H<0。现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2。下列叙述中正确的是
A.达平衡时甲中NH3的体积分数为75%
B.达平衡时甲、乙中NH3的体积分数乙>甲
C.达到平衡后,再向乙中加入0.25molN2(g)、0.75molH2(g)和1.5molNH3(g),平衡向生成NH3的方向移动
D.乙中反应的热化学方程式为2NH3(g) N2(g)+3H2(g);△H=+Q2kJ/mol
N2(g)+3H2(g);△H=+Q2kJ/mol
-
Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g) 2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。

①若图中c=1.6mol,则改变的条件是__________(填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________(填字母);此时该反应的平衡常数__________(填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________。
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
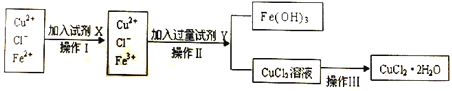
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
| 物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________(填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________。
2NH3△H<0。

