-
25℃时,浓度均为0.1mol•L﹣1的HA溶液和BOH溶液,pH分别是1和11.下列说法正确的是
A.在0.1 mol•L﹣1BA溶液中c(A﹣)+c(H+)=c(BOH)+c(OH﹣)
B.若将0.1 mol•L﹣1BOH溶液稀释至0.001 mol•L﹣1则溶液的pH=9
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A﹣)>c(B+)
D.若将上述两溶液按体积比1:2混合,则混合液中:c(B+)>c(A﹣)>c(OH﹣)>c(H+)
高二化学选择题困难题查看答案及解析
-
25℃时,浓度均为0.1mol·L-1的HA溶液和BOH溶液,pH分别是1和12。下列说法正确的是( )
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(OH-)
B.若将0.1mol·L-1BOH溶液稀释至0.001 mol·L-1则溶液的pH=10
C.若将一定量的上述两溶液混合后pH=7,则混
合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比l:2混合,则混合液中:c(B+)>c(A-)>c(OH-)>c(H+)
高二化学选择题困难题查看答案及解析
-
25℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(B+)
B.若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比1∶1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-)
高二化学选择题中等难度题查看答案及解析
-
25℃时,浓度均为0.1mol·L-1的HA溶液和BOH溶液,pH分别是1和12。下列说法正确的是
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(OH-)
B.若将0.1mol·L-1BOH溶液稀释至0.001 mol·L-1则溶液的pH=10
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比l:2混合,则混合液中:c(B+)>c(A-)>c(OH-)>c(H+)
高二化学选择题简单题查看答案及解析
-
25℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(B+)
B.若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比1∶1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-)
高二化学选择题中等难度题查看答案及解析
-
25 ℃时,浓度均为0.1 mol/L的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是( )
A. BOH溶于水,其电离方程式是BOH===B++OH-
B. 若一定量的上述两溶液混合后pH=7,则c(A-)=c(B+)
C. 在0.1 mol/L BA溶液中,c(B+)>c(A-)>c(OH-)>c(H+)
D. 若将0.1 mol/L BOH溶液稀释至0.001 mol/L,则溶液的pH=9
高二化学单选题中等难度题查看答案及解析
-
25 ℃时,浓度均为为0.1 mol/L的HA溶液和BOH溶液,pH分别是1和11,下列说法正确的
A.BOH溶于水,其电离方程式是BOH
B+ + OH-
B.若将一定量的上述溶液混合后pH = 7,则c(A- )= c(B+)
C.在0.1 mol/L BA溶液中,c(B+)> c(A- )> c(OH- )> c(H+)
D.若将0.1 mol/L BOH溶液稀释至0.001 mol/L,则溶液的pH = 9
高二化学选择题困难题查看答案及解析
-
25 ℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是( )
A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(OH-)+c(B+)
B.若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9
C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+)
D.若将上述两溶液按体积比1∶1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-)
高二化学选择题困难题查看答案及解析
-
25℃时,用浓度均为0.1 mol·L-1的NaOH溶液和盐酸分别滴定体积均为20mL、浓度均为0.1 mol·L-1的HA溶液与BOH溶液。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说法中正确的是
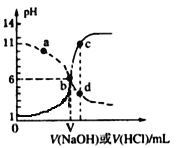
A. HA为弱酸,BOH为强碱
B. a点时,溶液中粒子浓度存在关系:c(B+) > c(Cl-) > c(OH-) > c(BOH)
C. c、d两点溶液混合后微粒之间存在关系:c(H+) = c(OH-) + c(BOH)
D. b点时两种溶液中水的电离程度相同,且V=20
高二化学单选题中等难度题查看答案及解析
-
25℃时,将浓度均为0.1 mol•L-1、体积分别为Va 和Vb 的HA 溶液与BOH 溶液按不同体积比混合,保持Va+Vb=100 mL,Va、Vb 与混合液的pH 的关系如图所示。下列说法正确的是
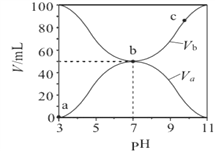
A. Ka(HA)=10-6 mol•L-1
B. b 点时,c(B+) = c(A-) = c(H+) = c(OH-)
C. c 点时,
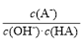 随温度升高而减小
随温度升高而减小D. a→c 过程中水的电离程度始终增大
高二化学单选题困难题查看答案及解析