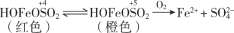-
某同学欲探究FeCl3溶液与NaHSO3溶液的反应,设计、完成实验并记录如下:
| 装置 | 反应时间 | 实验现象 |
| 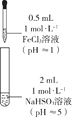
| 0~1 min | 产生红褐色沉淀Fe(OH)3,有刺激性气味气体SO2逸出 |
| 1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 |
| 30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
已知: Fe(OH)3+SO32-



 Fe2++SO42-
Fe2++SO42-
下列有关反应速率和化学平衡说法不正确的是
A.生成红色配合物的反应速率较快,红色配合物生成橙色配合物的速率较慢
B.增大溶液中SO32-浓度可以加速红褐色沉淀Fe(OH)3迅速溶解
C.O2的作用下,橙色HOFeOSO2浓度下降,平衡 不断正向移动
不断正向移动
D.30min时,若向该无色溶液中滴加少量FeCl3溶液,无明显现象
-
某实验小组对FeCl3分别与Na2SO3、NaHSO3的反应进行探究。
(甲同学的实验)
| 装置 | 编号 | 试剂X | 实验现象 |
| 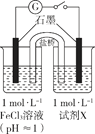
| I | Na2SO3溶液(pH≈9) | 闭合开关后灵敏电流计指针发生偏转 |
| II | NaHSO3溶液(pH≈5) | 闭合开关后灵敏电流计指针未发生偏转 |
(1)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。结合化学用语说明浓盐酸的作用:。
(2)甲同学探究实验I的电极产物______________。
①取少量Na2SO3溶液电极附近的混合液,加入______________,产生白色沉淀,证明产生了 。
。
②该同学又设计实验探究另一电极的产物,其实验方案为______________。
(3)实验I中负极的电极反应式为______________。
(乙同学的实验)
乙同学进一步探究FeCl3溶液与NaHSO3溶液能否发生反应,设计、完成实验并记录如下:
| 装置 | 编号 | 反应时间 | 实验现象 |
| 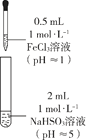
| III | 0~1 min | 产生红色沉淀,有刺激性气味气体逸出 |
| 1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 |
| 30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
(4)乙同学认为刺激性气味气体的产生原因有两种可能,用离子方程式表示②的可能原因。
① Fe3++3
 Fe(OH)3 +3SO2;②______________。
Fe(OH)3 +3SO2;②______________。
(5)查阅资料:溶液中Fe3+、 、OH-三种微粒会形成红色配合物并存在如下转化:
、OH-三种微粒会形成红色配合物并存在如下转化:
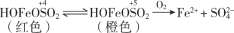
从反应速率和化学平衡两个角度解释1~30 min的实验现象:______________。
(6)解释30 min后上层溶液又变为浅红色的可能原因:______________。
(实验反思)
(7)分别对比I和II、II和III,FeCl3能否与Na2SO3或NaHSO3发生氧化还原反应和有关(写出两条)______________。
-
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表.
| 实验方案 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | A浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | B产生气体,可在空气中燃烧,溶液变成浅红色 |
| 3.钠与滴有酚酞试液的冷水反应 | C反应不十分强烈,产生的气体可以在空气中燃烧 |
| 4.镁带与2mol.L-1的盐酸反应 | D剧烈反应,产生可燃性气体 |
| 5.铝条与2mol.L-1的盐酸反应 | E生成白色胶状沉淀,既而沉淀消失 |
| 6.向AlCl3溶液滴加NaOH溶液至过量 | F生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:______;
(2)实验用品:仪器:①______②______③______④试管夹⑤镊子⑥小刀 ⑦玻璃片⑧砂纸等;药品:钠、镁带、铝条、2mol.L-1的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等.
(3)实验内容:(填写与实验方案相对应的实验现象)1______2______3______4______5______6______(用A-F表示);写出③的离子方程式______;
(4)实验结论:______.
-
(12分)某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
| 实验方案 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | A浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | B产生气体,可在空气中燃烧,溶液变成浅红色 |
| 3.钠与滴有酚酞试液的冷水反应 | C反应不十分强烈,产生的气体可以在空气中燃烧 |
| 4.镁带与2mol.L-1的盐酸反应 | D剧烈反应,产生可燃性气体 |
| 5.铝条与2 mol.L-1的盐酸反应 | E生成白色胶状沉淀,既而沉淀消失 |
| 6.向AlCl3溶液滴加NaOH溶液至过量 | F生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:________;
(2)实验用品:仪器:①________②________③________④试管夹⑤镊子⑥小刀 ⑦玻璃片⑧砂纸等;
药品:钠、镁带、铝条、2 mol.L-1的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等。
(3)实验内容:(填写与实验方案相对应的实验现象)
1________2________3________4________5________6________(用A-F表示);
写出③的离子方程式________;
(4)实验结论:________;
-
为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;②向上述稀硫酸中插入铜片,没有看到有气泡生成;③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。下列关于以上实验设计及现象的分析不正确的是( )
A. 实验①、②说明锌能与稀硫酸反应而铜不能
B. 实验③说明发生原电池反应时会加快化学反应速率
C. 实验③说明在该条件下铜可以与稀硫酸反应生成氢气
D. 实验④说明该原电池中铜为正极、锌为负极
-
为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,不正确的是
A.实验①、②说明锌能与稀硫酸反应而铜不能
B.实验③说明发生原电池反应时会加快化学反应速率
C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气
D.实验④说明该原电池中铜为正极、锌为负极
-
甲、乙两个实验小组利用 酸性溶液与
酸性溶液与 溶液反应研究影响反应速率的因素。
溶液反应研究影响反应速率的因素。
设计实验方案如下 实验中所用
实验中所用 溶液均已加入
溶液均已加入 :
:
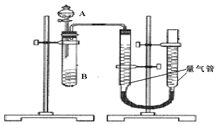
甲组:通过测定单位时间内生成 气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
| 序号 | A溶液 | B溶液 |
| ① |  溶液 溶液
|  溶液 溶液
|
| ② |  溶液 溶液
|  溶液 溶液
|
| ③ |  溶液 溶液
|  溶液和少量 溶液和少量
|
 该反应的离子方程式为 ______
该反应的离子方程式为 ______
 实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入
实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入 填“一次性”或“逐滴滴加”
填“一次性”或“逐滴滴加”
 完成该实验还需要 ______
完成该实验还需要 ______  填仪器名称
填仪器名称 ,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
乙组:通过测定 溶液褪色所需时间的多少来比较化学反应速率为了探究
溶液褪色所需时间的多少来比较化学反应速率为了探究 与
与 浓度对反应速率的影响,某同学在室温下完成以下实验
浓度对反应速率的影响,某同学在室温下完成以下实验
| 实验编号 | 1 | 2 | 3 | 4 |
| 水 | 10 | 5 | 0 | X |
| 
| 5 | 10 | 10 | 5 |
| 
| 5 | 5 | 10 | 10 |
| 时间 | 40 | 20 | 10 | --- |
 ______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
 号反应中,
号反应中, 的反应速率为 ______。
的反应速率为 ______。
 在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
| 时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 温度℃ | 25 | 26 | 26 | 26 | 
| 27 | 27 |
结合实验目的与表中数据,你得出的结论是 ______。
 从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______
从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______  填字母
填字母 。
。
A 硫酸钾  水
水  二氧化锰
二氧化锰  硫酸锰。
硫酸锰。
-
为研究硫酸铜的量对锌与稀硫酸反应氢气生成速率的影响,该同学设计了如下一系列实验。表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。下列说法正确的是
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4溶液 | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
A. V1=30,V6=10
B.反应一段时间后,实验A,E中的金属呈暗红色
C.加入MgSO4与Ag2SO4可以起与硫酸铜相同的加速作用
D.硫酸铜的量越多,产生氢气的速率肯定越快
-
(12分)某研究性课题小组对氢氧化钠溶液和稀盐酸中和反应的有关问题,进行了如下探究:
Ⅰ:(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如下图所示实验。

则X溶液是▲ 。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有25.00mL稀盐酸的锥形瓶中,用胶头滴管慢慢滴入氢氧化钠溶液,不断振荡,每加一滴溶液测定并记录一次溶液的pH值,直至氢氧化钠溶液过量。

①写出测定溶液pH值的操作方法:▲ ;
②上图中哪个图像符合该同学的记录▲ (填序号)。
(3)你认为甲、乙两位同学的实验中,▲ (填“甲同学”、“乙同学”、“甲乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由:▲ 。
Ⅱ:丙学生用0.100 mol·L-1氢氧化钠溶液滴定未知浓度的盐酸。他用移液管准确移取25.00mL未知浓度的盐酸置于一洁净的锥形瓶中,然后用0.100 mol·L-1的氢氧化钠溶液(指示剂为酚酞)进行滴定。滴定结果如下:
| 滴定次数 | 盐酸的体积/mL | NaOH溶液的体积/mL |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 2.00 | 20.20 |
| 2 | 25.00 | 1.02 | 21.03 |
| 3 | 25.00 | 0.20 | 20.20 |
(1) 根据以上数据计算出盐酸的物质的量浓度为▲ mol·L-1。
(2) 如果滴定的终点没有控制好,即NaOH溶液过量,溶液显深红色,如何补救?请设计实验方案。▲ 。
-
某研究性课题小组对氢氧化钠溶液和稀盐酸中和反应的有关问题,进行了如下探究:
Ⅰ:(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如下图所示实验.则X溶液是______.
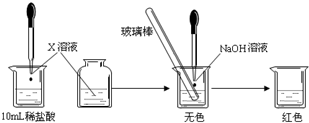
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应.在盛有25.00mL稀盐酸的锥形瓶中,用胶头滴管慢慢滴入氢氧化钠溶液,不断振荡,每加一滴溶液测定并记录一次溶液的pH值,直至氢氧化钠溶液过量.
①写出测定溶液pH值的操作方法:______;
②下图中哪个图象符合该同学的记录______(填序号).
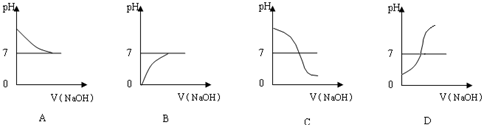
(3)你认为甲、乙两位同学的实验中,______(填“甲同学”、“乙同学”、“甲乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由:______.
Ⅱ:丙学生用0.100mol•L-1氢氧化钠溶液滴定未知浓度的盐酸.他用移液管准确移取.
25.00mL未知浓度的盐酸置于一洁净的锥形瓶中,然后用0.100mol•L-1的氢氧化钠溶液(指示剂为酚酞)进行滴定.滴定结果如下:
滴定次数 |
盐酸的体积/mL | NaOH溶液的体积/mL |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 2.00 | 20.20 |
| 2 | 25.00 | 1.02 | 21.03 |
| 3 | 25.00 | 0.20 | 20.20 |
(1)根据以上数据计算出盐酸的物质的量浓度为______mol•L-1.
(2)如果滴定的终点没有控制好,即NaOH溶液过量,溶液显深红色,如何补救?请设计实验方案.______.
Fe2++SO42-
 不断正向移动
不断正向移动