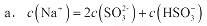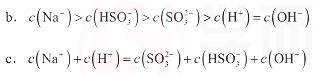-
化石燃料燃烧时会产生 进入大气形成酸雨,有多种方法可用于
进入大气形成酸雨,有多种方法可用于 的脱除。
的脱除。
 已知
已知 可参与如下热力学循环:
可参与如下热力学循环:

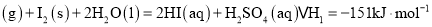



反应 的
的 ______
______
 碱性溶液吸收法。工业上常用碱性NaClO废液吸收
碱性溶液吸收法。工业上常用碱性NaClO废液吸收 ,反应原理为:
,反应原理为: ,为了提高吸收效率,常用
,为了提高吸收效率,常用  作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对
作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对 的吸收。该催化过程如下图所示:
的吸收。该催化过程如下图所示:
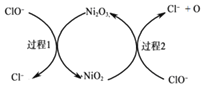
 过程1的离子方程式是
过程1的离子方程式是 ,过程2的离子方程式为______。
,过程2的离子方程式为______。
 也可用于脱硫,且脱硫效果比NaClO 更好,原因是______。
也可用于脱硫,且脱硫效果比NaClO 更好,原因是______。
 溶液、氨水等碱性溶液吸收法。已知
溶液、氨水等碱性溶液吸收法。已知 时,含硫物种
时,含硫物种 即水溶液中
即水溶液中 、
、 、
、 随pH变化如图1所示,脱硫效率随pH变化如图2所示。
随pH变化如图1所示,脱硫效率随pH变化如图2所示。
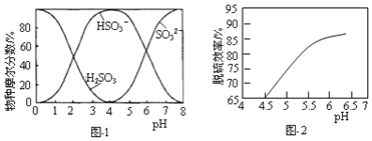
①当用 溶液吸收
溶液吸收 至溶液的pH为4时,发生反应的离子方程式是______。
至溶液的pH为4时,发生反应的离子方程式是______。
②当用氨水吸收 至溶液的
至溶液的 时,
时, 与溶液中存在的含硫物种之间的关系是
与溶液中存在的含硫物种之间的关系是 ______。
______。
③由实验测得氨水脱除 时,脱硫效率随pH的变化如图
时,脱硫效率随pH的变化如图 所示。在
所示。在 ,pH较小时脱硫效率低的可能原因是______;实际工艺中,吸收液的pH应控制在一定范围内,pH不宜过大的原因是______。
,pH较小时脱硫效率低的可能原因是______;实际工艺中,吸收液的pH应控制在一定范围内,pH不宜过大的原因是______。
-
化石燃料燃烧时会产生 SO2进入大气,有多种方法可用于 SO2的脱除。
(1)NaClO 碱性溶液吸收法。工业上可用 NaClO 碱性溶液吸收SO2。
①反应离子方程式是__________________________________________。
②为了提高吸收效率,常用 Ni2O3作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对SO2的吸收。该催化过程的示意图如图所示:
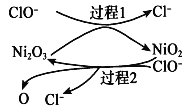
a.过程1的离子方程式是Ni2O3+ClO- =2NiO2 +Cl-,则过程2的离子方程式____________。
b.Ca(ClO)2也可用于脱硫,且脱硫效果比NaClO更好,原因是________________。
(2)碘循环工艺也能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:
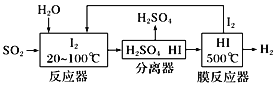
则碘循环工艺的总反应为:___________________________________________。
-
下列有关硫及其化合物说法不正确的是 ( )
A.大气中的硫可能以酸雨的形式进入土壤
B.煤和石油中的硫燃烧生成三氧化硫进入大气
C.化石燃料中的硫来自于形成化石燃料的生物体
D.煤和石油燃烧产生的颗粒物可能是导致雾霾的成因之一
-
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2,
(1)用化学方程式表示SO2形成硫酸型酸雨的反应: 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 。
(3)吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
| n(SO32﹣):n(HSO3﹣) | 99:1 | 1:1 | 1:99 |
| pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显 性。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母): 。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)= c(SO32-)+ c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如图:
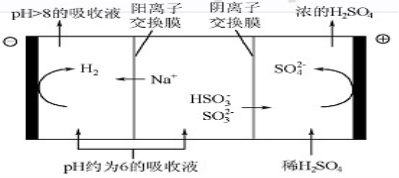
①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理: 。
-
(10分)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示S形成硫酸酸雨的反应方程式 , 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________。
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣),n(HSO3﹣)变化关系如下表:
| n(SO3²﹣):,n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显 性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
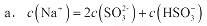
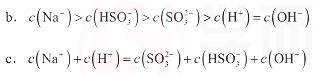
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
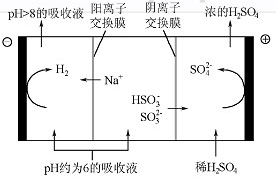
①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用。简述再生原理:
。
-
直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:______.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是______.
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显______性,用化学平衡原理解释:______.
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):______.
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
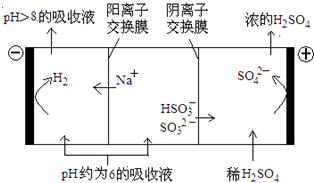
(4)当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:
①HSO3-在阳极放电的电极反应式是______.
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理:______.
-
右图关于碳循环的说法不正确的是:
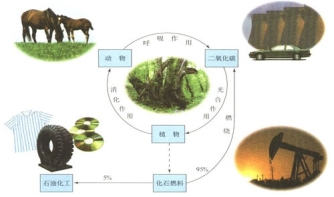
A.氧元素也参与了碳循环
B.绿色植物可吸收大气中CO2
C.大量燃烧化石燃料会造成温室效应
D.呼吸和光合作用时碳元素均被氧化
-
下列有关环境保护与绿色化学的叙述不正确的是( )
A. 形成酸雨的主要物质是硫的氧化物和氮的氧化物
B. 大气污染物主要来自化石燃料燃烧和工业生产过程产生的废气
C. 绿色化学的核心就是如何对被污染的环境进行无毒无害的治理
D. 水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的
-
【化学--选修化学与技术】
在工厂中常使用煤作燃料,但煤燃烧后会产生有害的SO2,按“循环经济”的模式,就是要将SO2收集起来,把它变为有用的东西.
(1)向大气中过量排放SO2将会形成酸雨污染.正常雨水的pH约为________.
(2)三氧化硫通入浓氨水,可得到一种肥料,写出反应的化学的方程式:________
(3)某空气监测是根据SO2和溴水的定量反应来测定SO2的含量.该反应的化学方程式为________.反应后溶液的pH________(填“变大”、“变小”或“不变”).若每次取样的空气为200mL,通入足量的溴水中,测得平均有2.408×1018个电子转移,则SO2的含量为________ mg•L-1,若规定空气中SO2含量不得超过0.02mg•L-1,则样气是否符合大气的质量标准________(填“符合”或“不符合”).
(4)近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法:
第一步是用Na2SO3水溶液吸收SO2;
第二步是加热吸收液,使之重新生成Na2SO3,同时得到含高浓度SO2水蒸气副产品,写出上述两步反应的化学方程式:
①________.
②________.
-
直接排放含SO2,的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2在钠碱循环法中,用Na2SO3溶液作为吸收液,吸收液吸收SO2的过程中,pH随n(SO32-): n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
(1)上表判断NaHSO3溶液显___________性,用化学平衡原理解释____________________________________________________________________________
(2)当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a. c(Na+ )=" 2c(" SO32-) + c( HSO3-)
b. c(Na+ )> c( HSO3-)>c( SO32-) >c(H+)>c(OH-)
c. c(Na+ )+ c(H+)="c(" HSO3-)+c( SO32-) +c(OH-)
当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
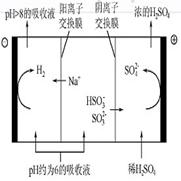
(3)HSO3-在阳极放电的电极反应式是_________________________________________
(4)当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
________________________________________________________________________
进入大气形成酸雨,有多种方法可用于
的脱除。
已知
可参与如下热力学循环:
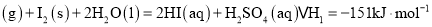
的
______
碱性溶液吸收法。工业上常用碱性NaClO废液吸收
,反应原理为:
,为了提高吸收效率,常用
作为催化剂。在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对
的吸收。该催化过程如下图所示:

过程1的离子方程式是
,过程2的离子方程式为______。
也可用于脱硫,且脱硫效果比NaClO 更好,原因是______。
溶液、氨水等碱性溶液吸收法。已知
时,含硫物种
即水溶液中
、
、
随pH变化如图1所示,脱硫效率随pH变化如图2所示。

溶液吸收
至溶液的pH为4时,发生反应的离子方程式是______。
至溶液的
时,
与溶液中存在的含硫物种之间的关系是
______。
时,脱硫效率随pH的变化如图
所示。在
,pH较小时脱硫效率低的可能原因是______;实际工艺中,吸收液的pH应控制在一定范围内,pH不宜过大的原因是______。