某温度下,弱酸H2A溶液中,存在H2A、HA-和A2-三种形态的粒子,其物质的量分数δ[δ(X)=]随溶液pH变化的关系如图所示,下列说法错误的是
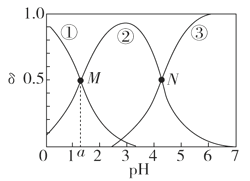
A.pH>4的溶液中,δ(A2-)=,
B.M点对应的溶液中水的电离程度小于N点
C.若图中a为1.2,则lg [Ka1(H2A)]=-1.2
D.曲线②代表的粒子是HA-
高二化学单选题困难题
某温度下,弱酸H2A溶液中,存在H2A、HA-和A2-三种形态的粒子,其物质的量分数δ[δ(X)=]随溶液pH变化的关系如图所示,下列说法错误的是

A.pH>4的溶液中,δ(A2-)=,
B.M点对应的溶液中水的电离程度小于N点
C.若图中a为1.2,则lg [Ka1(H2A)]=-1.2
D.曲线②代表的粒子是HA-
高二化学单选题困难题
某温度下,弱酸H2A溶液中,存在H2A、HA-和A2-三种形态的粒子,其物质的量分数δ[δ(X)=]随溶液pH变化的关系如图所示,下列说法错误的是

A.pH>4的溶液中,δ(A2-)=,
B.M点对应的溶液中水的电离程度小于N点
C.若图中a为1.2,则lg [Ka1(H2A)]=-1.2
D.曲线②代表的粒子是HA-
高二化学单选题困难题查看答案及解析
室温下,0.1 mol·L-1的某二元酸H2A溶液中,可能存在的含A粒子(H2A、HA-、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是( )

A. pH=5时,在NaHA和Na2A的混合溶液中:c(HA-)∶c(A2-)=1∶100
B. H2A的电离方程式:H2AH++HA-
C. 等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为c(Na+)>c(HA-)>c(A2-)
D. Na2A溶液必存在c(OH-)=c(H+)+c(HA-)+2c(H2A),各粒子浓度均大于0
高二化学单选题困难题查看答案及解析
常温下0.lmol·L-1的H2A溶液中H2A、HA-、A2-三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是
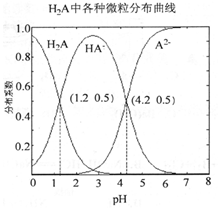
A. H2A为二元弱酸,其电离方程式为:H2AH++HA-、HA-
H++A2-
B. 在0.lmol•L-1NaHA溶液中,各离子浓度大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C. 在pH=1.2时,向H2A溶液中加入一定体积的0.lmo l·L-1的NaOH溶液使pH=4.2,则c(A2-)、c(HA-)、c(H2A)之和不变
D. 在 pH=3.0 时:c(A2-)+ c(HA-)<0.lmo l·L-1
高二化学选择题困难题查看答案及解析
H2R为二元弱酸,向一定体积的0.1mol/L的H2R溶液中逐滴加入一定浓度的NaOH溶液,溶液中不同形态的粒子(H2R、HR-、R2-)的物质的量分数a(X)随pH的变化曲线如图所示[a(X)=c(X)/[c(H2R)+c(HR-)+c(R2-)]]。下列说法错误的是
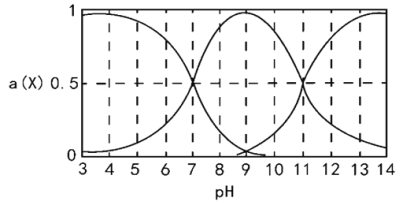
A. 常温下,K2(H2R)=1.0×10-11
B. 常温下,HR-在水中的电离程度大于其水解程度
C. pH=9时, c(Na+)>c(HR-)+2c(R2-)
D. pH=7时,c(H2R)=c(HR-)
高二化学单选题中等难度题查看答案及解析
25℃时,改变0.1mol·L -1二元弱酸H2A溶液的pH,溶液中的H2A 、HA-、 A2-的物质的量分数(X)随pH的变化如图所示[已知
(X)=
]。
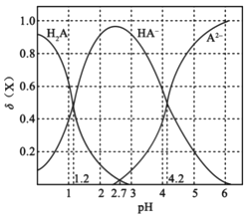
下列叙述错误的是
A. Ka1(H2A)的数量级为10-2
B. pH=4.2时,c(HA-)=c(A2-)>c(H+)
C. NaHA溶液中,HA-的电离平衡常数大于HA-的水解平衡常数
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+)则(H2A)和
(HA-)一定相等
高二化学null困难题查看答案及解析
改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知]。 下列叙述错误的是( )

A. pH=1.2时,c(H2A)=c(HA-) B. lg[K2(H2A)]=-4.2
C. pH=2.7时, c(HA-)>c(H2A)=c(A2-) D. pH= 4.2时,c(HA-)=c(A2-)=c(H+)
高二化学单选题困难题查看答案及解析
改变0.1mol/L二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数随pH的变化如图所示已知[
]。
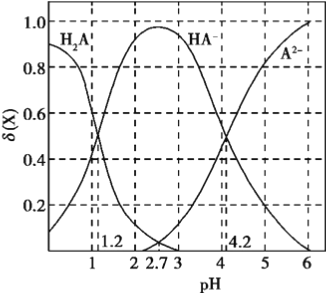
下列叙述错误的是
A. lg[K2(H2A)]=-4.2
B. pH=4.2时,c(HA-) = c(A2-) = c(H+)
C. pH=2.7时,c(HA-) >c(H2A)= c(A2-)
D. pH=1.2时,c(H2A)=c(HA-)
高二化学单选题困难题查看答案及解析
改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知:δ(X)=]。下列叙述错误的是
A. K1(H2A)=10-1.2
B. pH=2.7时,c(H2A)+c(HA-)+c(A2-)=0.1 mol·L-1
C. pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D. pH=4.2时,c(HA-)=c(A2-)=c(H+)
高二化学单选题中等难度题查看答案及解析
改变0.1mol·L-1二元弱酸H2A溶液的pH, 溶液中的H2A、HA-、A2-的物质的量分数∮(X)随pH的变化如图所示[已知:∮(X)= ]。下列叙述错误的是( )
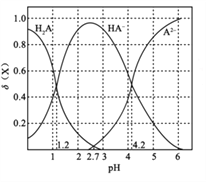
A. pH=1.2 时,c (H2A)=c(HA-) B. lg[K2(H2A)]=-4.2
C. pH=2.7时,c(HA-) >c(H2A)=c(A2-) D. pH=4.2时,c (HA-)=c(A2-)=c(H+)
高二化学单选题困难题查看答案及解析
改变0.1mol•L—1二元弱酸H2A溶液的pH,溶液中的H2A、HA—、A2—的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=c(x)/(c(H2A)+c(HA—)+c(A2—)])。下列叙述正确的是
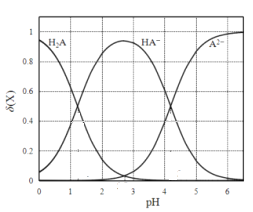
A. Ka2(H2A)的数量级为10-4
B. NaHA溶液中,HA-的水解能力小于HA-的电离能力
C. 在含H2A、HA-和A2-的溶液中,加入少量NaOH固体,δ(HA-)一定增大
D. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中δ(HA-)=δ(A2-)
高二化学单选题中等难度题查看答案及解析