-
Ⅰ.已知某无色溶液中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种,为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,往①的上层溶液中加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。
回答下列问题:
(1)一定不存在的离子为:____________;
(2)需要通过焰色反应来确定是否存在Na+吗?_________(填“是”或“否”),请简要说明原因_________。
Ⅱ.电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
(1)FeCl3溶液与金属铜发生反应的化学反应方程式是__________________ ;
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:
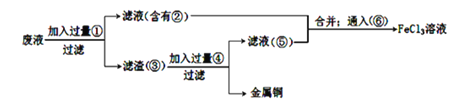
上述实验中加入或生成的有关物质的化学式为②_________ ; ④____________;
若向溶液②中加入氢氧化钠溶液,其实验现象为______________________ 。
高一化学综合题中等难度题查看答案及解析
-
某无色溶液中可能含有Na+、NH4+、Ba2+ 、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种,为检验其中含有的离子,进行如下实验:
①取10 mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体。下列关于原溶液的说法正确的是
A. 肯定存在NH4+、Cl-、Br- B. 是否存在Na+需要通过焰色反应来确定
C. SO42-、SO32-至少含有一种 D. 肯定不存在Ba2+、Cu2+、SO32-、CO32-
高一化学选择题中等难度题查看答案及解析
-
某溶液中含有CO32-、SO42-、 NH4+和M离子的物质的量之比为1:2:4:2,则离子M可能是
A. H+
B. K+
C. C1- D. Ba2+
高一化学选择题中等难度题查看答案及解析
-
已知:NH4+ + OH- == NH3 ↑+ H2O现有一混合物的水溶液,可能含有以下离子中的若干种: K+、NH4+、Ba2+、CO32-、Cl-、SO42-。现取两份各200 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36 g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,以下推测正确的是
A. 一定存在NH4+、CO32-、SO42-,一定不存在Ba2+ 、Cl-
B. 一定存在NH4+、CO32-、Cl-、SO42-,可能存在K+
C. c(SO42-)=0.2mol·L-1,c(NH4+)> c(SO42-)
D. 若溶液中存在NH4+、Cl-、CO32-、SO42-、K+五种离子,则c(K+)>0.2mol·L-1
高一化学单选题中等难度题查看答案及解析
-
已知:NH4+ + OH- =NH3↑+ H2O。现有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Ba2+、CO32-、Cl-、SO42-。现取两份200 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36 g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,以下推测正确的是
A. 一定存在NH4+、CO32-、SO42-,一定不存在Ba2+ 、Cl-
B. 一定存在NH4+、CO32-、Cl-、SO42-,可能存在K+
C. c(SO42-)=0.2mol·L-1,c(NH4+)> c(SO42-)
D. 若溶液中存在NH4+、Cl-、CO32-、SO42-、K+五种离子,则c(K+)>0.2mol·L-1
高一化学单选题中等难度题查看答案及解析
-
某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Na+、CO32﹣、SO42﹣、SiO32﹣、NO3﹣中的一种或几种离子,取该溶液进行实验,其现象及转化如下图所示。

请回答下列问题:
(1)由整体的实验过程可判断溶液X中一定不存在的阴离子有______。
(2)产生气体A的离子方程式为____________。
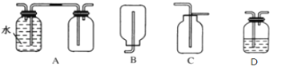
(3)在实验室中收集气体A,可选择如图装置中的______。
(4)写出④反应中生成溶液H的离子方程式____________。
(5)对不能确定是否存在的离子,请简述检测实验方案__________。
高一化学实验题困难题查看答案及解析
-
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:(已知:NH4++OH- = NH3↑+H2O)
第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热后,收集到0.08 mol气体。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g.。根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl- :
(2)由第二份进行的实验得知混合物中应含有 离子,其物质的量浓度为 。
(3)由第三份进行的实验可知12.54g沉淀的成分为 ,计算形成该沉淀的原混合物中各离子的物质的量 。
(4)综合上述实验,你认为以下结论正确的是
A.该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K+) ≥0.04mol
B.该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl-
C.该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl-
D.该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl-
高一化学填空题中等难度题查看答案及解析
-
某无色透明溶液,可能含有下列离子:Mg2+、Al3+、Fe3+、Ba2+、H+、NH4+、SO42-、HCO3-、Cl-、CO32-。取该溶液进行如下实验:
①取溶液少许,滴入AgNO3溶液产生白色沉淀;
②另取溶液少许,滴入BaCl2溶液产生白色沉淀,加入足量稀硝酸沉淀不溶解;
③另取原溶液500mL,加入过氧化钠固体,产生的沉淀的物质的量与加入过氧化钠的物质的量的关系如下图所示。
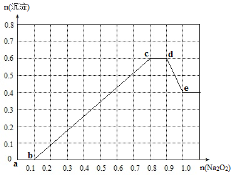
根据实验现象和数据分析,回答下列问题:
(1)de段发生的反应的离子方程式是 ;
(2)溶液中肯定存在的离子是 (用离子符号表示);
(3)溶液中可能存在的离子是 (用离子符号表示);
(4)原溶液中金属阳离子的浓度分别为 ;
(5)请在答题卡对应图上画出加入过氧化钠从0~1.1mol时,产生气体的物质的量随加入过氧化钠物质的量变化的曲线(假设生成的气体全部逸出)。
高一化学推断题中等难度题查看答案及解析
-
某待测液可能含有K+、NH4+、Ba2+、Cl-、CO32-、SO42-中的若干种离子.分别进行下述实验,以确定该溶液的组成.
实验步骤 实验现象 实验结论 ①取少量待测液,加入AgNO3溶液 有白色沉淀生成 待测液中Cl-离子______
(填“一定存在”、“一定不存在”或“不能确定”)②取100mL待测液,加足量浓NaOH溶液并加热 收集到气体约1.12L
(已折算成标准状况下的体积)反应的离子方程式是
______
检出离子的物质的量浓度是
______③取100mL待测液,加足量BaCl2溶液后,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 第一次称量白色沉淀质量为6.27g,第二次称量白色沉淀质量为2.33g - 实验分析:根据实验①~③,可判断待测液中一定存在的离子除K+离子外,还有的离子是______.
判断K+离子存在的理由是______.高一化学解答题中等难度题查看答案及解析
-
今有一混合溶液,只可能含有以下离子中的若干种:Na+、NH4+、Cl-、Ba2+、CO32-、SO42-、OH-,现取三份各100 mL的溶液进行如下实验(每步实验均仅进行完全),根据实验内容填写相应结论:
(1)第一份加足量NaOH溶液加热后,收集到0.68gNH3气体,原溶液中一定不含有________;
(2)第二份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
综合以上实验,原溶液中一定含有________、________,一定不含有________;
(3)第三份加入AgNO3溶液有沉淀产生。
原溶液中还一定存在______,可能存在_______(若没有,两空均可不填)
高一化学实验题中等难度题查看答案及解析