-
已知A、B、C、D、E、F是原子序数依次增大的六种短周期主族元素,A原子最外层电子数是次外层电子数的2倍,C是地壳中含量最多的元素,D是短周期原子半径最大的元素,E原子最外层电子数与C原子最外层电子数相等。回答下列问题:
(1)C元素在周期表中的位置是______________。
(2)从原子结构的角度解释最高价氧化物对应的水化物的酸性F的大于E的原因_______。
(3)E元素的低价氧化物与D元素的最高价氧化物对应的水化物反应生成的酸式盐,溶于水,溶液中所有离子由大到小的排列顺序是________。
(4)用H2或CO催化还原NO可以达到消除污染的目的。
已知:2NO (g)=N2 (g) + O2 (g) △H=﹣180.5kJ•mol﹣1
2H2O (l)=2H2 (g) + O2 (g) △H= + 571.6kJ•mol﹣1
则H2 (g)与NO (g)反应生成N2 (g)和H2O (l)的热化学方程式是_________。
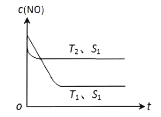
(5)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。如图表示在其他条件不变时,反应2NO (g) + 2CO(g)⇌2CO2 (g) + N2 (g)中,NO的浓度c (NO)随温度 (T)、催化剂表面积 (S)和时间 (t)的变化曲线。该反应的△H____0 (填“>”或“<”)。
(6)实验室制取F的单质时,常含有少量HCl气体,可用_________(试剂)除去HCl,请用平衡移动的原理解释原因:________。
-
A、B、C、D、E、F均为短周期元素,其原子序数依次增大.已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素.根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为______
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式______ CO2↑+4NO2↑+2H2O
-
A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为________
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式________。
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为___________________________________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)_______________。
(4)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:正极的电极反应式是___________________________________。
(5)已知:2CD2(g)  C2D4(g);△H<0。在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
C2D4(g);△H<0。在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
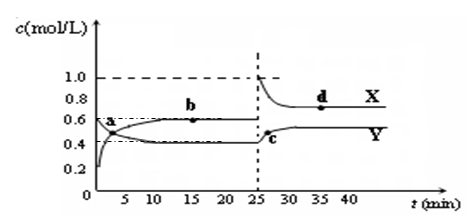
① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。
② 25 min时,增加了_______(填物质的化学式)________mol。
③ a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______(填字母)。
-
已知M、W、X、Y、Z是短周期中原子序数依次增大的5种主族元素,其中W、Z同族,M原子的最外层电子数是电子层数的3倍,元素X在同周期的主族元素中原子半径最大,Y是地壳中含量最多的金属元素。下列说法中正确的是
A.气态氢化物稳定性最强的是HZ
B.Y的单质可通过电解熔融的Y与Z形成的化合物获得
C.原子半径由小到大的顺序为rW<rM<rY
D.X的焰色反应通过蓝色的钴玻璃呈紫色
-
已知M、W、X、Y、Z是短周期中原子序数依次增大的5种主族元素,其中W、Z同族,M原子的最外层电子数是电子层数的3倍,元素X在同周期的主族元素中原子半径最大,Y是地壳中含量最多的金属元素。下列说法中正确的是
A.气态氢化物稳定性最强的是HZ
B.原子半径由小到大的顺序为W<M<Y
C.室温下,可用Y的容器盛装稀硝酸
D.X的单质可通过电解XZ的水溶液获得
-
已知M、W、X、Y、Z是短周期中原子序数依次增大的5种主族元素,其中W、Z同族,M原子的最外层电子数是电子层数的3倍,元素X在同周期的主族元素中原子半径最大,Y是地壳中含量最多的金属元素。下列说法中正确的是
A.气态氢化物稳定性最强的是HZ
B.原子半径由小到大的顺序为:rW<rM <rY
C.室温下,可用Y的容器盛装稀硝酸
D.X的单质可通过电解XZ的水溶液获得
-
X、Y、Z、M 是原子序数依次增大的四种短周期元素,已知X 原子的核外电子数等于其所在周期数,Y 原子的最外层电子数是内层电子数的2倍,M 是地壳中含量最高的金属元素,Z 和M 形成的化合物在盐酸和氢氧化钠溶液中均能溶解。下列说法中正确的是
A. 金属M 制品具有较强的抗腐蚀能力,说明M 的金属活动性较差
B. X、Y、Z 三种元素可以形成X2YZ、X2YZ2、X2YZ3等多种化合物
C. X、Z 可以形成原子个数之比为1:1和2 :1的两种离子化合物
D. X 和Y 形成化合物的熔、沸点一定低于Y 和Z 形成的化合物
-
(14分)A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为 。
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式 。FD2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为_____。
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为____________________________________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)_______________。
(4)C2A4─空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:正极的电极反应式是______________;负极的电极反应式为 。
-
(8分)A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为________。
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式________。 FB2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为__________________________。
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为__________________________________________; 由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)____________________________________________________________________。
(4)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时,负极的电极反应式为__________________________________.。
-
已知A、B、C、I)是短周期中原子序数依次增大的四种主族元素。A:在常温下呈气态,B原子最外层电子数是其电子层数的2倍,C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素。下列说法正确的是
A. A、C的氧化物均含离子键
B. c离子的半径小于D离子的半径
C. A、B可形成多种原子个数比为1:1的化合物D含D元素的盐溶液只能显碱性

