-
酱油在使用及储藏过程中颜色会变深,逐渐降低品质。实验小组通过实验研究温度、氧气、光照3个因素对酱油颜色的影响。
(查阅资料)① 通过色差仪检测L*值可监控酱油颜色变化,酱油颜色越深,L*值越小。
② 保鲜瓶具有的特点是挤出盛放的物质后,空气不会进入。
(实验准备)
将等量样品(同品牌、同批次、初始L*值为43.82的酱油)分装到500 mL的不同容器中,密封。
(进行实验)
实验1:将装有样品的多个透明玻璃瓶置于不同温度的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。
| 编号 | 温度 | 15天 | 30天 | 45天 |
| 1-1 | 5 ℃ | 43.77 | 43.53 | 42.91 |
| 1-2 | 28 ℃ | 43.71 | 43.19 | 42.85 |
| 1-3 | 45 ℃ | 43.67 | 42.55 | 40.89 |
实验2:将装有样品的两个容器置于28 ℃的恒温箱中。每15天,分别倒出100 mL酱油,剩余样品放回恒温箱。用色差仪检测倒出样品的L*值,结果如下。
| 编号 | 容器 | 15天 | 30天 | 45天 |
| 2-1 | 透明玻璃瓶 | 43.45 | 42.36 | 41.30 |
| 2-2 | 透明保鲜瓶 | 43.72 | 42.98 | 42.53 |
实验3:将装有样品的多个容器置于28 ℃的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。

(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2的目的是_____。
(3)实验3欲研究光照对酱油颜色的影响,应选用的容器是_____。
(4)家庭常使用透明玻璃瓶盛放酱油。解释“在相同时间内,使用过的酱油比未开封的酱油颜色深”可依据的实验是_____(填编号)。
(反思与评价)
(5)结合本实验,你对使用或储藏酱油的建议是_____。
(6)酱油在酿造过程中,有时会产生过量的铵盐(如NH4Cl)影响酱油的口感。可用碳酸钠除去铵盐,原理如下,补全该反应的化学方程式。Na2CO3 + 2NH4Cl === 2NaCl + 2NH3↑ + H2O +_____
-
课外小组研究“影响H2O2 生成O2反应速率的因素”的课题。通过查阅资料,他们提出如下猜想。
(提出猜想)催化剂和反应物浓度都会影响H2O2 生成O2 的反应速率
(实验过程)实验装置如图:
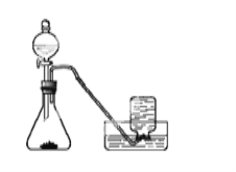
实验操作:检查装置的气密性良好。 将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2 50 mL | 5%H2O2 | 3%H2O250 mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105 s | 45s | 78 s |
(1)实验②中加入H2O2溶液的体积为__________mL;
(2)充分反应后,将实验②中剩余物质里的MnO2提取的方法是_____________;
(实验结论)该探究过程得出的结论是 ____________________________________;
(实验反思) H2O2在常温加入MnO2 后反应速率加快。小敏提出,为了更好的证明二氧化锰是否对H2O2 生成O2的反应速率有影响,还应该增加一组对比实验:该对比实验选用的药品和用量分别为________;小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象,出现这种实验结果的原因可能是:_______________________________________________。
-
课外小组研究“影响H2O2生成O2反应速率的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2 的反应速率
【实验过程】实验装置如图:
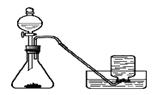
实验操作:检查装置的气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2 50 mL | 5%H2O2________ | 3%H2O250 mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105 s | 45s | 78 s |
(1)实验②中加入H2O2溶液的体积为________mL;
(2)充分反应后,将实验②中剩余物质里的MnO2提取的方法是________;
【结论】该探究过程得出的结论是 ________;
【反思】 H2O2在常温加入MnO2 后反应速率加快。小敏提出,为了更好的证明二氧化锰是否对H2O2生成O2的反应速率有影响,还应该增加一组对比实验。该实验选用的药品和用量为________;
【实验拓展】小敏用收集的气体进行氧气的性质实验。
(1)铁丝在氧气中燃烧,其反应的化学方程式为________;
(2)小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象。造成这种结果的可能原因是________。
-
课外小组研究“影响H2O2 生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
【提出猜想】催化剂和反应物浓度都会影响H2O2 生成O2的反应速率
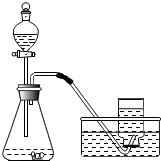
【实验过程】实验装置如图:
实验操作:检查装置的气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O250mL | 5%H2O2________ | 3%H2O250mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105s | 45s | 78s |
(1)实验②中加入H2O2溶液的体积为________mL;
(2)充分反应后,将实验②中剩余物质里的MnO2提取的方法是________;
【结论】该探究过程得出的结论是________;
【反思】H2O2在常温加入MnO2后反应速率加快.小敏提出,为了更好的证明二氧化锰是否对H2O2 生成O2的反应速率有影响,还应该增加一组对比实验.该实验选用的药品和用量为________;
【实验拓展】小敏用收集的气体进行氧气的性质实验.
(1)铁丝在氧气中燃烧,其反应的化学方程式为________;
(2)小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象.造成这种结果的可能原因是________.
-
(8分)某课外小组研究“影响H2O2 生成O2快慢的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2 生成O2 的快慢
【实验过程】实验装置图如下:
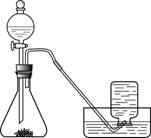
实验操作:检查装置气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2 100 mL | 5%H2O2 | 3%H2O2100 mL |
| 加入固体 | 0.5 g氯化钠固体 | 0.5 g二氧化锰 | |
| 收集气体的时间 | 165 s | 46s | 80 s |
(1)H2O2溶液和二氧化锰制取氧气的化学方程式为________。
(2)实验②中加入H2O2的体积为________mL。
(3)实验③中加入的固体和用量为________。
【结论】该探究过程得出的结论是 ________。
【反思】H2O2在常温下分解缓慢,加入MnO2 后反应明显加快。小红提出,为了更好的证明二氧化锰 和氯化钠是否对H2O2 生成O2快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为________。
【实验拓展】小红用收集的气体进行氧气的性质实验。
(1)检验氧气的方法是________。
(2)小红发现用该气体进行氧气的性质实验,现象都不明显。造成这种结果的原因是________。
-
某课外小组研究“影响H2O2 生成O2反应速率的因素”的课题。通过查阅资料,他们提出如下猜想。
(提出猜想)催化剂和反应物浓度都会影响H2O2 生成O2 的反应速率
(实验过程)实验装置如下图:
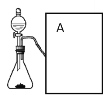
实验操作:检查装置的气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录:
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 反应物 | 5%H2O2 50 mL | 5%H2O2 __________ | 3%H2O250 mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105 s | 45s | 78 s |
①实验Ⅱ中加入H2O2溶液的体积为_______mL;
②充分反应后,将实验Ⅱ中剩余物质里的MnO2提取的方法是______;
(结论)该探究过程得出的结论是_____
③此实验中A处宜采用的气体收集方法是 _________ 。
-
某课外小组研究“影响H2O2生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
提出猜想:催化剂和反应物浓度都会影响H2O2生成O2的反应速率
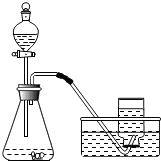
实验过程:实验装置如图:
实验操作:检查装置的气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 反应物 | 5%H2O250mL | 5%H2O2______ | 3%H2O250mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105s | 45s | 78s |
①实验Ⅱ中加入H2O2溶液的体积为______mL;
②充分反应后,将实验Ⅱ中剩余物质里的MnO2提取的方法是______;
结论:该探究过程得出的结论是______;
反思:H2O2在常温加入MnO2后反应速率加快.小敏提出,为了更好的证明二氧化锰是否对H2O2 生成O2的反应速率有影响,还应该增加一组对比实验.该实验选用的药品和用量为______;
实验拓展:小敏用收集的气体进行氧气的性质实验.
①铁丝在氧气中燃烧,其反应的化学方程式为______
-
某课外小组研究“影响H2O2生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
提出猜想:催化剂和反应物浓度都会影响H2O2生成O2的反应速率
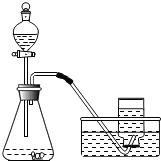
实验过程:实验装置如图:
实验操作:检查装置的气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 反应物 | 5%H2O250mL | 5%H2O2______ | 3%H2O250mL |
| 加入固体 | 0.5gCuO | 0.5gMnO2 | 0.5gMnO2 |
| 收集等体积O2所需时间 | 105s | 45s | 78s |
①实验Ⅱ中加入H2O2溶液的体积为______mL;
②充分反应后,将实验Ⅱ中剩余物质里的MnO2提取的方法是______;
结论:该探究过程得出的结论是______;
反思:H2O2在常温加入MnO2后反应速率加快.小敏提出,为了更好的证明二氧化锰是否对H2O2 生成O2的反应速率有影响,还应该增加一组对比实验.该实验选用的药品和用量为______;
实验拓展:小敏用收集的气体进行氧气的性质实验.
①铁丝在氧气中燃烧,其反应的化学方程式为______
-
(2011•海淀区二模)某课外小组研究“影响H2O2 生成O2快慢的因素”的课题.通过查阅资料,他们提出如下猜想.
[提出猜想]催化剂和反应物浓度都会影响H2O2 生成O2的快慢
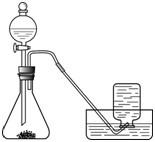
[实验过程]实验装置图如图所示:
实验操作:检查装置气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
| 实验编号 | ① | ② | ③ |
| 反应物 | 5%H2O2100mL | 5%H2O2 | 3%H2O2100mL |
| 加入固体 | 0.5g氯化钠固体 | 0.5g二氧化锰 | |
| 收集气体的时间 | 165s | 46s | 80s |
(1)H2O2溶液和二氧化锰制取氧气的化学方程式为______ 2H2O+O2↑
-
某化学兴趣小组对用过氧化氢分解生成水和氧气的实验条件进行探究。
【提出问题】哪些因素可能影响该反应的反应速率?
【查阅资料】影响化学反应速率的因素:
①主要因素:反应物本身的性质;
②外界因素:温度,浓度,压强,催化剂,光,激光,反应物颗粒大小,反应物之间的接触面积和反应物状态;
③另外,x射线,γ射线也会影响化学反应速率。
【作出猜想】下面是小组内三位同学所做的猜想,请你完成小丽的猜想。
小红同学:H2O2溶液的浓度可能影响该反应的反应速率。
小明同学:催化剂(MnO2)的用量可能影响该反应的反应速率.
小丽同学:我认为_______________可能影响该反应的反应速率。
【实验验证】
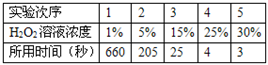
⑴.小红同学的实验是:每次均取10mL30%的H2O2溶液,然后稀释成不同浓度的溶液进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如表:(其他实验条件:温度、催化剂用量等均相同)
请你分析回答:H2O2溶液的浓度对过氧化氢分解制氧气反应速率有什么影响?
__________________
⑵.小明同学的实验是:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如表:(其他实验条件:过氧化氢溶液浓度、温度等均相同)
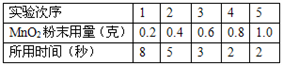
请你分析回答:该反应的化学方程式为_________________;催化剂MnO2的用量对过氧化氢分解制氧气反应速率有什么影响?__________
⑶.如果你是小丽同学,在验证你的猜想时,你的实验方案是:______________________。
【反思与交流】通过该探究实验,你还想探究的问题或还想学习的知识是______________________。










