-
X、Y、Z、W、H为原子序数依次增大的五种短周期元素,它们满足以下条件:元素周期表中,Z与Y相邻,Z与W也相邻; Y、Z和W三种元素的原子最外层电子数之和为17;H的单质常温下为黄绿色气体。请填空:
(1)Z、W、H简单阴离子的半径由大到小的顺序是____________(用离子符号表示)
(2)H的单质通入W的氢化物的水溶液中,可观察到有淡黄色沉淀生成,该现象说明H与W单质的氧化性强弱顺序为____________(用化学式表示)
(3)写出实验室制取H的单质的化学反应方程式________________
(4)X、Y、Z和W可组成一化合物,其原子个数之比为8︰2︰4︰1。其水溶液中各种离子的浓度由大到小的顺序为____________
高二化学填空题简单题查看答案及解析
-
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素.它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
A. X、Y、Z既能形成离子化合物.又能形成共价化合物
B. Y和Z元素的原子半径大小顺序为Y>Z
C. X与Y、Z之问形成的核外电子总数为10的微粒只有YX3和X2Z
D. Z、W元索的最简单氢化物的沸点和稳定性均为H2Z>H2W
高二化学选择题困难题查看答案及解析
-
结构决定性质,性质决定用途;已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,Z的单质在常温下均为无色气体,W原子的最外层电子排布是nSn npn+2,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出W元素的元素符号和该原子基态的电子排布式:__ _____
(2)写出Z元素的原子结构示意图和该原子基态的电子排布图:_ _____
(3)X单质和Z单质在一定条件下反应生成化合物E,则E的电子式是:________。E可以进行喷泉实验的主要原因是:________。
(4)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子反应方程式为___________ __________________ ________
(5)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序)为(写名称)________,该化合物的浓溶液与足量NaOH热浓溶液反应的离子方程式为:____________ __ __
高二化学推断题困难题查看答案及解析
-
V、W、X、Y、Z五种短周期元素的原子序数依次增大,在周期表中W与V、X相邻,Y与Z相邻,X、Y同主族。Z的化合物可以发生某一反应,其离子方程式为:
(未完成)。
(1)Y、Z两种元素的简单离子的半径大小关系为 (用离子符号表示)。
(2)五种元素中分子的空间构型相同的氢化物沸点高低排列顺序为
(用分子式表示),其原因是 。
(3)V与Z单质不能直接化合生成VZ4,在催化剂作用下由VY2与Z2反应制得VZ4,其化学反应方程式为VY2+Z2→VZ4+Y2Z2(未配平)。
①写出上述化学反应方程式 。
②Y2Z2分子中,Y与Z均满足8e-结构,则Y2Z2的结构式为 。
③Y与W两种元素形成一种重要化合物A,A分子的结构如图所示:
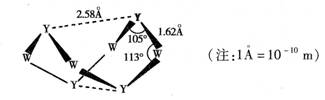
6mol Y2Z2与16mol W的简单氢化物恰好完全反应生成A、Y单质和一种中学化学中常见的盐。写出该反应的化学方程式: 。
高二化学填空题简单题查看答案及解析
-
A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为______,E原子核外有_____个未成对电子,五种元素中电负性最大的是_____(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)氯元素能与C(非碳元素符号)形成某化合物Q。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的结构式为___________。(如有配位键须用“→”标出)
(4)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是________(填标号)。
A.中心原子的价层电子对数目相等 B.都是非极性分子
C.中心原子的孤电子对数目相等 D.都含有极性键
E.都能与Na2O反应 F.固态时晶体类型不同
(5)D在空气中燃烧的产物分子构型为_________。固体DB3中存在如图所示的三聚分子,该分子中D原子的杂化轨道类型为________。

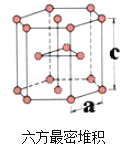
(6)E单质有两种同素异形体,高温下是体心立方堆积;但在常温下的晶体结构为如下图所示的六方最密堆积(底面是正六边形)。已知常温下晶体晶胞参数分别为a cm和c cm,则该晶体的密度可表示为________g·cm-3。(用含a和c的式子表示,用NA表示阿伏伽德罗常数的值)。
高二化学推断题困难题查看答案及解析
-
A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为__________________,E原子核外有_____个未成对电子,五种元素中电负性最大的是___________(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是______(填标号)。
A.中心原子的价层电子对数目相等B.都是非极性分子C.中心原子的孤电子对数目相等D.都含有极性键E.都能与Na2O反应F.固态时晶体类型不同
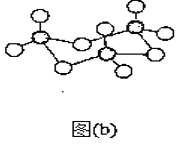
(4)D在空气中燃烧的产物分子构型为______。固体DB3中存在如图(b)所示的三聚分子,该分子中D原子的杂化轨道类型为________。
高二化学推断题困难题查看答案及解析
-
短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强元素。下列说法不正确的是( )
A. 原子半径: r(X) <r(Y) <r(Z) <r(W)
B. W的最高价氧化物的水化物是一种强碱
C. Y的简单氢化物比Z的简单氢化物沸点低
D. X、Y、Z 三种元素可以组成共价化合物和离子化合物
高二化学单选题中等难度题查看答案及解析
-
(8分)已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号:
X________、Y________、Z________、W________
(2)由以上元素中的两种元素组成的能溶于水产生气体且水溶液显碱性的化合物的电子式为。
(3)由X、Y、Z所形成的离子化合物是,它与W的最高氧化物的水化物的稀溶液反应的离子方程式是 。
高二化学填空题简单题查看答案及解析
-
现有X、Y、Z三种短周期元素,原子序数依次增大,它们原子的最外层电子数之和为20,X、Y是同周期相邻元素,Y、Z是同主族相邻元素.写出它们的元素符号:X______、Y______、Z______.
高二化学解答题中等难度题查看答案及解析
-
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。
下列说法正确的是 ( )
A. 五种元素的原子半径从大到小的顺序是:M﹥W>Z>Y>X
B. Z与同主族相邻元素的非金属性强弱,可通过它们的氧化物对应水化物的酸性强弱来判断
C. X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物
D. 用M单质的熔点高于其氧化物的熔点
高二化学单选题中等难度题查看答案及解析