-
(8分)某同学在用稀硫酸与锌粒(黄豆粒大小)制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有;
(2)硫酸铜溶液可以加快氢气生成速率的原因是________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有 ________、________。(例举两种措施)
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
请完成此实验设计,其中:V1=________,V6=________,V9=________;
实 验
混合溶液
A
B
C
D
E
F
4 mol/L H2SO4(mL)
40
V1
V2
V3
V4
V5
CuSO4(mL)
0
1
5
10
V6
40
H2O(mL)
V7
V8
V9
V10
15
0
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。
但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。
高一化学实验题简单题查看答案及解析
-
(Ⅰ)某同学在用稀硫酸与锌粒(黄豆粒大小)制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 、 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)要加快上述实验中气体产生氢气的速率,还可采取的措施有 、 (列举两种措施)。
(4)当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因______。
(Ⅱ)氢气是未来最理想的能源,科学家已研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O
2H2↑+O2↑。试回答下列问题:
(1)分解海水的反应属于_____反应(填“放热”或“吸热”)。
(2)燃料电池使用气体燃料和氧气直接反应产生电能,是一种很有前途的能源利用方式。某种氢氧燃料电池是用20℅KOH溶液作电解质,正极反应为: O2+4e-+2H2O ===4OH-,则电池供电的负极反应为:_____________。供电过程中,溶液的PH_________(填“增大”或“减小”)
(3)科学家最近研究出一种环保,安全的储氢方法,其原理可表示为:
NaHCO3+H2
HCOONa+H2O下列有关说法正确的是________。
A.储氢、释氢过程均无能量变化
B.NaHCO3具有离子键和共价键
C.储氢过程中,NaHCO3被氧化
D.释氢过程中,每消耗0.1mol H2O放出2.24L的H2
高一化学填空题困难题查看答案及解析
-
(10分)
某同学在用稀硫酸与锌粒(黄豆粒大小)制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)要加快上述实验中气体产生的速率,还可采取的措施有
、 、 。
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
请完成此实验设计,其中:V1= ,V6= ,V9= ;
实 验
混合溶液
A
B
C
D
E
F
4mol/LH2SO4/mL
40
V1
V2
V3
V4
V5
CuSO4/mL
0
1
5
10
V6
40
H2O/mL
V7
V8
V9
V10
15
0
该同学最后得出的结论为:当加入少量
溶液时,生成氢气的速率会大大提高。但当加入的
溶液超过一定量时,生成氢气的速率反而会下降。
高一化学计算题简单题查看答案及解析
-
某同学在用稀硫酸与锌制取氢气的实验中,发现反应条件不同,反应速率不同。请
回答下列问题:
(1)在用稀硫酸与锌制取氢气的实验中,加入少量硫酸铜溶液可加快氢气的生成速率。
①加入硫酸铜溶液后可以加快氢气生成速率的原因是 。
②实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4 溶液起相似作用的是 。
③为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
A
B
C
D
E
F
4 mol/L H2SO4(mL)
30
V1
V2
V3
V4
V5
饱和CuSO4溶液(mL)
0
0.5
2.5
5
V6
20
H2O(mL)
V7
V8
V9
V10
10
0
请完成此实验设计,其中:V1= ,V6= 。
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
(2)该同学为探究其它因素对锌与稀硫酸反应速率的影响,又做了以下实验,记录数据如下,回答下列问题:
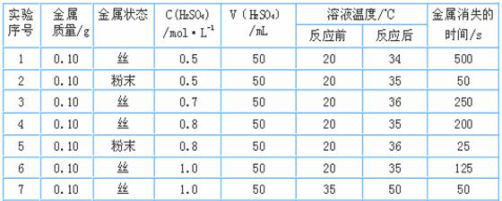
①由实验可推知,反应物的总能量 产物的总能量(填“<”“>”“=”)。
②实验2和5表明, 对反应速率有影响。
③实验4和5表明, 对反应速率有影响, 反应速率越快,
能表明同一规律的实验还有 (填实验序号)。
④本实验中影响反应速率的其他因素还有 。
高一化学实验题困难题查看答案及解析
-
(共11分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措施有________________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
A
B
C
D
E
F
4 mol·L-1 H2SO4/mL
30
V1
V2
V3
V4
V5
饱和CuSO4溶液/mL
0
0.5
2.5
5
V6
20
H2O/mL
V7
V8
V9
V10
10
0[
①请完成此实验设计,其中:V1==__________,V6==__________,V9==________。
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
高一化学实验题极难题查看答案及解析
-
(16分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是________;
(3)实验室中现有
、
、
、
等4中溶液,可与实验中
溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措施有________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
A
B
C
D
E
F
4mol/LH2SO4/mL
30
V1
V2
V3
V4
V5
饱和CuSO4溶液/mL
0 {007}
0.5
2.5
5
V6
20
H2O/mL
V7
V8
V9
V10
10
0
①请完成此实验设计,其中:V1=________,V6=________,V9=________;
②该同学最后得出的结论为:当加入少量
溶液时,生成氢气的速率会大大提高。但当加入的
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________。
高一化学填空题简单题查看答案及解析
-
(14分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是________;
(3)实验室中现有Na2SO3、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措施有________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验
混合溶液
A
B
C
D
E
F
4mol/L H2SO4/mL
30
V1
V2
V3
V4
V5
饱和CuSO4溶液/mL
0
0.5
2.5
5
V6
20
H2O/mL
V7
V8
V9
V10
10
0
①请完成此实验设计,其中:V1=________,V6=________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因。
高一化学实验题简单题查看答案及解析
-
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是________;
(3)实验室中现有
、
、
、
等4中溶液,可与实验中
溶液起相似作用的是________;
(4)要加快上述实验中气体产生的速率,还可采取的措旌有________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
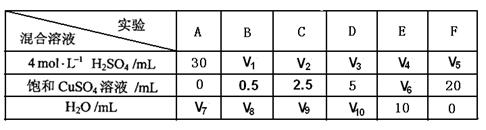
①请完成此实验设计,其中:V1=________,V6=________,V9=________;
②该同学最后得出的结论为:当加入少量
溶液时,生成氢气的速率会大大提高。但当加入的
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________
高一化学实验题困难题查看答案及解析
-
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.请回答下列问题:
(1)上述实验中的化学方程式有______;______.
(2)硫酸铜溶液可以加快氢气生成速率的原因是______;
(3)实验室中现有Na2SO4、Ag2SO4、MgSO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是______;
(4)要加快上述实验中气体产生的速率,还可采取的措施有(答一种即可):______.高一化学解答题中等难度题查看答案及解析
-
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是_______________________。
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是____________。
(3)要加快上述实验中气体产生的速率,还可采取的措施有_____________________(答两种)。
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
实验
混合溶液
A
B
C
D
E
F
4 mol·L-1 H2SO4/mL
30
V1
V2
V3
V4
V5
饱和CuSO4溶液/mL
0
0.5
2.5
5
V6
20
H2O/mL
V7
V8
V9
V10
10
0
①请完成此实验设计,其中:V1=________,V6=________,V9=______;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________。
高一化学实验题简单题查看答案及解析