-
纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈__________色。
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是__________。
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______。
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点________。
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
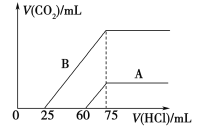
①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为_______mL。
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________,其物质的量之比为________。
-
纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈__________色。
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是__________。
A. 1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______。
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点________。
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
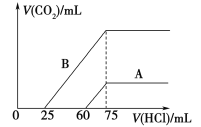
①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为_______mL。
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________,其物质的量之比为________。
-
下列有关钠及钠的化合物的说法中,正确的是
A. 一小块钠置于空气中足够时间,最终会变成Na2O2
B. 在饱和Na2CO3溶液中通入足量CO2有沉淀析出
C. 用洁净的铂丝蘸取溶液放置于酒精灯火焰上灼烧,焰色为黄色;该溶液为钠盐溶液
D. 7.8gNa2O2和6.2gNa2O分别溶于100g水中,得到溶液的质量分数前者更大
-
纯碱和小苏打是厨房中两种常见用品,它们都是白色固体,下列区分它们的说法正确的是( )
A.先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打
B.用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,火焰颜色为黄色的是小苏打
C.分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打
D.用两只小玻璃杯,分别加入少量的两种样品,再加入等浓度的食醋,产生气泡速率较快的是小苏打
-
下列实验结论或应用不正确的是
| 实验操作 | 现象 | 结论或应用 |
| A | 食醋浸泡水垢 | 产生无色气体 | 乙酸的酸性比碳酸强 |
| B | 用洁净的铂丝蘸取待测液置于酒精灯外焰灼烧 | 火焰呈黄色 | 待测液中含钠元素 |
| C | 碘酒滴到土豆片上 | 土豆片变蓝 | 淀粉遇碘变蓝 |
| D | 向苯中滴入适量浓溴水,振荡,静置 | 溶液上层呈橙红色,下层几乎无色 | 苯和溴发生取代反应,使溴水褪色 |
A. A B. B C. C D. D
-
碳酸钠俗称纯碱,在日常生产和生活中有着广泛的应用.某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl),然后再将NaHCO3制成Na2CO3.
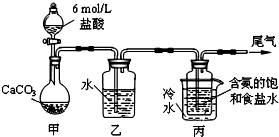
(1)装置乙的作用是__________.为防止污染空气,尾气中含有的__________需要进行吸收处理.
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有__________、__________、__________.
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1min的NaHCO3样品的组成进行了以下探究。取加热了t1min的NaHCO3样品19g完全溶于水制成溶液,然后向此溶液中不断滴加1mol•L﹣1的稀盐酸直到不再产生气泡,共消耗300ml稀盐酸.问该样品中NaHCO3和Na2CO3的物质的量之比是__________.
-
盐类水解在工农业生产和日常生活中有着广泛的应用,有关应用或说法与盐类水解无关的是
A. 用热的纯碱溶液洗涤餐具上的油污
B. 生活中常用明矾净水
C. 用稀硫酸或浓氨水除去铜器表面的铜绿
D. 长期使用硫酸铵化肥的土壤,易变酸性,可施用适量的熟石灰
-
纯碱和小苏打是厨房中两种常见用品,下列区分它们的说法中正确的是( )
A.分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打
B.用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,使火焰颜色发生明显变化的是小苏打
C.用两只试管,分别加入少量两种样品,再加入等浓度食醋,产生气泡速率较快的是小苏打
D.将两种样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打
-
下列对某些离子的检验及结论一定正确的是
A.先加入BaCl2溶液,产生白色沉淀,再加入HNO3溶液,白色沉淀不溶解,则溶液中一定含有大量的SO42﹣
B.用洁净的铂丝蘸取待测液,置于酒精灯火焰上灼烧,观察到火焰呈黄色,则表明待测液中一定含有Na+而不含K+
C.加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32﹣
D.加入氯化钠溶液,有白色沉淀产生,再加入稀硝酸沉淀不消失,一定有 Ag+
Ag+
-
下列实验及结论一定正确的是( )
A.将一小块钠投入硫酸铜溶液中,能得到红色的铜
B.用洁净的铂丝蘸取待测液,置于酒精灯火焰上灼烧,观察到火焰呈黄色,则表明待测液中一定含有Na+而不含K+
C.加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32-
D.加入氯化钠溶液,有白色沉淀产生,再加入稀硝酸沉淀不消失,一定有Ag+


