-
在常温下,向10mL浓度均为0.1mol·L-1的NaOH和Na2CO3混合溶液中滴0.1mol·L-1的盐酸,溶液pH随盐酸加入体积的变化如图所示。下列说法正确的是

A.在a点的溶液中,c(Na+)>c(CO32-)>c(Cl-)>c(OH-)>c(H+)
B.在b点的溶液中,2n(CO32-)+n(HCO3-)<0.001mol
C.在c点的溶液pH<7,是因为此时HCO3-的电离能力大于其水解能力
D.若将0.1mol·L-1的盐酸换成同浓度的醋酸,当滴至溶液的pH=7时:c(Na+)=c(CH3COO-)
-
如图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol·L-1 NaOH溶液时,溶液的pH随 NaOH溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是
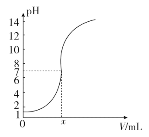
A. 原盐酸的浓度为0.10 mol·L-1
B. x的值为2.0
C. 当pH=12时,V值为20.4
D. 原盐酸的浓度为1.0 mol·L-1
-
25 ℃时,在10 mL浓度均为0.1 mol·L-1的NaOH和NH3·H2O混合溶液中滴加0.1 mol·L-1盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
B.加入20 mL盐酸时:c(Cl-)=c(NH4+)+c(Na+)
C.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
D.加入10 mL盐酸时:c(NH4+)+c(H+)=c(OH-)
-
25℃时,在10mL浓度均为0.1mol•L﹣1的NaOH和NH3•H2O混合溶液中滴加0.1mol•L﹣1盐酸,下列有关溶液中粒子浓度关系正确的是( )
A. 未加盐酸时:c(OH﹣)>c(Na+)=c(NH3•H2O)
B. 加入10mL盐酸时:c(NH4+)+c(H+)=c(OH﹣)
C. 加入盐酸至溶液pH=7时:c(Cl﹣)=c(Na+)
D. 加入20mL盐酸时:c(Cl﹣)=c(NH4+)+c(Na+)
-
25℃时,在10 mL浓度均为0.1mol/L NaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐 酸,下列有关溶液中粒子浓度关系正确的是
酸,下列有关溶液中粒子浓度关系正确的是
A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O)
B.加入10 mL盐酸时:c(NH4+) +c(H+) =c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D.加入20 mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
-
25℃时,在10 mL浓度均为0.1mol/L NaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是
A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O)
B.加入10 mL盐酸时:c(NH4+) +c(H+) =c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D.加入20 mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
-
25℃时,在10 mL浓度均为0.1 mol/L NaOH和NH3·H2O混合溶液中滴加0.1 mol/L盐酸,下列有关溶液中粒子浓度关系正确的是
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
B.加入10 mL盐酸时:c(NH )+c(H+)=c(OH-)
)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时:c(Cl-)=c(NH )+c(Na+)
)+c(Na+)
-
25℃时,在10 mL浓度均为0.1 mol/L NaOH和NH3 •H2O的混合溶液中,滴加0.1 mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+) =c(NH3·H2O)
B.加入10mL盐酸时:c(NH4+)+c(H+)+ c(Na+)= c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时: c(Cl-)= c(NH4+)+c(Na+)
-
常温下,向20 mL 0.1 mol/L酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液。有关微粒的物质的量与混合溶液的pH有如图关系。下列说法正确的是( )
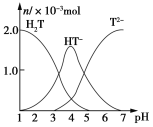
A. V(NaOH)=10 mL时,溶液中存在c(Na+)=2c(H2T)+2c(HT-)+2c(T2-)
B. V(NaOH)=20mL时,溶液中存在c(Na+)>c(HT-)>c(H+)>c(H2T)>c(T2-)
C. V(NaOH)=30mL时,溶液中存在c(Na+)>c(HT-)>c(T2-)>c(OH-)>c(H+)
D. V(NaOH)=40mL时,溶液中存在c(OH-)=c(HT-)+2c(H2T)+c(H+)
-
25℃时,在10mL浓度为0.1mol﹒L-1NaOH和NH3·H2O混合溶液中,滴加0.1mol·L-1的盐酸,下列有关溶液中粒子浓度关系正确的是
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
B.加入10mL盐酸时:c(NH4+)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20mL盐酸时:c(Cl-)=c(NH4+)+c(Na+)


