-
某二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA- H++A2-(25 ℃时Ka=5.0×10-3),下列有关说法中正确的是( )
H++A2-(25 ℃时Ka=5.0×10-3),下列有关说法中正确的是( )
A.H2A是弱酸
B.稀释0.1 mol·L-1 H2A溶液,因电离平衡向右移动而导致c(H+)增大
C.若0.1 mol·L-1 NaHA溶液中c(H+)=0.02 mol·L-1,则0.1 mol·L-1的H2A中c(H+)<0.12 mol·L-1
D.在0.1 mol·L-1的H2A溶液中,c(H+)=0.12 mol·L-1
-
某二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA- H++A2-(25℃时Ka=1.0×10-2),下列有关说法中正确的是( )
H++A2-(25℃时Ka=1.0×10-2),下列有关说法中正确的是( )
A.H2A是弱酸
B.稀释0.1 mol/L H2A溶液,因电离平衡向右移动而导致c(H+ )增大
C.在0.1 mol/L的H2A溶液中,c(H+)=0.12 mol/L
D.若0.1 mol/L NaHA溶液中c(H+)=0.02 mol/L,则0.1 mol/L的H2A中c(H+)< 0.12 mol/L
-
某二元酸(H2A)在水中的电离方程式为:H2A===H++HA-,HA- H++A2-(25 ℃时Ka=1.0×10-2),下列有关说法中正确的是
H++A2-(25 ℃时Ka=1.0×10-2),下列有关说法中正确的是
A. H2A是弱酸
B. 稀释0.1 mol·L-1H2A溶液,因电离平衡向右移动而导致c(H+)增大
C. 在0.1 mol·L-1的H2A溶液中,c(H+)=0.12 mol·L-1
D. 若0.1 mol·L-1 NaHA溶液中c(H+)=0.02 mol·L-1,则0.1 mol·L-1H2A中c(H+)< 0.12 mol·L-1
-
某二元酸H2A在水中的电离方程式是H2A=H++HA-,HA- H++A2-。回答下列问题:
H++A2-。回答下列问题:
(1) Na2A溶液显 (填“酸性”、“中性 ”或“碱性”),理由是 (用离子方程式或必要的文字说明)。
”或“碱性”),理由是 (用离子方程式或必要的文字说明)。
(2) 常温下,已知0.1 mol·L-1NaHA溶液pH=2,则0.1 mol·L-1H2A溶液中氢离子的物质的量浓度可能 0.11 mol·L-1(填“大于”、“等于”或“小于”), 理由是 。
(3) 0.1 mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是
(4) Na2A溶液中,下列表述正确的是
A.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
B.c(Na+)=2[c(HA-)+c(A2-)+c(H2A)]
C.c(OH-)=c(HA-)+c(H+)+2c(H2A)
D.c(OH-)=c(HA-)+c(H+)
-
某二元酸(化学式用H2A表示)在水中的电离方程式是H2A===H++HA-,HA-⇌H++A2-。回答下列问题:
(1)Na2A溶液显(填“酸性”、“中性”或“碱性”),理由是(用离子方程式或必要的文字说明)。
(2)常温下,已知0.1mol·L-1NaHA溶液pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能0.11mol·L-1(填“大于”、“等于”或“小于”),理由是。
(3)0.1mol·L-1N aHA溶液中各种离子浓度由大到小的顺序是。
aHA溶液中各种离子浓度由大到小的顺序是。
(4)Na2A溶液中,下列表述正确的是。
A.cNa++cH+=cHA-+2cA2-+cOH—
B.cNa+=2(cHA-+cA2-+cH2A)
C.cOH—=cHA-+cH++2cH2A
D.cOH—=cHA-+cH+
-
某二元酸(化学式用H2A表示)在水中的电离方程式是(第一步电离完全):H2A═H++HA- HA-⇌H++A2-
回答下列问题:
(1)Na2A溶液显______(填“酸性”、“中性”、“碱性”)理由是:(用离子方程式表示)______.
(2)0.1mol/L的H2A溶液的pH______1(填“<”“=”“>”)
(3)0.1mol/L的Na2A溶液中,下列微粒浓度关系错误的是______.
A、c(Na+)=2c(A2-)=0.2mol/L
B、c(OH-)=c(H+)+c(HA-)
C、c ( Na+)+c ( H+)=c( OH-)+c (HA-)+2c (A2-)
D、c(Na+)=2c (A2-)+2c (HA-)
-
某二元酸(化学式用H2A表示)在水中的电离方程式是(第一步电离完全):
H2A == H+ + HA- HA-  H+ + A2-
H+ + A2-
回答下列问题:
(1)Na2A溶液显____________(填“酸性”、“中性”、“碱性”)
理由是:(用离子方程式表示)__________________________________________。
(2)0.1mol/L的H2A溶液的pH_________1(填“<” “=” “>”)
(3)0.1mol/L的Na2A溶液中,下列微粒浓度关系错误的是_____________。
A、c(Na+) =2c(A2-) = 0.2 mol/L
B、c(OH-) = c(H+) + c(HA-)
C、c ( Na+ ) + c ( H+ ) = c( OH- ) + c (HA- ) + 2c (A2-)
D、c(Na+) = 2c (A2-) + 2c (HA-)
-
某二元酸(化学式用H2A)表示,在水中的电离方程式是:
H2A = H+ + HA-, HA- H+ + A2- 回答下列问题:
H+ + A2- 回答下列问题:
(1)Na2A溶液呈________(填”酸性,中性或碱性”),理由是,用离子方程式表示:
________.
(2)若0.1 mol?L-1NaHA溶液的pH = 2,则0.1 mol?L-1H2A溶液中氢离子的物质的量浓度可能是___________0.11 mol?L-1(填>、<、=)。理由是_________________________
(3)0.1 mol?L-1NaHA溶液中各种离子浓度由大到小的顺序是______________________
-
某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A===H++HA-,HA- H++A2-回答下列问题:
H++A2-回答下列问题:
(1)Na2A溶液显________(填“酸性”“中性”或“碱性”),用离子方程式表示其原因________________。
(2)在0.1 mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是____________。
A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HA-)+2c(H2A)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+)
(3)常温下,已知0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中c(H+)可能___________(填“>”、“<”或“=”)0.11 mol·L-1;理由是_______________________。
(4)比较①0.1 mol·L-1 Na2A溶液 ②0.1 mol·L-1 Na2SO4溶液,两种溶液中阴离子总浓度的大小①________②(填“>”、“<”或“=”)。
(5)O3可由臭氧发生器(原理如图)电解稀硫酸制得。
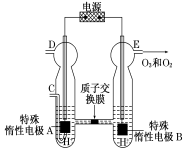
①图中阴极为______________(填“A”或“B”),其电极反应式 为_______________________。
为_______________________。
②若C处通入O2,则A极的电极反应式为______________。
③若C处不通入O2,D、E处分别收集到x L和y L气体(标准状况),则E处收集的气体中O3所占的体积分数为______________(忽略O3的分解)。
-
某二元酸(H2A)在水中的电离方程式是H2A=H++HA-,HA- H++A2-。
H++A2-。
(1)Na2A溶液显_________(填“酸性”“中性”或“碱性”)。理由是__________(用离子方程式表示)。
(2)已知0.1mol/L的NaHA溶液的pH=2,则0.1mol/L的H2A溶液中c(H+ )_______(填“<”“>”或“=”)0.11mol/L。
(3)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式不正确的是__(填字母)。
A.c(A2- )+c(HA-)=0.1mol/L
B.c(OH-)=c(H+) +c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(4)若向0.1mol/L的H2A溶液中加入等体积等浓度的NaOH溶液,则溶液中各离子浓度由大到小的顺序为__________________。
H++A2-(25 ℃时Ka=5.0×10-3),下列有关说法中正确的是( )
