-
火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)===N2(g)+2H2O(g)ΔH =-534 kJ·mol-1
H2O2(l)===H2O(l)+ O2(g)ΔH =-98 kJ·mol-1
O2(g)ΔH =-98 kJ·mol-1
H2O(l)===H2O(g)ΔH =44 kJ·mol-1
(1)试写出N2H4和液态H2O2反应生成气态水的热化学方程式_________________。
(2)化学键的键能是指气态原子间形成1mol化学键时释放的能量。下表列出了某些化学键的键能:
| 化学键 | H-H | O=O | O-H |
| 键能 (kJ·mol-1) | 436 | x | 463 |
请回答下列问题:
①如图表示某反应的能量变化关系图,此反应为____________(填“放热”或“吸热”)反应,其中ΔH = ________kJ·mol-1(用含C和D的字母表示);

②若此能量变化关系图表示如下反应:H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则B=_________kJ·mol-1,x=___________。
-
(8分)过氧化氢和臭氧都是常见的绿色氧化剂,工业生产中有着重要用途。
(1)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)===H2O(l)+ O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1
H2O(l)===H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式_________________________。
(2)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+O3(g) NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是________________。
NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是________________。

a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.该反应为放热反应
d.Δt1=Δt2时,NO的转化量:a~b段小于b~c段
-
火箭推进器常以联氨(N2H4)为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式:
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O (l) DH2=–44 kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) DH3=–196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为
A.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=+817.63 kJ·mol-1
B.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-641.63 kJ·mol-1
C.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=-641.63 kJ·mol-1
D.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-817.63 kJ·mol-1
-
(火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:N2H4(g)+O2(g)═N2(g)+2H2O(g)△H1=﹣533.23kJ•mol﹣1
H2O(g)═H2O (l)△H2=﹣44kJ•mol﹣1
2H2O2(l)═2H2O(l)+O2(g)△H3=﹣196.4kJ•mol﹣1
则联氨与过氧化氢反应的热化学方程式可表示为
A.N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol﹣1
B.N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63 kJ•mol﹣1
C.N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=﹣641.63 kJ•mol﹣1
D.N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣817.63 kJ•mol﹣1
-
火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式: N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=﹣533.23kJ•mol﹣1;H2O(g)=H2O (l)△H2=﹣44kJ•mol﹣1;2H2O2(l)=2H2O(l)+O2(g)△H3=﹣196.4kJ•mol﹣1则联氨与过氧化氢反应的热化学方程式可表示为( )
A. N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol﹣1
B. N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣641.63 kJ•mol﹣1
C. N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=﹣641.63 kJ•mol﹣1
D. N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=﹣817.63 kJ•mol﹣1
-
火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1;H2O(g)=H2O (l)△H2=-44kJ•mol-1;2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1则联氨与过氧化氢反应的热化学方程式可表示为( )
A.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=+817.63kJ•mol-1
B.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63kJ•mol-1
C.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-641.63kJ•mol-1
D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-817.63kJ•mol-1
-
按要求书写热化学方程式(是离子反应的也可用离子方程式表示).
(1)表示强酸和强碱中和热的热化学方程式:______.
(2)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供.反应过程中生成的气体可参与大气循环.测得当反应过程中有1mol水蒸气生成时放出161kJ的热量.试写出反应过程中的热化学方程式:______.
(3)由氢气和氧气反应生成1mol水蒸气.放热241.8kJ.写出该反应的热化学方程式:______.若1g水蒸气转化成液态水放热2.5kJ,则反应H2(g)+ O2(g)=H2O(l)的△H=______kJ•mol-1,H2的燃烧热为______kJ•mol-1
O2(g)=H2O(l)的△H=______kJ•mol-1,H2的燃烧热为______kJ•mol-1
(4)已知A、B两种气体在一定条件下可发生反应:2A+B═C+3D+4E.现将相对分子质量为M的A气体mg和足量B气体充入一密闭容器中恰好完全反应后,有少量液滴生成.在相同温度下测得反应前后压强分别为6.06×105Pa和1.01×106Pa,又测得反应共放出QkJ热量.试根据上述实验数据写出该反应的热化学方程式______.
-
2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)(液态)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全反应生成氮气和1 mol气态水过程中的能量变化图。

(1)该反应属于________(填“吸热”或“放热”)反应。
(2)写出该火箭推进器中相关反应的热化学方程式:__________________。
(3)若该火箭推进器中H2O2有12 mol共价键发生断裂,则反应释放出的热量______kJ。
-
氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃剂。N2H4 (1)与N2O4(g)生成4 mol H2O(g)时放出热量1077 kJ,写出其热反应方程式:_____________________________________。
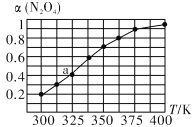
(2)N2O4与NO2之间存在反应N2O4(g) 2NO2 (g)将一定量的 N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
2NO2 (g)将一定量的 N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度的变化如图所示。
①由图推测该反应ΔH_______0(填“>”或“<”),理由为__________________________。
②图中a点对应温度下,已知N2O4的起始压强p0为108 kPa,列式计算该温度下反应的平衡常数Kp =____________。(保留一位小数,并带单位。用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③在一定条件下,该反应N2O4、NO2两者的消耗速率与自身压强间存在关系:v消耗(N2O4)=k1· P(N2O4),v消耗(NO2)=k2·P2(NO2),其中k1、k2是与反应温度有关的速率常数。则一定温度下,k1、k2与平衡常数Kp的关系是k1=________________。
-
火箭推进剂由肼(N2H4)和液态过氧化氢组成,当它们混合反应时,即产生大量N2和H2O(g),并放出大量的热量。已知0.4mol液态肼与足量液态H2O2反应,生成N2和H2O(g)并放出256.65kJ热量。
(1)反应的热化学方程式为____________;
(2)反应中的氧化剂是_______;
(3)当放出256.65kJ热量时,转移电子数_______;
(4)此燃料的优点是____________________。
O2(g)ΔH =-98 kJ·mol-1



