-
(8分)近年来,我国储氢纳米碳管研究获得重大进展,电弧法合成的碳纳米管,常伴有大量的物质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法除去,同时生成的产物对环境不会产生污染。在整个反应体系中除了碳单质外,还有K2Cr2O7 、K2SO4、Cr2(SO4)3、H2SO4、H2O和X。
(1)根据题意,可判断出X是____________(写化学式)。
(2)在反应中,氧化剂应是____________(写化学式),硫酸的作用是_____________。
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目。
(4)在上述反应中,若产生22 g X物质,则反应中转移的电子数目为_____________。
高三化学填空题简单题查看答案及解析
-
近年来,我国储氢纳米碳管研究获得重大进展,电弧法合成的碳纳米管,常伴有大量的物质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法除去,同时生成的产物对环境不会产生污染。在整个反应体系中除了碳单质外,还有K2Cr2O7 、K2SO4、Cr2(SO4)3、H2SO4、H2O和X。
(1)根据题意,可判断出X是____________(写化学式)。
(2)在反应中,氧化剂应是____________(写化学式),硫酸的作用是_____________。
(3)写出并配平该反应的化学方程式,并标出电子转移的方向和数目。
(4)在上述反应中,若产生22 g X物质,则反应中转移的电子数目为_____________。
高三化学填空题中等难度题查看答案及解析
-
(8分)近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,长伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:__C+___K2Cr2O7+__H2SO4(稀 ) → ___CO2+__K2SO4+ Cr2(SO4)3+ __ ___
(1)完成并配平上述反应的化学方程式
(2)此反应的氧化剂______,还原剂______
(3)硫酸在上述反应中表现出的性质是____________(填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若产生11克气体物质,则转移电子的数目___________
高三化学填空题中等难度题查看答案及解析
-
(13分)近年来,我国对储氢纳米碳管的研究获得了重大进展,电弧法合成的纳米碳管常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其反应的化学方程式为:
C + K2Cr2O7+ H2SO4(稀)== CO2+ K2SO4+ Cr2(SO4)3+
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为 。
高三化学填空题中等难度题查看答案及解析
-
(10分)近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管,常伴有大量物质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:
C+ K2Cr2O7 + H2SO4(稀)
CO2↑+ K2SO4 + Cr2 (SO4 ) 3+ . ________
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是________,氧化产物是________。
(3)H2SO4在上述反应中表现出来的性质是________(填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11g气体物质,则转移电子的数目为________。
高三化学填空题中等难度题查看答案及解析
-
(8分)近年来,我国研究储氢碳管获得重大进展,用电弧法合成碳纳米管,常伴有大量碳纳米颗粒生成,这种碳纳米颗粒可用氧化气化法除去,其反应的化学方程式为:
_________C +___________K2Cr2O7 +__________H2SO4(稀 ) → __ _CO2+__________K2SO4+ ________Cr2(SO4)3+________ ____________
(1)此反应的氧化剂_▲ ___,还原剂__▲___
(2)硫酸在上述反应中表现出的性质是__▲ _____(填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目_▲ ______
高三化学选择题中等难度题查看答案及解析
-
近年来,我国储氢碳纳米管研究获重大进展,电弧法合成的碳纳米管,常伴有大量的碳纳米颗粒生成。这种碳纳米颗粒可用氧化气化法提纯。其反应的离子方程式为(其中a、b、c、d、e 、f为反应计量数):aC + bCr2O72-+ cH+ = dCO2↑+ eCr3+ + f H2O。有关上述反应的叙述中正确的是 ( )
A.当a = 3时,e = 2
B.反应中既可用稀硫酸又可用浓硝酸酸化
C.若产生11 g气体物质,则有6.02×1023个电子发生转移
D.反应计量数b、c、e有如下关系:3e =2b + c
高三化学单选题极难题查看答案及解析
-
2001年1月6日,我国525名两院院士投票评选出1999年中国十大科技进步奖,其中一项是:储氢碳纳米管研究获重大进展。电弧法合成的碳纳米管,常伴有大量杂质——纳米颗粒。这种碳纳米颗粒可用氧化汽化法提纯。
其反应式是3C+2 K2Cr2O7+ 8H2SO4 3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
(1)单线法标出电子转移的数目和方向。
(2)此反应的氧化剂是________氧化产物是________。
(3)H2SO4在上述反应中表现出来的性质是(填选项编号)
A、酸性 B、氧化性 C、吸水性 D、脱水性
(4)上述反应中若产生0.1mol气体物质,则转移电子的物质的量是________mol.
高三化学填空题简单题查看答案及解析
-
(16分)请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)我国储氢纳米碳管研究已取得重大进展。用电弧法合成的碳纳米管中常伴有大量碳
纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
___C + ___K2Cr2O7 + _______= ___ CO2↑ + ___K2SO4 + ___Cr2(SO4)3 +___H2O
请完成并配平上述化学方程式。
(2)工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g)
CH3OH(g) △H1=-116 kJ·mol-1
①下列措施中有利于增大该反应的反应速率的是____________。
A.使用高效催化剂 B.降低反应温度
C.增大体系压强 D.不断将CH3OH从反应混合物中分离出来
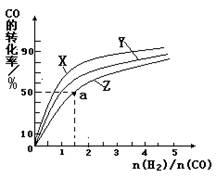
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2)/n(CO)的起始组成比的关系如右图所示。已知容器体积1L,起始时CO的物质的量均为1mol。据此判断在上述三种温度中,曲线Z对应的温度是__________;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K =_______________________。
③已知:
△H2=-283 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气的热化学方程式为_________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其溶度积常数Ksp=
c(Ca2+)·c(CO32—)=2.8×10−9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为5.6×10 -5 mol/L ,则生成沉淀所需CaCl2溶液的最小浓度为________________________。
高三化学填空题中等难度题查看答案及解析
-
请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化后气化的方法提纯,其除杂质过程为把杂质用热的重铬酸钾(K2Cr2O7)酸性溶液浸泡发生反应,溶液逐渐变成浅绿色(Cr3+),同时产生使澄清石灰水变浑浊的气体,写出反应的离子方程式:____________________________________________。
(2)焦炭可用于制取水煤气。测得24g碳与水蒸气完全反应生成水煤气时,吸收了263.2kJ热量。该反应的热化学方程式为_________________________________。
(3)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为CO(g)+2H2(g)
CH3OH(g) △H1=-116kJ·mol-1。
①下列措施有利于提高反应物转化率的是___________(填序号)。
A.及时将CH3OH与反应混合物分离 B.降低反应温度
C.减小体系压强 D.使用高效催化剂
②乙醇电池具有很高的实用价值。如右图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池的负极反应式为_________________________________。

③已知:CO(g)+
O2(g)=CO2(g) △H2=-283 kJ·mol-1
H2(g)+
O2(g)=H2O(g) △H3=? kJ·mol-1
1mol气态甲醇完全燃烧生成CO2和水蒸气时放出热量651kJ,则△H3=________________。
④在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律,如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答下列问题:
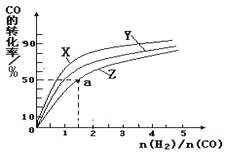
(i)在上述三种温度中,曲线X对应的温度是______________________。
(ii)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)
CH3OH(g)的平衡常数K=___________。
(4)CO2经常用氢氧化钠溶液来吸收,现有0.2moCO2,若用100mL3 mol/LNaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为______________________。
高三化学综合题中等难度题查看答案及解析