-
已知:(A)Cu2+,Fe2+在pH为4~5的条件下不水解而Fe3+却几乎全部水解;(B)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O.用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取50mL纯净的盐酸,加入一定量的粗CuO加热搅拌,充分反应后过滤,经测定溶液的pH是3
②向滤液中加入双氧水,搅拌.
③向②中加入过量纯CuO,微热,搅拌,此时测定溶液的pH为4,过滤.
④把③所得滤液浓缩.
填空:
(1)②中发生反应的离子方程式是______.
(2)③中过滤后滤渣的成分是______.
(3)①③中如何用pH试纸测定溶液的pH值:______.
(4)③中pH升高的原因是:______.(用离子方程式表示)高二化学解答题中等难度题查看答案及解析
-
已知:(A)Cu2+,Fe2+在pH为4~5的条件下不水解而Fe3+却几乎全部水解;(B)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O.用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取50mL纯净的盐酸,加入一定量的粗CuO加热搅拌,充分反应后过滤,经测定溶液的pH是3。
②向滤液中加入双氧水,搅拌。
③向②中加入过量纯CuO,微热,搅拌,此时测定溶液的pH为4,过滤。
④把③所得滤液浓缩。
填空:
(1)②中发生反应的离子方程式是________;
(2)③中过滤后滤渣的成分是________;
(3)①③中如何用pH试纸测定溶液的pH值:________;
(4)直接加热溶液,蒸干________(选填“能”或“不能”)得到氯化铜晶体(CuCl2·2H2O),原因是________。
高二化学填空题中等难度题查看答案及解析
-
已知:(A)Cu2+,Fe2+在pH为4~5的条件下不水解而Fe3+却几乎全部水解;(B)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O。用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取50mL的盐酸,加入一定量的粗CuO加热搅拌,充分反应后过滤,溶液的pH是3
②向滤液中加入双氧水,搅拌。
③向②中加入过量纯CuO,微热,搅拌,此时测定溶液的pH为4,过滤。
④把③所得滤液浓缩。
(1)②中发生反应的离子方程式是 。
(2)③中过滤后滤渣的成分是 。
(3)①③中如何用pH试纸测定溶液的pH值: 。
(4)③中pH升高的原因是: 。(用离子方程式表示)
高二化学填空题困难题查看答案及解析
-
已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是
A.向溶液中通入Cl2,再加入纯净的CuO粉末调节pH为4~5
B.向溶液中通入Cl2,再通入NH3,调节pH为4~5
C.向溶液中通入H2S使Fe2+沉淀
D.加入纯Cu将Fe2+还原为Fe
高二化学选择题中等难度题查看答案及解析
-
已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是
A. 向溶液中通入H2S使Fe2+沉淀
B.向溶液中通入Cl2,再通入NH3,调节pH值为4~5
C. 加入纯Cu将Fe2+还原为Fe
D.向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4~5
高二化学选择题简单题查看答案及解析
-
已知:在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取一定量的粗CuO,加入过量浓盐酸,加热并搅拌,充分反应后过滤,溶液的pH为1。
②向滤液中通入Cl2,搅拌。
③向②中加入适量物质A,微热,搅拌,调整溶液的pH,过滤。
④把③所得滤液浓缩。
(1)①中加热并搅拌的目的是_____________________________。
(2)②中发生反应的离子方程式是_________________________。
(3)③中的物质A可能是__________________;调整的PH范围是_______________;
过滤后滤渣的成分是__________________。
(4)③中发生反应的离子方程式是_________________________。
(5)①③中如何用pH试纸测定溶液的pH值:_________________________。
高二化学解答题简单题查看答案及解析
-
(10分)已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,所需溶液的pH分别为6.4、6.4、3.7。现由含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其配制成水溶液,然后按图示步骤进行提纯:
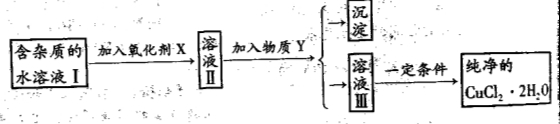
请回答下列问题:
(1)本实验最适合的氧化剂是( )(填下面的序号)
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是 ;(用化学式表示)
(3)本实验用碱沉淀法能否达到目的? ;原因是 ;
(4)除去Fe3+的原理是 ;
高二化学填空题中等难度题查看答案及解析
-
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、6.4、3.7。现有含FeClx杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
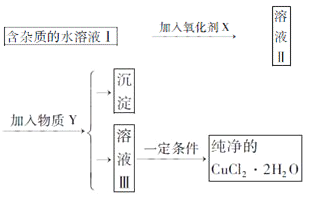
请回答下列问题:
(1)本实验最适合的氧化剂X是__________。(选填下面的序号)
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是__________。
(3)本实验用加碱沉淀的目的是否能达到?__________。原因是__________。
(4)加氧化剂的目的为__________。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________。如何操作? __________。·
高二化学实验题中等难度题查看答案及解析
-
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
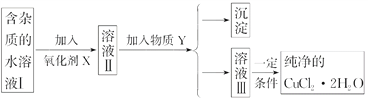
请回答下列问题:
(1)本实验最适合的氧化剂X是________(填序号)。
A.K2Cr2O7 B.NaClO
C.H2O2 D.KMnO4
(2)物质Y是________。
(3)除去Fe3+的有关离子方程式是____________________、_______________________。
(4)加氧化剂的目的是____________________________________________。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________,应如何操作?_____。
高二化学综合题困难题查看答案及解析
-
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图所示步骤进行提纯:
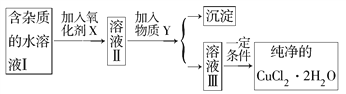
请回答下列问题:
(1)本实验最适合的氧化剂X是________(填序号)。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是____________________________________。
(3)加氧化剂X的有关离子方程式是_______________________________。
(4)加氧化剂X的目的是_____________________________________________。
(5)为什么不能直接蒸发结晶得到CuCl2·2H2O晶体?____________。
高二化学综合题中等难度题查看答案及解析