-
(14分)某晶体(结晶水合物)由五种短周期元素组成。常温下,将该晶体溶于蒸馏水后可电离出三种离子(忽略水的电离),其中两种离子含有的电子数均为10个。将该溶液分成等量2份,一份中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,产生白色沉淀;向另一份中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

请回答下列问题:
(1)若该晶体的摩尔质量为906g·mol-1,写出该晶体的化学式 ;
(2)B点溶液的pH 7(填“<”、“>”或“=”),用化学用语表示其原因 。
(3)若向该晶体的水溶液中逐滴加入Ba(OH)2溶液至产生最多的沉淀,写出该变化的离子方程式 。
(4)C点溶液中所含溶质的化学式为 ;此时溶液中各种离子浓度由大到小顺序为 。
-
甲是一种含有结晶水的盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出两种阳离子和一种阴离子,其中A、B两元素可形成10电子的阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入过氧化氢的酸性溶液,呈红色;
③取少量甲溶液于试管中,向其中加入稀盐酸后,再加入BaCl2溶液,出现白色沉淀;
④取少量甲溶液于试管中加入适量NaOH溶液,加热;
回答下列问题:
(1)实验③可证明溶液中含有 。
(2)用离子方程式表示实验②中现象的原因: , 。
(3)实验④中出现的现象是 。
(4)经测定甲晶体的摩尔质量为392 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
-
(10分)X、Y、Z、W、V为前四周期常见的五种元素,其中四种为短周期元素。X原子核外电子数等于其电子层数;常温常压下,Y单质固体难溶于水而易溶于 ;Z的氢化物在水中可完全电离出氢离子;W原子的电子层数是其价电子数的3倍;V的单质是一种应用最为广泛的金属。
;Z的氢化物在水中可完全电离出氢离子;W原子的电子层数是其价电子数的3倍;V的单质是一种应用最为广泛的金属。
请回答下列问题:
(1)写出实验室通过加热制备Z单质的离子方程式________;
(2)W的两种常见氧化物中阳离子和阴离子个数比为2:1的是________
(写化学式);
(3)写出X、Y、W三种元素组成的化合物的水溶液与Z单质反应的离子方程式________(可不配平);
(4)检验V的最高价简单离子常用的试剂是________;
(5)将12gY单质完全燃烧的产物通入1OOmL1.2 的氢氧化钠溶液中,所得溶液
的氢氧化钠溶液中,所得溶液
中含有的主要离子分别是
-
某结晶水合物,含有两种阳离子和一种阴离子,其中所含元素均为短周期元素。为确定其组成,有同学进行了如下实验:称取906 g样品,溶于水,将溶液分成两等份,待用。
①向一份溶液中逐滴加入6 mol·L-1 NaOH溶液,先观察到有白色沉淀产生,而后产生使湿润的红色石蕊试纸变蓝色的气体,继续滴加NaOH,白色沉淀又逐渐消失,最后得到无色透明溶液。向其中加入足量BaCl2溶液,可得不溶于稀盐酸的白色沉淀466 g。
②取另一份溶液,加入足量6 mol·L-1 NaOH溶液,加热,收集到标准状况下的气体224 mL。然后,往溶液中通入足量CO2,过滤,将所得沉淀洗涤、烘干、灼烧,得白色固体0.51 g。
请回答:
(1)该结晶水合物中含有的两种阳离子是 、 ;一种阴离子是 。
(2)试通过计算确定该结晶水合物的化学式,请写出计算过程。
-
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素.甲溶于水后可电离出三种离子,其中一种由A、B组成的10电子阳离子.B元素有一种核素没有中子,A元素原子核内质子数比E的少1,D、E处于同主族.
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入适量NaOH溶液,加热;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀.
回答下列问题:
(1)D的元素符号是______,C在周期表中的位置______;
(2)用离子方程式表示实验②中现象的原因:______;______;
(3)实验③中出现的现象是______;
(4)经测定甲晶体的摩尔质量为392g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为______.
-
(13分)甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出三种离子,其中一种离子是由A、B两元素形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入足量NaOH溶液,加热,部分实验现象如下:产生有刺激气味的气体;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C的元素符号是 ,D在周期表中的位置: 周期 族
(2)用离子方程式表示实验②中现象的原因:________ 。
(3)实验③中出现的现象还有 。
(4)经测定甲晶体的摩尔质量为284 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
-
甲是一种盐,由A、B、C、D、E五种短周期元素元素组成。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示;

④取少量甲溶液于试管中,加入过量NaOH溶液并加热;
回答下列问题:
(1)D在周期表中的位置 写出化合物AB3的电子式
(2)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比1:1,且1 mol 甲晶体中含有12 mol结晶水。则甲晶体的化学式为 。
(3)实验③中根据图像得V(0a):V(ab):V(bc)= 。
(4)实验④中离子方程式是 。
-
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入适量NaOH溶液,加热;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C的元素符号是________,D在周期表中的位置________。
(2)用离子方程式表示实验②中现象的原因:。
(3)实验③中出现的现象是____。
(4)经测定甲晶体的摩尔质量为392 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为________。
-
(14分) A、B、C、D均为短周期的非金属元素,且原子序数依次增大。A、B可形成一种极易溶于水的碱性气体X,A、B、C元素可组成离子晶体,该晶体的化学式为A4B2C3;A和D可形成极易溶于水的酸性气体Y,X分子比Y分子少8个电子
(1)请写出四种元素的元素符号:A________B________C________D________
(2)用离子方程式表示A4B2C3的水溶液显酸性的原因________
(3)用电子式表示B2 ________用电子式表示ADC________
-
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:
①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
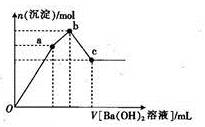
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为_ 。
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。 则晶体甲的化学式为_ _。
(3)图像中V(Oa):V(ab):V(bc)= _ 。
(4)写出ab段发生反应的离子方程式:_ 。
(5)配成的甲溶液物质的量浓度是_ 。

