-
(15分)氰化物有剧毒,氰化电镀会产生大量含氰化物的废水,该电镀含氰废水中的氰化物主要是以CN一和[Fe(CN)6]3-两种形式存在。研究表明可采用双氧水氧化法处理电镀含氰废水。某化学兴趣小组模拟双氧水氧化法探究有关因素对该破氰反应速率的影晌(破氰反应是指氧化剂将CN-氧化的反应)。
【查阅资料】
①Cu2+可作为双氧水氧化法废水处理过程中的催化剂;
②Cu2十在偏碱性条件下对双氧水分解影响较弱,可以忽略不计;
③[Fe(CN)6]3-较CN一难被双氧水氧化,pH越大,[Fe(CN)6]3-越稳定,越难被氧化。
[实脸设计]
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验编号 | 实验目的 | 初始pH | 废水样品体积mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积mL |
| ① | 为以下实验作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | | | | | | 10 |
【数据处理]
实验测得含氰废水中的总氰浓度(以CN一表示)随时间变化关系如下图所示。
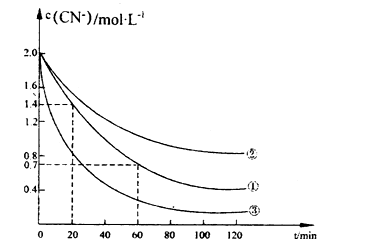
(2)实验①中20——60 min时间段反应速率v(CN-)= ____mol·L-1∙min-1。
【解释和给论]
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是______
(填一点即可)。
在偏碱性条件下,含氰废水中的CN一最终被双氧水氧化为HCO3- ,同时放出NH3,试写出该反应的离子方程式:
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实脸并验证上述结论,完成下表中内容。
(己知:废水中的CN一浓度可用离子色谱仪测定)
| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
-
(15分)氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN—等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
I.查阅资料:含氰化物的废水破坏性处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
II.实验验证:破坏性处理CN-的效果。
化学兴趣小组的同学在密闭系统中用图10装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
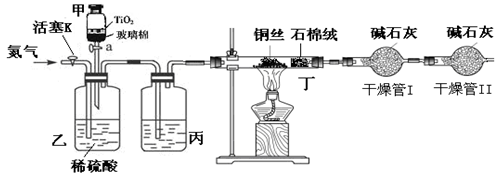
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol·L—1)倒入甲中,塞上橡皮塞。
步骤3:________
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式________。
(2)完成步骤3________。
(3)丙装置中的试剂是________,丁装置的目的是________。
(4)干燥管Ⅱ的作用是________。
(5)请简要说明实验中通入N2的目的是________。
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为________。
-
氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中.某化学小组同学对含氰化物废水处理进行研究.
I.查阅资料:含氰化物的废水破坏性处理方法.
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等.
II.实验验证:破坏性处理CN-的效果.
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
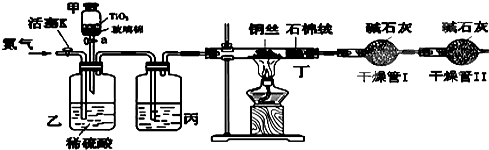
步骤1:取一定量废水进行加热蒸发、浓缩.
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL倒入甲中,塞上橡皮塞.
步骤3:______.
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞.
步骤5:打开活塞K,通一段时间N2,关闭活塞K.
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式______.
(2)完成步骤3______.
(3)丙装置中的试剂是______,丁装置的目的是______.
(4)干燥管Ⅱ的作用是______.
(5)请简要说明实验中通入N2的目的是______.
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为______.
-
氰化物是剧毒物质,传统生产工艺的电镀废水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl2氧化法处理这种废水,涉及两个反应:反应i,CN- +OH-+Cl2 OCN- +Cl-+H2O(未配平);
OCN- +Cl-+H2O(未配平);
反应ii,OCN- + OH-+ Cl2 X + Y + Cl-+ H2O(未配平)。
X + Y + Cl-+ H2O(未配平)。
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1: 1
B.X、Y是CO2、N2,且均为反应ii的氧化产物
C.该废水处理工艺过程中须采取措施,防止Cl2逸出到空气中
D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl2 4.48×103L
-
生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应)。
【相关资料】
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在。
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计。
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化。
【实验过程】
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(1)请完成以下实验设计表(表中不要留空格)。
| 实验序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | ________ | 7 | 60 | ______ | ______ | 10 |
实验测得含氰废水中的总氰浓度(以CN-表示)随时间变化关系如图所示。
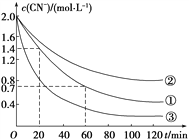
(2)实验①中20~60 min时间段反应速率:v(CN-)=______mol·L-1·min-1。
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是____________________(填一点即可)。在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO,同时放出NH3,试写出该反应的离子方程式:____________。
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他们设计实验并验证上述结论,完成下表中内容(已知:废水中的CN-浓度可用离子色谱仪测定) ______。
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
-
电镀产生的工业废水含有的重金属离子(Cu2+、Ni2+等)和CN形成难以除去的络合物,用电解法制备高铁酸钠(Na2FeO4)处理废水是目前比较先进的方法。已知氰化氢有毒易挥发。电解装置如图所示,下列选项正确的是( )
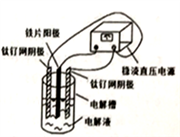
A. 铁片连接电源的负极
B. 电解时,每生成lmolFeO42-,转移电子3mol
C. CN被氧化成CO2和N2,Cu2+、Ni2+形成难溶碱而除去
D. 已知HFeO4-的氧化性比FeO42-更强,故pH<7时处理废水效率更高
-
氰化物有剧毒,我国工业废水中氰化物(CN-)的最高允许排放浓度为0.5 mg/L;对废水中CN-的处理方法是:在碱性条件下,用Cl2将废水的中CN-转化成N2和CO2等,使废水得到净化。发生的反应为:2CN- + 8OH-+ 5Cl2 = 2CO2 ↑+ N2 ↑+10 Cl-+ 4H2O ;下列有关说法正确的是( )
A.上述反应中氧化产物只有N2
B.经测定,NaCN的水溶液呈碱性,说明CN—能促进水的电离
C.若上述反应生成0.4 mol CO2,则溶液中阴离子增加的物质的量为2 mol
D.现取1 L含CN-1.04mg/L的废水,至少需用4.0×10-5mol Cl2处理后才符合排放标准
-
氰化物有剧毒,我国工业废水中氰化物(CN-)的最高允许排放浓度为0.5 mg/L。对废水中CN-的处理方法是:在碱性条件下,用Cl2将废水中的CN-转化成N2和CO2等,使废水得到净化。发生的反应为2CN-+8OH-+5Cl2===2CO2+N2+10Cl-+4H2O。下列有关说法不正确的是( )
A. 上述反应中氧化产物有N2和CO2
B. 经测定,NaCN的水溶液呈碱性,说明CN-能促进水的电离
C. 若上述反应生成0.4 mol CO2,则溶液中阴离子增加的物质的量为2 mol
D. 现取1 L含CN-1.02 mg/L的废水,至少需用5.0×10-5 mol Cl2处理后才符合排放标准
-
含氰根(CN−)的废水必须经处理后排放。某电镀废水pH≈12,氰化物以CN−、Cu(CN)32−等形式存在(均以CN−计),处理流程如下:

(1)HCN是一元弱酸,用离子方程式表示NaCN水溶液显碱性的原因:______。
(2)二次处理阶段,使用不同方法氧化。
①过硫酸钾(K2S2O8)氧化法:K2S2O8溶液将CN−(N为-3价)氧化成毒性弱的CNO−(N为-3价)。
Ⅰ.碱性溶液中S2O82−在一定条件下氧化CN−生成CNO−和SO42−的离子方程式是______。
Ⅱ.不同浓度的K2S2O8溶液对CN−的去除率如图1。工业上选用浓度为1 mmol·L−1
K2S2O8溶液,不用0.75 mmol·L−1和2 mmol·L−1的原因是______。

Ⅲ.研究CN−的氧化去除机理。(文献中为碱性条件下的结论)
文献:a.没有Cu+,S2O82−对CN−没有去除效果。
b.S2O82−和Cu+反应生成硫酸根自由基(SO4−·)和CuO。
c.SO4−·可能转变为羟基自由基(·OH)。
d.SO4−· 、·OH均可将CN−氧化为CNO−。叔丁醇只可以使·OH失
去活性,乙醇可以使SO4−· 、·OH均失去活性。
实验:相同条件下,向含Cu(CN)32−的碱性废水中加入叔丁醇,CN−的去除率没有影响;加入乙醇,CN−的去除率降低50%。两种不同的CN−的氧化去除机理如图2,结合文献和实验回答下列问题:
ⅰ.补全“机理一”_______________。
ⅱ.从“机理二”可看出CuO参与了去除CN−,列举其证据:______。
②电解法:碱性环境中,在阳极发生两步反应,CN−放电生成CNO−,CNO−再放电生成CO2和N2,第二步的阳极反应式是______。
-
氰化钠(NaCN)是一种重要化工原料,用于化学合成、电镀、冶金等方面。NaCN有剧毒,含氰废水需经无害化处理才能排放,某电镀厂含氰废水的一种工业处理流程如下:
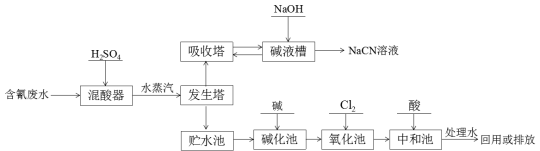
已知:HCNO的结构式是:H-O-C≡N
HCN的Ka = 6.02×10-10
[Ag(CN)2]-(aq)  Ag+(aq) + 2CN-(aq) K = 1.3×10-21
Ag+(aq) + 2CN-(aq) K = 1.3×10-21
回答下列问题:
(1)CN-中两原子均为8电子稳定结构,请写出CN-的电子式_____________________。
(2)氰化钠遇水会产生剧毒氢氰酸,请写出相应的离子方程式 。
(3)向发生塔中通水蒸汽的目的是 。
(4)氧化池中氰化物的降解分两步进行
CN-被氯气氧化成低毒的CNO- ,写出相应的离子方程式 ,
CNO-被氯气氧化成无毒的两种气体,写出相应的离子方程式
(5)贮水池中废水须先经碱化后再进行氧化的原因___________________________。
(6)电镀厂电镀银时需要降低镀层金属的沉积速度,使镀层更加致密。电解液使用Na[Ag(CN)2],请写出阴极反应式 ,解释工业电镀中使用氰离子(CN-)的原因 。







