-
含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目
。
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子方程式________
。
患者被送往医院后,医生往往让其服用________
(填题干所列7种物质中的1种)来解毒。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面________
,
则发生了钝化;若铁棒表面 ,则未发生反应。
高三化学填空题中等难度题查看答案及解析
-
用下图装置可以进行测定SO2转化成SO3的转化率。已知SO3的熔点是16.8℃,沸点是44.8℃。气体发生装置中所涉及反应的化学方程式为:Na2SO3(s) + H2SO4 → Na2SO4 + H2O + SO2↑。
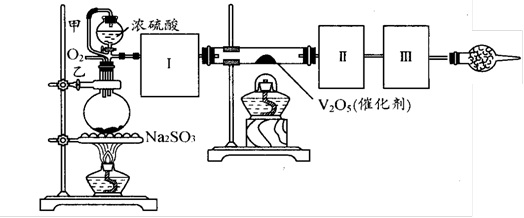
根据题意完成第35~40题:
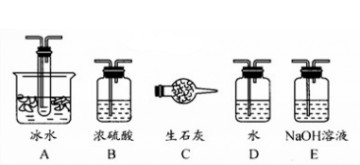
35.根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是________、_________、_________。
36.从乙处均匀通入O2,为使SO2有较高的转化率,实验中在:①加热催化剂;②滴加浓硫酸的顺序中,应采取的操作是先_______后_________(填编号)。
37.在制取SO3的过程中,若温度过高,SO2的转化率会________(填“升高”、“不变”或“降低”)。
38.实验结束后,如果取出收集SO3的仪器并敞口露置于空气中,能够看到的现象是:
__________________。
39.该实验一般使用较浓的硫酸制SO2,不可使用稀硫酸,简述其原因:___________。
40.用a mol Na2SO3粉末与足量较浓的硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了b g,则实验中SO2的转化率为________(用含a、b的代数式填写)。
高三化学选择题中等难度题查看答案及解析
-
下列各组物质能满足如图所示转化关系的是(图中箭头表示一步转化)
a
b
c
d
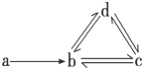
①
S
SO2
H2SO3
H2SO4
②
Si
SiO2
H2SiO3
Na2SiO3
③
Cu
CuO
CuSO4
Cu(OH)2
④
N2
NO
NO2
HNO3
A. ②③ B. ①④ C. ①② D. ③④
高三化学单选题中等难度题查看答案及解析
-
下列有关实验正确的是
A.装置用于Na2SO3和浓H2SO4反应制取少量的SO2气体
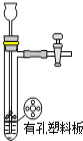
B.装置用于灼烧CuSO4·5H2O
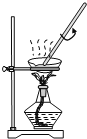
C.装置用于收集氯气并防止污染空气
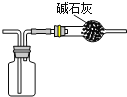
D.装置用于实验室制备少量乙酸乙酯
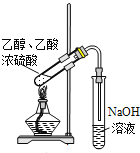
高三化学单选题中等难度题查看答案及解析
-
下列物质中的分类组合正确的是 ( )
A B C D
强电解质 HF CuSO4 H2SO4 BaSO4
弱电解质 HI CH3COOH CaCO3 NH3·H2O
非电解质 SO2 Cu H2O CH3CH2OH
高三化学选择题中等难度题查看答案及解析
-
下列各项关系中正确的是
A. 0.1 mol/L Na2SO3溶液中:c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3)=0.2 mol/L
B. 常温下,pH=a的稀H2SO4与pH=b的氨水等体积混合后恰好完全反应,则a+b<14
C. 0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合:
c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH)
D. pH相同的三种溶液①NH4Cl ②(NH4)2SO4 ③NH4HSO4,c(NH4+)大小关系为:①>②>③
高三化学选择题困难题查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
实验结论
A
将SO2通入紫色石蕊试液中,溶液变红
SO2与水反应生成H2SO3造成溶液显酸性
B
向久置的Na2SO3溶液中加入足量Ba(NO3)2溶液,出现白色沉淀,再加入足量稀盐酸,部分沉淀溶解
部分Na2SO3被氧化
C
向20%蔗糖溶液中加入少量稀H2SO4,加热,再加入银氨溶液,未出现银镜
蔗糖未水解
D
向某黄色溶液中加入淀粉 KI 溶液,溶液呈蓝色
溶液中含 Br2
A. A B. B C. C D. D
高三化学单选题中等难度题查看答案及解析
-
(10分)最近雾霾天气肆虐我国大部分地区,其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是 。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7,H2CO3的电离常数为K1=4.30×10-7,K2=15.60×10-11,则下列微粒可以大量共存的是 (填序号)
A.CO32- 、HSO3- B.HSO3- 、HCO3- C.SO32- 、HCO3- D.HCO3-、H2SO3
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-)
91:9
1:1
9:91
pH
8.2
7.2
6.2
①根据上表判断NaHSO3溶液显 性,试解释原因
②在NaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(H2SO3)+c(H+)= c(SO32-)+c(OH-)
C.c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)
D.c(H+)+ c(Na+)=2c(SO32-)+c(HSO3-)+ c(OH-)
高三化学填空题困难题查看答案及解析
-
下列有关实验操作、实验现象和结论都正确的是 ( )。
选项 实验操作 实验现象 结论
A 在Ba(NO3)2溶液中分别滴入H2SO3和H2SO4溶液 均有白色沉淀 沉淀均为BaSO4
B 混合装有Cl2和NH3两集气瓶中的气体 产生大量白烟 NH3显还原性和碱性
C 溶液X中滴入盐酸酸化的FeCl3溶液,再滴入淀粉溶液 溶液变蓝色 溶液X中一定含有I-
D 向浓度均为0.01 mol·L-1的NaCl和Na2S的混合溶液中滴入少量AgNO3溶液 出现黑色沉淀 Ksp(Ag2S)> Ksp(AgCl)
高三化学选择题中等难度题查看答案及解析
-
下列根据实验操作和现象所得出的结论正确的是
选项 实验操作 实验现象 结论
A 在Ba(NO3)2溶液中分别滴入H2SO3及H2SO4溶液 均有白色沉淀 沉淀均为BaSO4
B 混合装有Cl2和NH3量集气瓶中的气体 产生大量白烟 NH3显还原性和碱性
C 溶液X中滴入盐酸酸化的FeCl2溶液,再滴入淀粉溶液 溶液变蓝色 溶液X中一定含有I-
D 向浓度居委0.01mol/LNaCl和Na2S的混合溶液中滴入少量AgNO3 出现黑色沉淀 Ksp(Ag2S)>Ksp(AgCl)
高三化学选择题中等难度题查看答案及解析