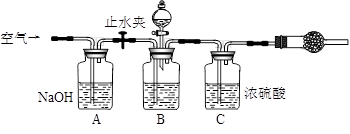-
现有一瓶含NaCl杂质的Na2CO3样品,某同学设计了一种测定其纯度的方法,装置如下图,其中A容器中盛有样品10.0 g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。
(1)该同学重复操作了三次,每次操作均正确,且装置不漏气,可是结果数据出现了较大偏差(容器内反应均完全,装置内空气的影响忽略不计),请你分析可能的原因______。
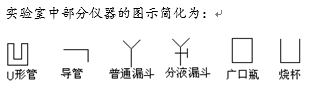
(2)通过仔细分析,该同学重新设计了一套实验装置如下图,请回答有关问题:
(可供选择的试剂还有Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水)
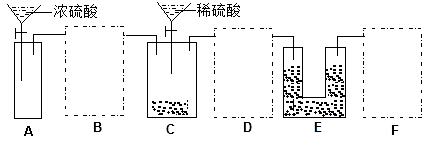
①该套装置未画完整,请在你认为需要补充装置的虚框内画出合适的简图,并注明试剂。______
②A装置的广口瓶中应加入的试剂是__________;该装置的作用是________________。
③如果实验后测得E装置质量增重3.52 g,则该Na2CO3试样的纯度为__________。
(3)测定该Na2CO3试样纯度的方法有多种,请你利用不同的反应原理再设计一套方案。
要求写出实验操作流程和试样中Na2CO3纯度的表达式__________。(试剂任选)
操作流程按下列图示表述:

①操作流程为:

②实验时称量样品的质量为a克,所测物质的质量为b克,该试样中Na2CO3纯度的表达式为:__________。
-
现有一份NaOH固体样品,里面混有少量的Na2CO3、NaCl杂质,某同学用中和滴定的方法来测定NaOH的纯度。其操作如下:
①称取a g样品放入锥形瓶中,加水,振荡,使固体充分溶解。
②向该溶液中加入足量的BaCl2溶液,使CO 沉淀完全。
沉淀完全。
③向所得混合液中滴入2~3滴酚酞指示剂,然后用c mol·L-1的盐酸进行滴定。
④当反应达终点时,测得消耗盐酸的体积为V mL。
⑤计算样品的纯度。
试回答下面的问题
(1)滴定终点时溶液颜色如何变化:_____________________________________________。
(2)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,是否会对NaoH的含量测定造成影响(填“是”或“否”)___________,理由是_______________________________。
(3)第②步中生成的BaCO3沉淀未过滤出来就直接用盐酸滴定,能否改用甲基橙作指示剂(填“能”或“否”)__________。若改用甲基橙作指示剂则实验结果_______________(填“偏大”、“偏小”或“不变”)。
(4)根据上述实验数据,写出计算NaOH纯度的表达式
__________________________________。
-
(10分)工业纯碱中常常含有NaCl、Na2SO4等杂质。为测定某工业纯碱的纯度,设计了如下图实验装置。
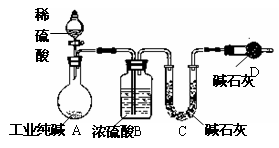
依据实验设计,请回答:
(1)装置中盛装稀硫酸的仪器名称是________;
装置D的作用是________
________。
(2)为达到测定某工业纯碱的纯度实验目的,一次实验中至少应 进行称量操作的次数为________。
(3)若不考虑操作、药品及其用量等方面
的影响,该实验测得结果会(填“偏高”、“偏低”、“无影响”);
原因是________
(你若认为无影响,该空不用回答)。
-
(18分)工业生产的纯碱中常含有少量NaCl杂质。为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
【方案一】取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量。
【方案二】用0.100 mol/L盐酸滴定。
【方案三】用稀酸将CO32-转化为CO2,测定CO2的质量。
解答1-4小题:
1.方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。称量时所需定量实验仪器为____________________。判断是否达到恒重的标准是_____________________________________________________。
2.方案二的具体过程为:
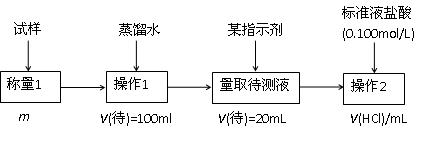
①操作1所需要的仪器有_____________________________________________。
②滴定时选择的指示剂为甲基橙。当溶液____________________________________时,说明达到了滴定终点。
③为减少偶然误差,通常的处理办法是_______________________________。
④滴定时若锥形瓶内有少量液体溅出,则测定结果_________。(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果_________。
3.方案三的实验装置如下图:
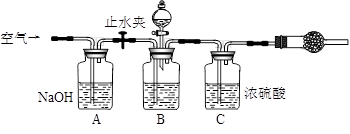
操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H2SO4至不再产生气体为止;⑥ 打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g。
该方案样品中纯碱的质量分数为__________________________(用代数式表示)。
上图中装置A的作用是_____________________。装置C的作用是_____________________。有同学认为空气中的水蒸气会进入干燥管导致测量结果_____________(填“偏大”、“偏小”或“无影响”)。改进措施可以是______________________________________________。
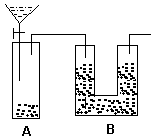
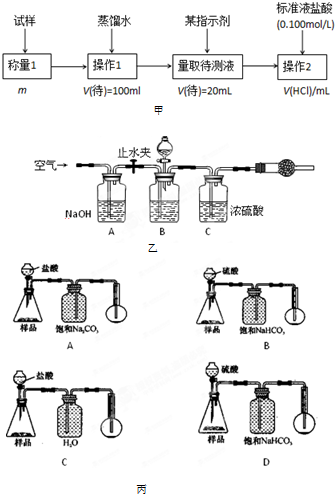
4.若用下图装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量。则下列装置中,最合理的是______。(选填序号)
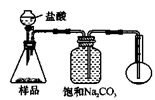
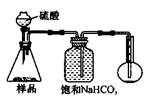
A B
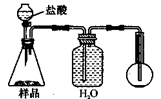
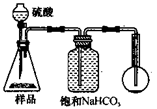
C D
-
工业生产的纯碱中常含有少量NaCl杂质.为测定某纯碱样品的纯度,化学课外活动小组设计了两种实验方案:
【方案一】取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量.
【方案二】用稀酸将CO32-转化为CO2,测定CO2的质量.
(1)方案一的操作步骤有:①称量样品W1 g并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量沉淀W2 g并进行恒重操作,最后称量沉淀W3 g.
称量时所需定量实验仪器为______.根据方案一的数据,算出样品中纯碱的质量分数为______(用代数式表示).
(2)方案二的实验装置如图:
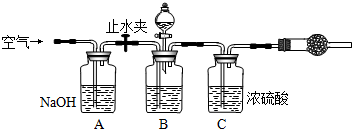
操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④缓缓鼓入空气数分钟;⑤关闭止水夹,缓慢加入稀H2SO4至不再产生气体为止;⑥打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g.
根据方案二的数据,算出样品中纯碱的质量分数为______(用代数式表示).图中装置A的作用是______.装置C的作用是______.如果没有装置A和实验操作④⑦,会导致测量结果______(填“偏大”、“偏小”或“无影响”).有同学认为空气中的水蒸气会进入干燥管导致测量结果______(填“偏大”、“偏小”或“无影响”),改进措施可以是______.
-
工业生产的纯碱中常含有少量NaCl杂质.为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
方案一:取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量.
方案二:用0.100mol/L盐酸滴定.
方案三用稀酸将CO32-转化为CO2,测定CO2的质量.
(1)方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作.称量时所需定量实验仪器为______.判断是否达到恒重的标准是______.
(2)方案二的具体过程如图甲:
①操作1所需要的仪器有______.
②滴定时选择的指示剂为甲基橙.当溶液______时,说明达到了滴定终点.
③为减少偶然误差,通常的处理办法是______.
④滴定时若锥形瓶内有少量液体溅出,则测定结果______.(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果______.
(3)方案三的实验装置如图乙:操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H2SO4至不再产生气体为止;⑥打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g.该方案样品中纯碱的质量分数为______(用代数式表示).上图中装置A的作用是______.装置C的作用是______.有同学认为空气中的水蒸气会进入干燥管导致测量结果______(填“偏大”、“偏小”或“无影响”).改进措施可以是______.
(4)若用如图丙装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量.则下列装置中,最合理的是______.(选填序号)
-
为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙二位同学设计了二种不同的实验方案.
已知:2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═4NaOH+O2
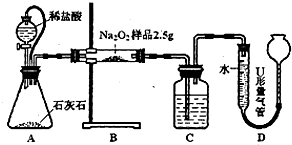
甲:用图l所示装置,通过测定Na2O2与CO2反应生成O2的体积来测定样品的纯度.
(1)C中所盛的药品是:______.
(2)A中橡皮管的作用是:______.
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是______(填选项字母).
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙:称取3.500g试样,配成1000.00mL溶液,用0.1000mol•L-1的标准盐酸滴定.
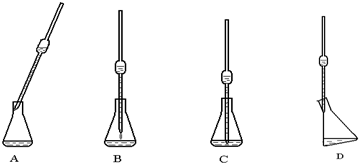
(4)取上述所配溶液25.00mL于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图______,取溶液所用仪器的名称是______.
(5)滴定操作平行实验的数据记录如下表:
| 滴定次数 | 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
由表中数据计算样品中Na2O2纯度为______.
-
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量10.0 g 含有少量易溶杂质的样品(杂质不与盐酸反应),配成500mL待测溶液。称量时,样品可放在________(填编号字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定时,用0.2000 mol/L的盐酸来滴定待测溶液,不可选用________(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中,眼睛应注视________________________________________________;在铁架台上垫一张白纸,其目的是__________________________________________。
(4)根据下表中数据,计算被测烧碱溶液的物质的量浓度是________mol/L,烧碱样品的纯度是________。
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) |
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
(5)在中和滴定操作过程中,有以下各项因操作不当引起的实验误差,用“偏高”、“偏低”或“无影响”等填空:
①滴定管用蒸馏水洗净后,未用已知浓度的标准溶液润洗,使滴定结果__________。
②锥形瓶未用待装溶液润洗,使滴定结果__________。
③装标准溶液的滴定管在滴定前尖嘴处有气泡,滴定终了无气泡,使滴定结果__________。
④滴定前平视凹液面,滴定终了俯视凹液面,使滴定结果___________________。
-
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量10.0g含有少量中性易溶杂质的样品,配成500mL待测溶液。 用0.100mol L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
(2)将该烧碱样品配成500mL待测溶液需要的玻璃仪器有________________________。
(3)滴定过程中,眼睛应注视_________________________,若用酚酞作指示剂达到滴定终点颜色变化是______________________________________________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________molL-1,烧碱样品的纯度是___________。
| 滴定次数 | 待测溶液 体积(mL) | 标准酸体积 |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) |
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
① 观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果____________。
② 若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果____________。
-
某学生用中和滴定法测定某烧碱样品的纯度。先准确称量10.0g含有少量中性易溶杂质的样品,配成500mL待测溶液。用0.200mol/L的盐酸标准液滴定待测液,滴定时用酚酞做指示剂。试根据实验回答下列问题:
(1)下列有关滴定操作的顺序正确的是
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液
③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④ B.③⑤①②④ C.③⑤②①④ D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视_________,本实验滴定达到终点的标志是_________________________。
(3)根据下表数据,计算被测烧碱溶液的物质的量浓度是 ,烧碱样品的纯度是___________
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 |
| 滴定前刻度(mL) | 滴定后刻度(mL) |
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| 第三次 | 10.00 | 0.20 | 24.20 |
| | | |
(4)若该实验修改成“用待测碱液滴定盐酸标准液”,则下列操作会使烧碱样品纯度偏高的是
A.锥形瓶用蒸馏水洗净后,先用盐酸标准液润洗再装标准液。
B.碱式滴定管用蒸馏水洗净后未润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前仰视碱式滴定管读数,滴定后俯视滴定管读数