-
在四个恒容密闭容器中按左下表相应量充入气体,发生反应2N2O(g) 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如下图所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如下图所示:
| 容器 | 容积/L | 起始物质的量/mol |
| N2O | N2 | O2 |
| Ⅰ | V1 | 0.1 | 0 | 0 |
| Ⅱ | 1.0 | 0.1 | 0 | 0 |
| Ⅲ | V3 | 0.1 | 0 | 0 |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 |
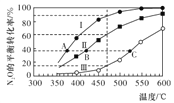
下列说法正确的是
A. 该反应的正反应放热
B. 相同温度下反应相同时间,平均反应速率:v(Ⅰ)>v(Ⅱ)
C. 容器Ⅳ在470℃进行反应时,起始反应速率:v正(N2O)<v逆(N2O)
D. 图中A、B、C三点处容器内总压强:pA(I)< pB(Ⅱ)<pC(Ⅲ)
-
在一定条件下,N2和O2于密闭容器中发生如下反应:2N2(g)+O2(g) 2N2O(g)。下列说法能说明该反应达到化学平衡状态的有
2N2O(g)。下列说法能说明该反应达到化学平衡状态的有
A.反应不再进行 B.反应体系中的c(N2)不再发生变化
C.c(N2O) = c(N2) D.N2O的分解速率与生成速率相等
-
在一定条件下,N2和O2于密闭容器中发生如下反应:2N2(g)+O2(g) 2N2O(g)。下列说法能说明该反应达到化学平衡状态的有
2N2O(g)。下列说法能说明该反应达到化学平衡状态的有
A. 反应不再进行 B. 反应体系中的c(N2)不再发生变化
C. c(N2O) = c(N2) D. N2O的分解速率与生成速率相等
-
在恒温恒容密闭容器中发生反应2NO2 2NO+O2,不能说明反应达到平衡状态的是( )
2NO+O2,不能说明反应达到平衡状态的是( )
A. 2v(O2)=v(NO2) B. 单位时间内生成n mol O2的同时生成2n molNO2
C. 混合气体的颜色不再改变 D. 混合气体的平均相对分子质量不再改变
-
在恒容密闭容器中发生反应2NO2  2NO+O2,下列所述可以说明反应达到平衡状态的是
2NO+O2,下列所述可以说明反应达到平衡状态的是
A.单位时间内生成n molO2的同时生成2n molNO
B.混合气体的平均相对分子质量不再改变
C.混合气体的颜色不再改变
D.混合气体的密度不再改变
-
在2L的密闭容器中放入4mol N2O5,发生如下反应:2N2O5(g)⇌4NO2(g)+O2(g).反应5min后,测得N2O5转化了20%,求:
(1)υ(NO2)、υ(O2)分别为多少?
(2)5min时,N2O5占混合气体总体积的百分比是多少?
-
在恒温下的密闭容器中,有可逆反应:2NO2 N2O4,下列不能说明反应达到了平衡状态的是 ( )
N2O4,下列不能说明反应达到了平衡状态的是 ( )
A.N2O4生成速率与N2O4分解速率相等时
B.混合气体平均相对分子质量保持不变时
C.NO2的分子数与N2O4分子数比为2∶1时
D.体系颜色不再发生改变时
-
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)  4NO2(g)+O2(g)△H>0,T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g)△H>0,T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)mol/L | 5.00 | 3.53 | 2.50 | 2.50 |
下列说法中不正确的是:
A. T1温度下,500s时O2的浓度为0.74mol/L
B. 平衡后其他件不变,将容器的体积压缩到原来的1/2,则再平衡时c(N2O5)>5.00 mol/L
C. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
D. T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为0.5
-
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g) △H>0一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s[K] | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
下列说法中错误的是
A.500 s时O2的浓度为0.075 mol/L
B.平衡后,升高温度,正反应速率先增大后减小
C.平衡后,要使平衡常数增大,改变的条件是升高温度
D.1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L
-
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)  4NO2(g) + O2(g) △H =+Q kJ/mol (Q>0),某温度下,向2L的密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g) + O2(g) △H =+Q kJ/mol (Q>0),某温度下,向2L的密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol/L | 5.0 | 3.5 | 2.5 | 2.5 |
下列说法正确的是
A. 500s内N2O5分解速率为6×10-3mol/(L·s)
B. 该温度下的平衡常数K =125
C. 反应达平衡时,吸收的热量为5Q kJ
D. 其他条件不变,若开始时c(N2O5)=10mol/L,则达平衡后c(N2O5)=5mol/L
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如下图所示:
